 是元素周期表中的短周期元素,其性质或结构信息如下表,回答下列问题:
是元素周期表中的短周期元素,其性质或结构信息如下表,回答下列问题:| 元素 | X | Y | Z | V | W |
| 性质信息 | 单质为有色气体,有毒,可用于自来水消毒 | 日常生活中常见金属,熔化时并不滴落,好像有一层膜兜着 | 其单质在空气中约占 左右 左右 | 单质为淡黄色晶体,质脆,不溶于水,微溶于酒精 | 位于第ⅣA,是形成的化合物最多的元素之一 |
(1)
 离子结构示意图为
离子结构示意图为(2)
 、Y和V三元素中原子半径由大到的小顺序为
、Y和V三元素中原子半径由大到的小顺序为 用元素符号表示
用元素符号表示
(3)以上五种元素中,它的氢化物与其最高价氧化物的水化物能反应生成盐的是
 填元素符号
填元素符号 以上五种元素的最高价氧化物的水化物中,酸性最强的是
以上五种元素的最高价氧化物的水化物中,酸性最强的是 填化学式
填化学式 。
。(4)
 是一种常见的溶剂。已知
是一种常见的溶剂。已知 在氧气中完全燃烧,生成
在氧气中完全燃烧,生成 和
和 ,若
,若 在
在 中完全燃烧,则所得气体混合物在标准状况下的体积为
中完全燃烧,则所得气体混合物在标准状况下的体积为
更新时间:2022-08-25 11:04:24
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分,请参照元素①—⑧在表中的位置,用化学用语回答下列问题:
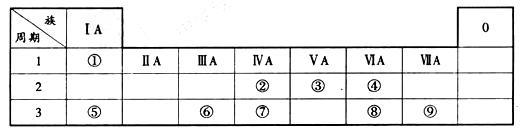
(1)④、⑤、⑥的原子半径由大到小的顺序为(填元素符号)________ 。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是(填化学式)________ 。
(3)①、④,⑤、⑨中的某些元素可形成既含离子键又含共价键的化合物,写出其中任意一种化合物的电子式:________ 。
(4)由②和④组成,且②和④的质量比为3:8的化合物的结构式是________ 。
(5)⑥单质与⑤的最高价氧化物的水化物反应的离子方程式为_________ 。
(6)⑧、⑨两元素非金属性较强的是(写元素符号)_____ ,举二个例子说明推断依据:_______ 。

(1)④、⑤、⑥的原子半径由大到小的顺序为(填元素符号)
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是(填化学式)
(3)①、④,⑤、⑨中的某些元素可形成既含离子键又含共价键的化合物,写出其中任意一种化合物的电子式:
(4)由②和④组成,且②和④的质量比为3:8的化合物的结构式是
(5)⑥单质与⑤的最高价氧化物的水化物反应的离子方程式为
(6)⑧、⑨两元素非金属性较强的是(写元素符号)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】如表是元素周期表的一部分,回答下列有关问题:
(1)写出⑥的元素符号:_______ ,画出⑨的原子结构示意图_______ 。
(2)写出③的单质在空气中燃烧后产物的电子式:_______ 。
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的是_______ ,呈两性氢氧化物的是_______ 。(填化学式)
(4)用电子式表示出④的氯化物的形成过程:_______ 。
(5)写出实验室制取⑧的单质的化学方程式:_______ 。
| 周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)写出③的单质在空气中燃烧后产物的电子式:
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的是
(4)用电子式表示出④的氯化物的形成过程:
(5)写出实验室制取⑧的单质的化学方程式:
您最近一年使用:0次
【推荐3】1869年,俄国化学家门捷列夫提出了元素周期律,并在此基础上发表了第一张元素周期表。为了纪念元素周期表诞生150年,联合国将2019年定为“国际化学元素周期表年”,并认为元素周期表是“科学共同的语言”。 、Ⅱ
、Ⅱ 元素属于
元素属于___________ 区。
②2017年5月9日我国发布了113号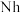 、115号
、115号 、117号
、117号 、118号
、118号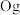 四种元素,则下列说法正确的是
四种元素,则下列说法正确的是___________ (填字母序号)。
a.113号元素在周期表中的位置是第七周期Ⅴ 族
族
b.117号元素 位于金属与非金属分界线上,属于准金属,可能是半导体
位于金属与非金属分界线上,属于准金属,可能是半导体
c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:
(2)认识原子结构与元素周期表的关系:见表中元素 的信息,其中“
的信息,其中“ ”称为该元素原子的
”称为该元素原子的___________ ,该元素 能层上具有
能层上具有___________ 种不同运动状态的电子。
(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:
___________  (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是___________ 。
②前四周期同族元素的某种性质 随核电荷数的变化趋势如图所示,则下列说法正确的是
随核电荷数的变化趋势如图所示,则下列说法正确的是___________ (填字母)。 、
、 、
、 表示氧族元素,则
表示氧族元素,则 表示对应氢化物的稳定性
表示对应氢化物的稳定性
B.若 、
、 、
、 表示卤族元素,则
表示卤族元素,则 表示对应简单离子的还原性
表示对应简单离子的还原性
C.若 、
、 、
、 表示第Ⅰ
表示第Ⅰ 族元素,则
族元素,则 表示对应离子的氧化性
表示对应离子的氧化性
D.若 、
、 、
、 表示第Ⅱ
表示第Ⅱ 族元素,则
族元素,则 表示最高价氧化物对应水化物的碱性
表示最高价氧化物对应水化物的碱性

 、Ⅱ
、Ⅱ 元素属于
元素属于②2017年5月9日我国发布了113号
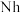 、115号
、115号 、117号
、117号 、118号
、118号 四种元素,则下列说法正确的是
四种元素,则下列说法正确的是a.113号元素在周期表中的位置是第七周期Ⅴ
 族
族b.117号元素
 位于金属与非金属分界线上,属于准金属,可能是半导体
位于金属与非金属分界线上,属于准金属,可能是半导体c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:

(2)认识原子结构与元素周期表的关系:见表中元素
 的信息,其中“
的信息,其中“ ”称为该元素原子的
”称为该元素原子的 能层上具有
能层上具有(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:

 (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是②前四周期同族元素的某种性质
 随核电荷数的变化趋势如图所示,则下列说法正确的是
随核电荷数的变化趋势如图所示,则下列说法正确的是
 、
、 、
、 表示氧族元素,则
表示氧族元素,则 表示对应氢化物的稳定性
表示对应氢化物的稳定性B.若
 、
、 、
、 表示卤族元素,则
表示卤族元素,则 表示对应简单离子的还原性
表示对应简单离子的还原性C.若
 、
、 、
、 表示第Ⅰ
表示第Ⅰ 族元素,则
族元素,则 表示对应离子的氧化性
表示对应离子的氧化性D.若
 、
、 、
、 表示第Ⅱ
表示第Ⅱ 族元素,则
族元素,则 表示最高价氧化物对应水化物的碱性
表示最高价氧化物对应水化物的碱性
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】元素是构成我们生活的世界中一切物质的“原材料”。
(1)自18世纪以来,科学家们不断探索元素之谜。通过从局部到系统 的研究过程,逐渐发现了元素之间的内在联系。下面列出了几位杰出科学家的研究工作。
上述科学家的研究按照时间先后排序合理的是_________ (填数字序号)。
(2)1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,如图所示。
①门捷列夫将已有元素按照相对原子质量排序,同一_________ (填“横行”或“纵列”)元素性质相似。结合表中信息,猜想第4列方框中“?=70”的问号表达的含义是_________ ,第5列方框中“Te=128?” 的问号表达的含义是_________ 。
②到20世纪初,门捷列夫周期表中为未知元素留下的空位逐渐被填满。而且,随着原子结构的逐渐揭秘,科学家们发现了元素性质不是随着相对原子质量 递增呈现周期性变化,而是随着原子序数 (核电荷数)递增呈现周期性变化。其本质原因是_________ (填字母序号)。
A.随着核电荷数递增,原子核外电子排布呈现周期性变化
B.随着核电荷数递增,原子半径呈现周期性变化
C.随着核电荷数递增,元素最高正化合价呈现周期性变化
(3)在现有的元素周期表中有A、B、D、E、X、Y、Z七种短周期元素。X与Y处于同一周期,Y的最高价氧化物的水化物与强酸、强碱均能反应。Z的单质常温下为气态,同条件下相对于氢气的密度比为35.5。其余信息如图所示:
①上述七种元素中,处于第二周期的有_________ (用元素符号表示,下同),X在周期表中的位置是_________ 。
②E的原子结构示意图为_________ ,写出Z元素气态氢化物的电子式:_________ 。
③B单质与E的最高价氧化物的水化物在一定条件下发生反应的化学方程式为_________ ;Y单质与X的最高价氧化物的水化物溶液反应的离子方程式为_________ 。
④B和D的最高价氧化物的水化物的化学式分别为_________ 、_________ ,二者酸性前者_________ (填“强于”或“弱于”)后者,原因是B和D的非金属性有差异,利用原子结构解释产生差异的原因: _________ 。
(1)自18世纪以来,科学家们不断探索元素之谜。通过
序号 | ① | ② | ③ | ④ |
科学家 | 纽兰兹 | 道尔顿 | 德贝莱纳 | 尚古尔多 |
工作 | 发现“ | 创立 | 发现了5组性质相似的“ | 认为 |
上述科学家的研究按照时间先后排序合理的是
(2)1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,如图所示。

①门捷列夫将已有元素按照相对原子质量排序,同一
②到20世纪初,门捷列夫周期表中为未知元素留下的空位逐渐被填满。而且,随着原子结构的逐渐揭秘,科学家们发现了元素性质不是随着
A.随着核电荷数递增,原子核外电子排布呈现周期性变化
B.随着核电荷数递增,原子半径呈现周期性变化
C.随着核电荷数递增,元素最高正化合价呈现周期性变化
(3)在现有的元素周期表中有A、B、D、E、X、Y、Z七种短周期元素。X与Y处于同一周期,Y的最高价氧化物的水化物与强酸、强碱均能反应。Z的单质常温下为气态,同条件下相对于氢气的密度比为35.5。其余信息如图所示:

①上述七种元素中,处于第二周期的有
②E的原子结构示意图为
③B单质与E的最高价氧化物的水化物在一定条件下发生反应的化学方程式为
④B和D的最高价氧化物的水化物的化学式分别为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】有A、B、C、D、E、F、G 7种元素,试按下述所给的条件推断:
①A、B、C是同一周期的金属元素,已知原子核外均有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;
②D、E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体;
④G是除氢外原子半径最小的主族元素
(1)A的名称是____ ,B位于周期表中位置 _________ ,C的原子结构示意图是________________ 。
(2)A元素与D元素形成的化合物的电子式是_________ 。
(3)G的单质与水反应的化学方程式是________ 。
(4)在上述七种元素中,最高价氧化物对应的水化物碱性最强的是_____ (填化学式,下同),气态氢化物最稳定的是__________ 。
(5)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是_______________ 。
①A、B、C是同一周期的金属元素,已知原子核外均有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;
②D、E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体;
④G是除氢外原子半径最小的主族元素
(1)A的名称是
(2)A元素与D元素形成的化合物的电子式是
(3)G的单质与水反应的化学方程式是
(4)在上述七种元素中,最高价氧化物对应的水化物碱性最强的是
(5)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E、F为1~20元素中的6种,其原子序数依次增大。A、B元素形成的化合物是“可燃冰”的主要成分;C、E同主族,且它们的化合物是形成酸雨的主要物质;E、D、F原子半径依次增大,D、F单质均可与冷水反应生成气体,且F单质反应比D单质剧烈。
(1)F的元素名称是_________ ,它在元素周期表中的位置是________ 。
(2)C与D可形成D2C和D2C2两种化合物,D2C2中含化学键的类型有_________ ,D2C的电子式为_________ 。
(3)C、D、E的简单离子按离子半径从大到小的顺序排列为_________ (填离子符号)。
(4)F与A2C反应的化学方程式是_________ 。
(5)E的最高价含氧酸的浓溶液具有强氧化性,可与B的单质在加热条件下反应,写出该化学方程式_________ 。
(1)F的元素名称是
(2)C与D可形成D2C和D2C2两种化合物,D2C2中含化学键的类型有
(3)C、D、E的简单离子按离子半径从大到小的顺序排列为
(4)F与A2C反应的化学方程式是
(5)E的最高价含氧酸的浓溶液具有强氧化性,可与B的单质在加热条件下反应,写出该化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】现有X、Y、Z、W、M、N六种短周期主族元素,其原子序数依次增大。X的简单氢化物可用作制冷剂,Z的最高价氧化物对应的水化物为强碱,W形成的简单离子在同周期中半径最小,M与Y同主族,M的最高正化合价与最低负价的代数和为4。
(1)元素x在周期表中的位置__________ , 上述元素 中最高价氧化物对应的水化物酸性最强的是_____________ (填化学式)。
(2)写出由Y、Z两种元素形成的淡黄色固体的电子式__________ 。
(3)写出工业上用电解ZN的水溶液制备N单质的化学方程式:____________________ 。
(4)由Y、Z、M三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气体产生,该盐的化学式为____________________ 。
(5)用化学平衡移动原理解释N的单质难溶于ZN的饱和溶液的原因:____________________ 。
(6)向KI溶液中通入适量的N单质后,再滴加一定量的CCl4,振荡静置后溶液分层,下层为紫色,继续通入N单质并充分振荡,混合溶液逐渐褪为无色,若反应中1 mol还原剂转移10 mol电子,写出该反应的化学反应方程式:______________ 。
(1)元素x在周期表中的位置
(2)写出由Y、Z两种元素形成的淡黄色固体的电子式
(3)写出工业上用电解ZN的水溶液制备N单质的化学方程式:
(4)由Y、Z、M三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气体产生,该盐的化学式为
(5)用化学平衡移动原理解释N的单质难溶于ZN的饱和溶液的原因:
(6)向KI溶液中通入适量的N单质后,再滴加一定量的CCl4,振荡静置后溶液分层,下层为紫色,继续通入N单质并充分振荡,混合溶液逐渐褪为无色,若反应中1 mol还原剂转移10 mol电子,写出该反应的化学反应方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,请参照元素①——⑨在表中的位置,回答问题
(1)表中⑧是用于半导体材料的元素,其元素符号为____ ,其在周期表中的位置是____ 。
(2)②、③、④的原子半径最小是____ (填元素符号),其原子结构示意图是____ 。
(3)⑤、⑥、⑦的最高价氧化物对应的水化物,碱性最强的是____ (填化学式)。
(4)①和③形成的原子个数比为1:1的化合物的电子式为____ 。
(5)⑤和⑨形成的化合物属于____ (填“离子化合物”或“共价化合物”),用电子式表示其形成过程____
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)表中⑧是用于半导体材料的元素,其元素符号为
(2)②、③、④的原子半径最小是
(3)⑤、⑥、⑦的最高价氧化物对应的水化物,碱性最强的是
(4)①和③形成的原子个数比为1:1的化合物的电子式为
(5)⑤和⑨形成的化合物属于
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、M、Q、R 是 6 种短周期元素,其原子半径及主要化合价如下:
(1)元素 X 在元素周期表中的位置是_____
(2)元素 M 组成的单质的电子式为_____
(3)单质铜和元素M的最高价氧化物对应水化物的稀溶液发生反应的离子方程式为_________________
(4)元素Q和R形成的化合物A是果实催熟剂,用A制备乙醇的化学方程式是_____
(5)元素Q、元素 Z 的含量影响钢铁性能,若钢样中元素 Z 以 FeZ 的形式存在,高温下在过量空气中反应生成ZO2和一种红棕色的氧化物,则反应的化学方程式是_____
| 元素代号 | X | Y | Z | M | Q | R |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.075 | 0.077 | 0.037 |
| 主要化合价 | +2 | +3 | +6,-2 | +5,-3 | +4,-4 | +1 |
(2)元素 M 组成的单质的电子式为
(3)单质铜和元素M的最高价氧化物对应水化物的稀溶液发生反应的离子方程式为
(4)元素Q和R形成的化合物A是果实催熟剂,用A制备乙醇的化学方程式是
(5)元素Q、元素 Z 的含量影响钢铁性能,若钢样中元素 Z 以 FeZ 的形式存在,高温下在过量空气中反应生成ZO2和一种红棕色的氧化物,则反应的化学方程式是
您最近一年使用:0次



