X、Y、Z、M、Q、R 是 6 种短周期元素,其原子半径及主要化合价如下:
(1)元素 X 在元素周期表中的位置是_____
(2)元素 M 组成的单质的电子式为_____
(3)单质铜和元素M的最高价氧化物对应水化物的稀溶液发生反应的离子方程式为_________________
(4)元素Q和R形成的化合物A是果实催熟剂,用A制备乙醇的化学方程式是_____
(5)元素Q、元素 Z 的含量影响钢铁性能,若钢样中元素 Z 以 FeZ 的形式存在,高温下在过量空气中反应生成ZO2和一种红棕色的氧化物,则反应的化学方程式是_____
| 元素代号 | X | Y | Z | M | Q | R |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.075 | 0.077 | 0.037 |
| 主要化合价 | +2 | +3 | +6,-2 | +5,-3 | +4,-4 | +1 |
(2)元素 M 组成的单质的电子式为
(3)单质铜和元素M的最高价氧化物对应水化物的稀溶液发生反应的离子方程式为
(4)元素Q和R形成的化合物A是果实催熟剂,用A制备乙醇的化学方程式是
(5)元素Q、元素 Z 的含量影响钢铁性能,若钢样中元素 Z 以 FeZ 的形式存在,高温下在过量空气中反应生成ZO2和一种红棕色的氧化物,则反应的化学方程式是
更新时间:2020-05-27 12:16:39
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应。
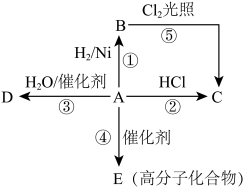
回答下列问题:
(1)写出C、D、E的结构简式:C__________ ,D__________ ,E__________ 。
(2)写出②③两步反应的化学方程式,并注明反应类型:
②_________ (反应类型__________ )。
③_________ (反应类型__________ )。

回答下列问题:
(1)写出C、D、E的结构简式:C
(2)写出②③两步反应的化学方程式,并注明反应类型:
②
③
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐2】乙烯产量是衡量一个国家石油化工水平的标志,根据乙烯的转化图,完成下列问题:______ 。
(2)反应④的化学方程式为______ 。反应类型为______ 反应。
(3)下列有关说法正确的是______。
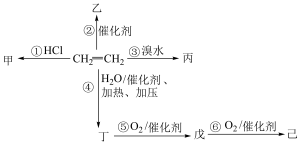
(2)反应④的化学方程式为
(3)下列有关说法正确的是______。
| A.可以用燃烧的方法区别乙烯和甲烷 |
| B.丙为难溶于水的黄色油状液体 |
| C.丁可以使酸性高锰酸钾溶液褪色 |
| D.医疗上常用体积分数为75%的己溶液做消毒剂 |
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐3】已知有机物A能发生以下转化,并且A可以作为水果的催熟剂,在一定条件下A可以发生加聚反应,形成高分子化合物E。
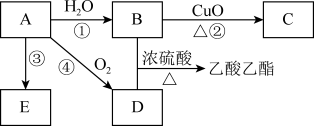
(1)E_______ (填“能”或“不能”)使酸性KMnO4溶液褪色。
(2)D分子中的官能团名称是_______ 。
(3)请写出B和CuO加热生成C的化学方程式:_______ 。
(4)下列说法正确的是_______(填序号)

(1)E
(2)D分子中的官能团名称是
(3)请写出B和CuO加热生成C的化学方程式:
(4)下列说法正确的是_______(填序号)
| A.乙酸乙酯在冷的饱和纯碱溶液中的溶解度较小,但是热的纯碱溶液比较容易除去乙酸乙酯这类酯类油污 |
| B.C常温下是一种无色、无味,水溶性很好的液体 |
| C.分别取相同质量的C和D,完全燃烧,耗氧量相同 |
| D.反应②和④的反应类型相同 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表的一部分, 请参照元素①~@在表中的位置,用化学用语作答:

(1)元素⑤、⑥、⑦、⑨的离子半径由大到小的顺序为_______________ (填离子符号) ;
(2)元素⑧、⑨、⑩的最高价含氧酸的酸性由强到弱的顺序为___________ (用化学式表示);
(3)写出⑥在空气中加热燃烧后产物的电子式:____________________ 。
(4)已知某些不同族元素的性质也有一定的相似性,如元素②与元素⑦的氢氧化物有相似的性质。写出元素②的氢氧化物与NaOH溶液反应的离子方程式:__________________________ 。
(5)已知砷(As)为第VA族元素,位于元素⑧的下一周期,它的化合物可用于杀虫及医疗。
①As的原子结构示意图为________________ 。
②Y是由④⑥⑩三种元素组成的化合物,是生活中常见的消海剂。砷的氢化物可与Y的水溶液反应,生成砷的最高价含氧酸,则该反应的化学方程式为___________________ 。消耗l mol 还原剂时,转移电子的物质的量为_____________ mol。

(1)元素⑤、⑥、⑦、⑨的离子半径由大到小的顺序为
(2)元素⑧、⑨、⑩的最高价含氧酸的酸性由强到弱的顺序为
(3)写出⑥在空气中加热燃烧后产物的电子式:
(4)已知某些不同族元素的性质也有一定的相似性,如元素②与元素⑦的氢氧化物有相似的性质。写出元素②的氢氧化物与NaOH溶液反应的离子方程式:
(5)已知砷(As)为第VA族元素,位于元素⑧的下一周期,它的化合物可用于杀虫及医疗。
①As的原子结构示意图为
②Y是由④⑥⑩三种元素组成的化合物,是生活中常见的消海剂。砷的氢化物可与Y的水溶液反应,生成砷的最高价含氧酸,则该反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知A、B、C、D、E为中学常见的五种物质,均含元素Y,有的还可能含有元素X、Z,元素X、Y、Z的原子序数依次递增。
①元素Y在A、B、C、D、E中所呈化合价依次递增,其中只有B为单质。
②常温下将气体D通入水中发生反应,生成C和E。
③工业上以A、空气和水为原料,通过催化氧化法制成E。
请回答以下问题:
(1)A分子的空间构型是__________ ;从轨道重叠的方式看,B分子中的共价键类型有__________ 。
(2)写出②中反应的化学方程式:___________________________________________ 。
(3)工业上,若输送Cl2的管道漏气,用A进行检验时可观察到大量白烟,同时有B生成,写出有关反应的化学方程式:_________________________________________________ 。
①元素Y在A、B、C、D、E中所呈化合价依次递增,其中只有B为单质。
②常温下将气体D通入水中发生反应,生成C和E。
③工业上以A、空气和水为原料,通过催化氧化法制成E。
请回答以下问题:
(1)A分子的空间构型是
(2)写出②中反应的化学方程式:
(3)工业上,若输送Cl2的管道漏气,用A进行检验时可观察到大量白烟,同时有B生成,写出有关反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)元素周期表可分为不同的区域,在下面元素周期表中全部是金属元素的区域为_______ 。
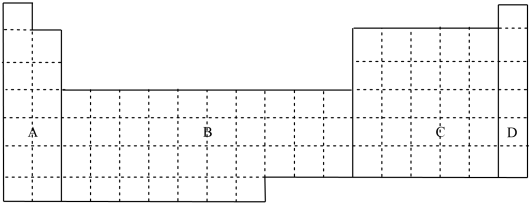
a.A b.B c.C d.D
(2)短周期主族元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子数的2倍;Y元素单质为双原子分子,其氢化物水溶液呈碱性;Z元素原子核外M层电子数目与K层相等;1mol单质W跟盐酸完全反应,能置换出33.6L的H2(标准状况);
①请写出元素X的一种核素的化学符号_______ ;
②写出元素Y在周期表中的位置_______ ;
③Z、W两元素相比较,金属性较强的元素是_______ (填元素符号),可以验证该结论的实验是_______ 。
(a)比较两种元素单质的熔点
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)比较这两种元素的最高价氧化物对应水化物的碱性
(d)比较这两种元素的气态氢化物的稳定性
(1)元素周期表可分为不同的区域,在下面元素周期表中全部是金属元素的区域为

a.A b.B c.C d.D
(2)短周期主族元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子数的2倍;Y元素单质为双原子分子,其氢化物水溶液呈碱性;Z元素原子核外M层电子数目与K层相等;1mol单质W跟盐酸完全反应,能置换出33.6L的H2(标准状况);
①请写出元素X的一种核素的化学符号
②写出元素Y在周期表中的位置
③Z、W两元素相比较,金属性较强的元素是
(a)比较两种元素单质的熔点
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)比较这两种元素的最高价氧化物对应水化物的碱性
(d)比较这两种元素的气态氢化物的稳定性
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、W、M、N为原子序数依次增大的六种短周期元素,常温下,六种元素的常见单质中三种为气体,三种为固体。X与M,W与N分别同主族,在周期表中X是原子半径最小的元素,且X能与Y、Z、W分别形成电子数相等的三种分子,Z、W的最外层电子数之和与M的核外电子总数相等。试回答下列问题:
(1)N元素在周期表中的位置为_____ ;Y的简单氢化物的稳定性_____ (填“>”“<”或“=”)W的简单氢化物的稳定性。
(2)X、Z形成的含18电子的化合物的结构式为_____ 。
(3)由X、Z、W、N四种元素组成的一种离子化合物A,已知A既能与盐酸反应,又能与氯水反应,写出A与足量盐酸反应的离子方程式_____ 。
(4)X和W组成的化合物中,既含有极性共价键又含有非极性共价键的是_____ (填化学式),此化合物可将碱性工业废水中的CN-氧化,生成碳酸盐和氨气,相应的离子方程式为_____ 。
(1)N元素在周期表中的位置为
(2)X、Z形成的含18电子的化合物的结构式为
(3)由X、Z、W、N四种元素组成的一种离子化合物A,已知A既能与盐酸反应,又能与氯水反应,写出A与足量盐酸反应的离子方程式
(4)X和W组成的化合物中,既含有极性共价键又含有非极性共价键的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E五种元素,已知:
①A原子的最外层电子数是次外层电子数的两倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同,E原子的M层上的电子数比K层多5。
②常温下B2是气体,它对氢气的相对密度是16。
③C的单质在B2中燃烧,生成淡黄色固体F。F与AB2反应可生成B2。
④D的单质在B2中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体DB2。D在DB2中的含量为50%。根据以上情况回答:
(1)E位于第__ 周期__ 族;
(2)C的离子结构示意图是____ ,F中的化学键为_____ ;
(3)AB2的电子式为__ ;F和AB2反应的化学方程式为______ ;
(4)C、D、E三种元素的原子半径从小到大的顺序为__ ;(用元素符号回答)
(5)常温下,E的单质与C的最高价氧化物对应水化物的水溶液反应的离子方程式为__________ 。
①A原子的最外层电子数是次外层电子数的两倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同,E原子的M层上的电子数比K层多5。
②常温下B2是气体,它对氢气的相对密度是16。
③C的单质在B2中燃烧,生成淡黄色固体F。F与AB2反应可生成B2。
④D的单质在B2中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体DB2。D在DB2中的含量为50%。根据以上情况回答:
(1)E位于第
(2)C的离子结构示意图是
(3)AB2的电子式为
(4)C、D、E三种元素的原子半径从小到大的顺序为
(5)常温下,E的单质与C的最高价氧化物对应水化物的水溶液反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】已知X、Y、Z、W四种元素分别是元素周期表中连续三个短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y与X形成的分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。试判断:
(1)写出Z离子的结构示意图:_______
(2)由以上元素两两形成的化合物中,溶于水显碱性的气态氢化物的电子式为_______ ,含有非极性共价键的共价化合物的化学式为_______ 。
(3)由X、Y、Z所形成的的常见离子化合物是_______ (填化学式)
(4)用电子式表示W2Z2的形成过程:_______ 。
(1)写出Z离子的结构示意图:
(2)由以上元素两两形成的化合物中,溶于水显碱性的气态氢化物的电子式为
(3)由X、Y、Z所形成的的常见离子化合物是
(4)用电子式表示W2Z2的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】短周期主族元素A、B、C、D、E、F的原子序数依次增大,它们的原子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C、D是空气中含量最多的两种元素,D、E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(1)写出D与E以1∶1的原子个数比形成的化合物的电子式:__ 。F在周期表中的位置__ 。
(2)B、D形成的化合物BD2中存在的化学键为__ 键(填“离子”或“共价”,下同)。A、C、F三种元素形成的化合物CA4F为__ 化合物。
(3)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为__ 。
(4)A、C、D、E的原子半径由大到小的顺序是__ (用元素符号表示)。
(5)元素B和F的非金属性强弱,B的非金属性___ 于F(填“强”或“弱”),并用化学方程式证明上述结论__ 。
(1)写出D与E以1∶1的原子个数比形成的化合物的电子式:
(2)B、D形成的化合物BD2中存在的化学键为
(3)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为
(4)A、C、D、E的原子半径由大到小的顺序是
(5)元素B和F的非金属性强弱,B的非金属性
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E、F是分属三个短周期的主族元素,且原子序数依次增大。A、D同主族,B的氢化物水溶液呈碱性,C、E同主族,形成的化合物EC2是形成酸雨的主要物质之一。请用化学用语回答下列问题:
(1)F在元素周期表中的位置为_______________ 。
(2)常温下,液态的B2A4与气态的BC2两者发生反应生成无毒物质,16g B2A4发生反应放热akJ,该反应的热化学方程式为____________________________________________ 。
(3)D2E溶液在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色,H的电子式为_________________ 。写出在空气中长期放置生成H的化学反应方程式为:___________________________________ 。H的溶液与稀硫酸反应产生的现象为____________________________________ 。
(4)化学家发现一种化学式为A4B4的离子化合物,一定条件下1mol 熔融A4B4电离生成两种离子各1mol,则该物质熔融时的电离方程式为____________________________________ 。
(5)向30mL某浓度由A、B、C、D中三种元素形成的一元强碱溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V[HCl(aq)]的关系有下列图示两种情况(不计CO2的溶解)。则曲线Y表明M中的溶质为_______________ ;原NaOH溶液的物质的量浓度为____________ ;由曲线X、Y可知,两次实验通入的CO2的体积比为_________ 。

(1)F在元素周期表中的位置为
(2)常温下,液态的B2A4与气态的BC2两者发生反应生成无毒物质,16g B2A4发生反应放热akJ,该反应的热化学方程式为
(3)D2E溶液在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色,H的电子式为
(4)化学家发现一种化学式为A4B4的离子化合物,一定条件下1mol 熔融A4B4电离生成两种离子各1mol,则该物质熔融时的电离方程式为
(5)向30mL某浓度由A、B、C、D中三种元素形成的一元强碱溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V[HCl(aq)]的关系有下列图示两种情况(不计CO2的溶解)。则曲线Y表明M中的溶质为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】Ⅰ.A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上的电子数之和。
(1)B为_______ ,D的最高价氧化物对应的水化物是______ ,简单离子半径大小B_______ (填“>”“<”或“=”)C。
(2)写出A、B的化合物与E反应的化学方程式:_______ 。
(3)A、B两元素形成的化合物属于______ (填“离子”或“共价”)化合物。
Ⅱ.随原子序数的递增,八种短周期元素原子半径的相对大小、最高正价或最低负价的变化如图所示。

回答下列问题:
(1)A、B均为以上某两种元素组成的分子,A中有四个原子核和10个电子,B中有6个原子核和18个电子,则A的分子式为________ ,B的分子式为_________ 。
(2)比较e、f两种元素对应离子的半径大小______ (用元素离子符号表示);非金属性g_____ (填“强于”或“弱于”)h,用一个化学方程式证明你的判断________ 。
(1)B为
(2)写出A、B的化合物与E反应的化学方程式:
(3)A、B两元素形成的化合物属于
Ⅱ.随原子序数的递增,八种短周期元素原子半径的相对大小、最高正价或最低负价的变化如图所示。

回答下列问题:
(1)A、B均为以上某两种元素组成的分子,A中有四个原子核和10个电子,B中有6个原子核和18个电子,则A的分子式为
(2)比较e、f两种元素对应离子的半径大小
您最近一年使用:0次



