A、B、C、D、E、F是分属三个短周期的主族元素,且原子序数依次增大。A、D同主族,B的氢化物水溶液呈碱性,C、E同主族,形成的化合物EC2是形成酸雨的主要物质之一。请用化学用语回答下列问题:
(1)F在元素周期表中的位置为_______________ 。
(2)常温下,液态的B2A4与气态的BC2两者发生反应生成无毒物质,16g B2A4发生反应放热akJ,该反应的热化学方程式为____________________________________________ 。
(3)D2E溶液在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色,H的电子式为_________________ 。写出在空气中长期放置生成H的化学反应方程式为:___________________________________ 。H的溶液与稀硫酸反应产生的现象为____________________________________ 。
(4)化学家发现一种化学式为A4B4的离子化合物,一定条件下1mol 熔融A4B4电离生成两种离子各1mol,则该物质熔融时的电离方程式为____________________________________ 。
(5)向30mL某浓度由A、B、C、D中三种元素形成的一元强碱溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V[HCl(aq)]的关系有下列图示两种情况(不计CO2的溶解)。则曲线Y表明M中的溶质为_______________ ;原NaOH溶液的物质的量浓度为____________ ;由曲线X、Y可知,两次实验通入的CO2的体积比为_________ 。

(1)F在元素周期表中的位置为
(2)常温下,液态的B2A4与气态的BC2两者发生反应生成无毒物质,16g B2A4发生反应放热akJ,该反应的热化学方程式为
(3)D2E溶液在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色,H的电子式为
(4)化学家发现一种化学式为A4B4的离子化合物,一定条件下1mol 熔融A4B4电离生成两种离子各1mol,则该物质熔融时的电离方程式为
(5)向30mL某浓度由A、B、C、D中三种元素形成的一元强碱溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V[HCl(aq)]的关系有下列图示两种情况(不计CO2的溶解)。则曲线Y表明M中的溶质为

更新时间:2017-05-21 19:44:08
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】如图所示:下图为A → E五种含同种元素的物质相互转化的关系图,其中A、B、C、D常温下都是气体,D呈红棕色。按要求回答下列问题:
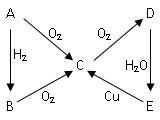
(1) A物质的电子式_______ ;B物质是含______ 键
的______ 分子(填“极性”或者“非极性”)
(2)下列反应的化学方程式为:
①B→C:_____________________________________________
②D→E:_____________________________________________
(3)实验室制取B的化学方程式为:__________________________________________ ,通常用___________ 来干燥B气体;
已知B可以与灼热的氧化铜反应得到A气体和金属铜,则该反应的化学方程式为:________________________________________________ 。

(1) A物质的电子式
的
(2)下列反应的化学方程式为:
①B→C:
②D→E:
(3)实验室制取B的化学方程式为:
已知B可以与灼热的氧化铜反应得到A气体和金属铜,则该反应的化学方程式为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
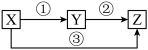
【推荐2】有X、Y、Z三种物质,它们之间存在如下转化关系:
(1)若X、Y、Z三种物质的焰色反应均为黄色,三个反应均为化合反应,则Y的化学式为_________ ,Z的电子式为_________ ;Y、Z两种物质相比,相同的化学键类型为__________ ,当由X制取Z的上述两种途径生成Z的量相等时,转移电子数目比为________ 。
(2)若X、Y、Z三种均为常见化合物且三种物质中均含有相同的两种短周期元素,0.1 mol/L的三种物质的溶液pH:Y>X>Z>7,则①的化学方程式为___________________ ,③的离子方程式为__________________ 。
(3)若X、Y、Z三种物质均含有同一种金属元素,X是单质,Y是日常生活中最重要的盐,②的反应条件为电解,则②的化学方程式为_________________ ,③的离子方程式为________ 。
(1)若X、Y、Z三种物质的焰色反应均为黄色,三个反应均为化合反应,则Y的化学式为
(2)若X、Y、Z三种均为常见化合物且三种物质中均含有相同的两种短周期元素,0.1 mol/L的三种物质的溶液pH:Y>X>Z>7,则①的化学方程式为
(3)若X、Y、Z三种物质均含有同一种金属元素,X是单质,Y是日常生活中最重要的盐,②的反应条件为电解,则②的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、D、F均是由短周期元素组成的单质,常温下C是液体, D、F为气体,A、B、E为固体,其中B为淡黄色固体。
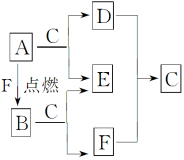
请回答下列问题:
(1)B和E的化学式:B________ ,E________ 。
(2)A与C反应的离子方程式为____________________________________________________________ 。
(3)下列关于A的叙述正确的是________ (填序号)。
①A有很强的还原性 ②A的焰色反应呈紫色
③少量A可以保存在冷水里 ④A着火时应选用泡沫灭火器
(4)将A、镁、铝各0.3 mol分别放入100 mL 1 mol·L-1的盐酸中,同温同压下产生的气体体积之比是________ (填序号)。
①1∶2∶3 ②6∶3∶2 ③3∶1∶1 ④1∶1∶1

请回答下列问题:
(1)B和E的化学式:B
(2)A与C反应的离子方程式为
(3)下列关于A的叙述正确的是
①A有很强的还原性 ②A的焰色反应呈紫色
③少量A可以保存在冷水里 ④A着火时应选用泡沫灭火器
(4)将A、镁、铝各0.3 mol分别放入100 mL 1 mol·L-1的盐酸中,同温同压下产生的气体体积之比是
①1∶2∶3 ②6∶3∶2 ③3∶1∶1 ④1∶1∶1
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C是由周期表中短周期元素组成的三种常见化合物,甲、乙、丙是三种单质,这些单质和化合物之间存在如图所示的关系,完成下列空白:
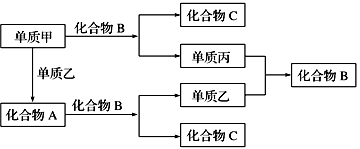
(1)向酚酞试液中加入化合物A的粉末,现象为________ 。
(2)单质甲与化合物B反应的离子方程式为__________ 。5.05g单质甲—钾合金溶于200mL水生成0.075mol氢气,确定该合金的化学式为______ 。
(3)向一定体积某浓度的化合物C的溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示两种情况。
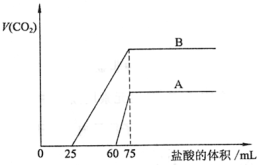
①由A确定滴加前60mL的盐酸时,发生反应的离子方程式为_____________________
②B对应的溶液M低温蒸干后得到固体a克,将a克固体充分加热至恒重后,固体质量减少_____ 克。
③由A、B可知,两次实验通入的CO2的体积比为___________

(1)向酚酞试液中加入化合物A的粉末,现象为
(2)单质甲与化合物B反应的离子方程式为
(3)向一定体积某浓度的化合物C的溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示两种情况。

①由A确定滴加前60mL的盐酸时,发生反应的离子方程式为
②B对应的溶液M低温蒸干后得到固体a克,将a克固体充分加热至恒重后,固体质量减少
③由A、B可知,两次实验通入的CO2的体积比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】 已知:A为含金属离子的淡黄色固体化合物,E、X为空气中常见气体,A、B、C、D含有相同的金属离子,其转化关系如下图(部分产物已略去)。
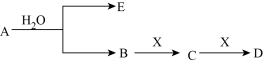
请回答下列问题:
(1)这种金属离子的离子结构示意图为____________ 。
(2) 请写出A的电子式______________________________________ 。常温常压下,15.6 g A与足量的水充分反应放出热量a kJ,写出该反应的热化学方程式为_________________________________________________________ 。
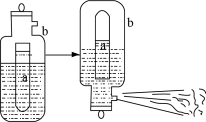
(3)D常用于一种泡沫灭火器,构造如图。内筒a是玻璃瓶,外筒b是钢瓶,平时泡沫灭火器内筒外筒盛有液态试剂,当遇火警时,将灭火器取下倒置,内外筒液体试剂立即混合产生大量CO2泡沫灭火。从液态试剂在灭火器中长久放置和快速灭火两个角度分析,则a中盛________ ,b中盛________ ,反应的化学方程式为_______________________
(4)将一定量的气体X通入2 L B的溶液中,向所得溶液中边逐滴加入稀盐酸边振荡至过量,产生的气体与盐酸物质的量的关系如图(忽略气体的溶解和HCl的挥发)。

请回答:b点溶液中所含溶质的化学式为___________ ,物质的量之比为____________ ,

请回答下列问题:
(1)这种金属离子的离子结构示意图为
(2) 请写出A的电子式

(3)D常用于一种泡沫灭火器,构造如图。内筒a是玻璃瓶,外筒b是钢瓶,平时泡沫灭火器内筒外筒盛有液态试剂,当遇火警时,将灭火器取下倒置,内外筒液体试剂立即混合产生大量CO2泡沫灭火。从液态试剂在灭火器中长久放置和快速灭火两个角度分析,则a中盛
(4)将一定量的气体X通入2 L B的溶液中,向所得溶液中边逐滴加入稀盐酸边振荡至过量,产生的气体与盐酸物质的量的关系如图(忽略气体的溶解和HCl的挥发)。

请回答:b点溶液中所含溶质的化学式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某小组为测定某碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,甲、乙两组同学分别进行了下列相关实验。
方案Ⅰ.甲组同学用沉淀分析法,按如下图所示的实验流程进行实验:
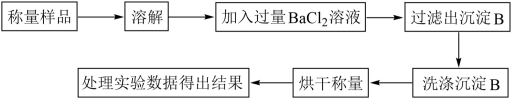
(1)洗涤沉淀B的操作是___________
(2)若实验中测得样品质量为m g,沉淀质量为n g,则碳酸钠的质量分数为___________
方案Ⅱ.乙组同学的主要实验流程图如下:

按如下图所示装置进行实验:
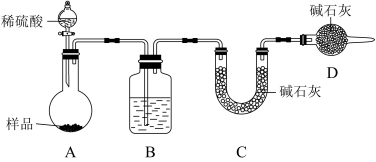
(3)该实验中装置B盛放的物质是___________ ,分液漏斗中___________ (填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(4)在C中装碱石灰来吸收净化后的气体。
①样品中碳酸钠的质量分数越大,则实验中干燥管C在充分吸收气体前后的质量差___________ (填“越大”、“越小”或“不变化”)
②D装置的作用是___________
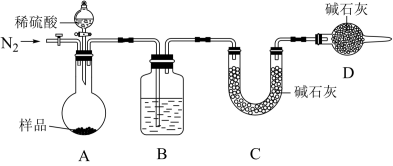
(5)有同学认为为了减少实验误差,在反应前后都要通入N2(如下图),反应后通入N2的目的是___________ 。
方案Ⅰ.甲组同学用沉淀分析法,按如下图所示的实验流程进行实验:

(1)洗涤沉淀B的操作是
(2)若实验中测得样品质量为m g,沉淀质量为n g,则碳酸钠的质量分数为
方案Ⅱ.乙组同学的主要实验流程图如下:

按如下图所示装置进行实验:

(3)该实验中装置B盛放的物质是
(4)在C中装碱石灰来吸收净化后的气体。
①样品中碳酸钠的质量分数越大,则实验中干燥管C在充分吸收气体前后的质量差
②D装置的作用是
(5)有同学认为为了减少实验误差,在反应前后都要通入N2(如下图),反应后通入N2的目的是

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E均为短周期元素,且原子序数依次增大,请根据表中信息回答下列问题:
(1)E在元素周期表中的位置_________________ ;
(2)B的最简单气态氢化物分子空间构型_____________ ;其沸点高于同主族的其它气态氢化物原因_______ ;
(3)D的最高价氧化物对应水化物的化学键类型______________ ;
(4)B、C、D、E简单离子半径大小________________ (用元素符号表示);
(5)由A、B、C与H元素组成的一种常见的酸式盐与过量的D的最高价氧化物对应的水化物反应的离子方程式_______________________ ,在25℃,101kPa下,2gE单质在C2气体中完全燃烧后恢复到原状态,放热18.72kJ,该反应的热化学方程式_____________________ 。
| 元素符号 | 元素性质或原子结构 |
| A | A是形成化合物最多的元素 |
| B | B元素的单质在空气中含量最多 |
| C | C元素在地壳中含量最多 |
| D | D元素在同周期中金属性最强 |
| E | 常温常压下,E元素形成的单质是淡黄色固体,常在火山口附近沉积 |
(2)B的最简单气态氢化物分子空间构型
(3)D的最高价氧化物对应水化物的化学键类型
(4)B、C、D、E简单离子半径大小
(5)由A、B、C与H元素组成的一种常见的酸式盐与过量的D的最高价氧化物对应的水化物反应的离子方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】I.在恒温、体积为1.0L的密闭容器中通入1.0 mol N2和x mol H2发生如下反应N2(g)+3H2(g) 2NH3(g) ,20 min后达到平衡,测得反应放出的热量为18.4 kJ,混合气体的物质的量为1.6 mol,容器内的压强变为原来的80%。请回答下列问题:
2NH3(g) ,20 min后达到平衡,测得反应放出的热量为18.4 kJ,混合气体的物质的量为1.6 mol,容器内的压强变为原来的80%。请回答下列问题:
(1)20 min内,V(N2)=______ 。
(2)该反应的热化学方程式为____________ 。
(3)下列叙述中能表示该反应达到平衡状态的是_______ (填序号)。
①N2体积分数保持不变②单位时间断裂03tmol H- H键,同时生成0.6 molN-H键
③混合气体的密度不再改变④2v正(H2)=3v逆(NH3)⑤混合气体的平均摩尔质量不再改变
II.1883年,瑞典化学家阿伦尼乌斯创立了电离学说,在水溶液范围内对酸、碱作出了严密的概括。请回答下列有关水溶液的问题:
(4) ①用电离方程式表示氨水溶液是碱性的原因________ ;
②用离子方程式表示碳酸钠溶液显碱性的原因__________ 。
 2NH3(g) ,20 min后达到平衡,测得反应放出的热量为18.4 kJ,混合气体的物质的量为1.6 mol,容器内的压强变为原来的80%。请回答下列问题:
2NH3(g) ,20 min后达到平衡,测得反应放出的热量为18.4 kJ,混合气体的物质的量为1.6 mol,容器内的压强变为原来的80%。请回答下列问题:(1)20 min内,V(N2)=
(2)该反应的热化学方程式为
(3)下列叙述中能表示该反应达到平衡状态的是
①N2体积分数保持不变②单位时间断裂03tmol H- H键,同时生成0.6 molN-H键
③混合气体的密度不再改变④2v正(H2)=3v逆(NH3)⑤混合气体的平均摩尔质量不再改变
II.1883年,瑞典化学家阿伦尼乌斯创立了电离学说,在水溶液范围内对酸、碱作出了严密的概括。请回答下列有关水溶液的问题:
(4) ①用电离方程式表示氨水溶液是碱性的原因
②用离子方程式表示碳酸钠溶液显碱性的原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】50mL 0.50 盐酸与50mL 0.55
盐酸与50mL 0.55 NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应的反应热。回答下列问题:
NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应的反应热。回答下列问题:

(1)写出该反应的热化学方程式_______ 。(中和反应的反应热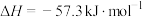 )
)
(2)若将装置中的玻璃搅拌器换成环形铜丝搅拌棒,实验数值结果与57.3 相比
相比_______ (填“偏大”或“偏小”),产生偏差的原因可能是_______ 。
(3)实验操作过程中,实验数据如下表:
上述实验中温度变化的平均值为_______ ℃,若近似认为0.50 稀盐酸与0.55
稀盐酸与0.55 NaOH溶液的密度均为1
NaOH溶液的密度均为1 ,反应所得溶液的比热容
,反应所得溶液的比热容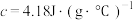 ,则中和热△H的数值为
,则中和热△H的数值为_______  (保留1位小数)。
(保留1位小数)。
(4)如果用0.50 的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”的数值将
的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”的数值将_______ (填“偏大”、“偏小”、“不变”),原因是_______ 。
(5)实验中改用60mL 0.5 盐酸跟50mL 0.55
盐酸跟50mL 0.55 NaOH溶液进行反应,调整反应物用量后所放出的热量与原实验
NaOH溶液进行反应,调整反应物用量后所放出的热量与原实验_______ (填“相等”或“不相等”,下同),所求中和反应反应热与原实验_______ ,简述理由:_______ 。
 盐酸与50mL 0.55
盐酸与50mL 0.55 NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应的反应热。回答下列问题:
NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应的反应热。回答下列问题:
(1)写出该反应的热化学方程式
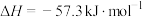 )
)(2)若将装置中的玻璃搅拌器换成环形铜丝搅拌棒,实验数值结果与57.3
 相比
相比(3)实验操作过程中,实验数据如下表:
| 温度 实验次数 | 起始温度 /℃ /℃ | 终止温度 /℃ /℃ | ||
| HCl | NaOH | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 29.4 |
| 2 | 27.0 | 27.4 | 27.2 | 31.2 |
| 3 | 25.9 | 25.9 | 25.9 | 29.4 |
| 4 | 26.4 | 26.2 | 26.3 | 29.7 |
 稀盐酸与0.55
稀盐酸与0.55 NaOH溶液的密度均为1
NaOH溶液的密度均为1 ,反应所得溶液的比热容
,反应所得溶液的比热容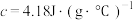 ,则中和热△H的数值为
,则中和热△H的数值为 (保留1位小数)。
(保留1位小数)。(4)如果用0.50
 的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”的数值将
的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”的数值将(5)实验中改用60mL 0.5
 盐酸跟50mL 0.55
盐酸跟50mL 0.55 NaOH溶液进行反应,调整反应物用量后所放出的热量与原实验
NaOH溶液进行反应,调整反应物用量后所放出的热量与原实验
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】现有A、B、C、D四种短周期主族元素,其中原子序数依次增大。已知B和D同主族。A元素的最高正价和最低负价的绝对值之差为2;1molC单质能与冷水反应,在标准状况下生成11.2LH2;D-的电子层结构与Ar原子相同。请回答下列问题:
⑴在下图塔式周期表相应位置标出A、B、C、D四种元素的元素符号。同时在图中将过渡元素涂黑。
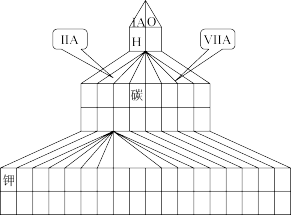
_____________
⑵用电子式表示B与C形成化合物的过程___________ 。
⑶图中“钾”和D形成的简单离子的半径大小为________________ (用离子符号和“>”、“=”或“<”表示)。
⑷元素非金属性强弱比较有很多方法,其中A和D的非金属性强弱的研究方案中比较可行的是_______ (填序号)。
①比较两种单质的颜色②比较氢化物的稳定性
③比较原子半径大小④比较最高价氧化物对应水化物的酸性
⑸A元素能与另外三种元素中的一种元素形成共价化合物,分子中的原子个数比为1:3,相对分子质量为120.5。则该物质的结构式为____________ 。
⑴在下图塔式周期表相应位置标出A、B、C、D四种元素的元素符号。同时在图中将过渡元素涂黑。

⑵用电子式表示B与C形成化合物的过程
⑶图中“钾”和D形成的简单离子的半径大小为
⑷元素非金属性强弱比较有很多方法,其中A和D的非金属性强弱的研究方案中比较可行的是
①比较两种单质的颜色②比较氢化物的稳定性
③比较原子半径大小④比较最高价氧化物对应水化物的酸性
⑸A元素能与另外三种元素中的一种元素形成共价化合物,分子中的原子个数比为1:3,相对分子质量为120.5。则该物质的结构式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、D、E、F、G为短周期元素,且原子序数依次递增。A、F同主族,E、G同主族。A与其他非金属元素化合时易形成共价键,F与其他非金属元素化合时易形成离子键,且F+与E2-核外电子排布相同。由以上元素组成的物质BE和D2具有相同的电子数。
请回答下列问题:
(1)F位于第________ 周期第________ 族。
(2)G的离子结构示意图为_______________________________________________ 。
(3)用电子式表示D2的形成过程:________________________________________ 。
(4)由A、E、F三种元素形成的化合物的化学式为________ ,属于________ 化合物。
(5)B的最高价是________ ,由A、B组成的化合物中,含A的质量分数最高的物质的化学式是________ ;A、B组成的化合物中与D2相对分子质量相等的物质的化学式是________ ,有________ 对共用电子对。
请回答下列问题:
(1)F位于第
(2)G的离子结构示意图为
(3)用电子式表示D2的形成过程:
(4)由A、E、F三种元素形成的化合物的化学式为
(5)B的最高价是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】联合国大会将2019年定为“化学元素周期表国际年”,表明了元素周期律的重要性。如表列出了元素周期表中短周期的一部分,a~i代表9种短周期元素。
请用化学用语回答下列问题:
(1)a和b形成的化合物可用作催化剂,其化学式为___________ 。
(2)元素c、d形成的简单离子半径大小关系为___________ >___________ (填离子符号)。
(3)9种元素中非金属性最强的是___________ (填元素符号)。
(4)若单质c与水反应得到3.36L的气体(标准状况),则消耗单质c的质量为___________ g。
(5)写出实验室制备g的最高价氧化物对应的水化物的离子方程式___________ 。
(6)预测将i的单质通入h的氢化物的水溶液中___________ (填“能”或“不能”)发生反应,请简述预测的依据:___________ 。
| 周期 | ⅠA | 0 | |||||||
| 1 | ⅡA |  | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | a | b | c | d | |||||
| 3 | c | f | g | h | i | ||||
(1)a和b形成的化合物可用作催化剂,其化学式为
(2)元素c、d形成的简单离子半径大小关系为
(3)9种元素中非金属性最强的是
(4)若单质c与水反应得到3.36L的气体(标准状况),则消耗单质c的质量为
(5)写出实验室制备g的最高价氧化物对应的水化物的离子方程式
(6)预测将i的单质通入h的氢化物的水溶液中
您最近一年使用:0次



