已知:A为含金属离子的淡黄色固体化合物,E、X为空气中常见气体,A、B、C、D含有相同的金属离子,其转化关系如下图(部分产物已略去)。
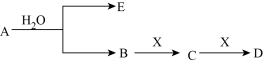
请回答下列问题:
(1)这种金属离子的离子结构示意图为____________ 。
(2) 请写出A的电子式______________________________________ 。常温常压下,15.6 g A与足量的水充分反应放出热量a kJ,写出该反应的热化学方程式为_________________________________________________________ 。
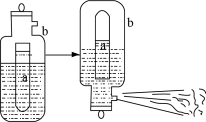
(3)D常用于一种泡沫灭火器,构造如图。内筒a是玻璃瓶,外筒b是钢瓶,平时泡沫灭火器内筒外筒盛有液态试剂,当遇火警时,将灭火器取下倒置,内外筒液体试剂立即混合产生大量CO2泡沫灭火。从液态试剂在灭火器中长久放置和快速灭火两个角度分析,则a中盛________ ,b中盛________ ,反应的化学方程式为_______________________
(4)将一定量的气体X通入2 L B的溶液中,向所得溶液中边逐滴加入稀盐酸边振荡至过量,产生的气体与盐酸物质的量的关系如图(忽略气体的溶解和HCl的挥发)。

请回答:b点溶液中所含溶质的化学式为___________ ,物质的量之比为____________ ,

请回答下列问题:
(1)这种金属离子的离子结构示意图为
(2) 请写出A的电子式

(3)D常用于一种泡沫灭火器,构造如图。内筒a是玻璃瓶,外筒b是钢瓶,平时泡沫灭火器内筒外筒盛有液态试剂,当遇火警时,将灭火器取下倒置,内外筒液体试剂立即混合产生大量CO2泡沫灭火。从液态试剂在灭火器中长久放置和快速灭火两个角度分析,则a中盛
(4)将一定量的气体X通入2 L B的溶液中,向所得溶液中边逐滴加入稀盐酸边振荡至过量,产生的气体与盐酸物质的量的关系如图(忽略气体的溶解和HCl的挥发)。

请回答:b点溶液中所含溶质的化学式为
更新时间:2020-10-25 10:40:23
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是由质子数小于18的元素组成的一些单质及其化合物之间的转化关系图。常温常压下,D、F、K均为无色无刺激性气味的气体,B是最常见的无色液体,A是由单质C在D中燃烧生成的淡黄色固体。(反应中生成的部分物质已略去)
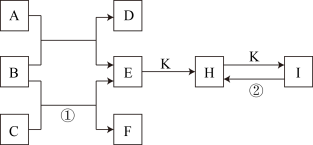
请回答下列问题:
(1)物质A的化学式为________ ;
(2)化合物I的化学式为________ ;
(3)反应①的离子方程式为_____________ ;
(4)反应②的化学方程式为______________ 。

请回答下列问题:
(1)物质A的化学式为
(2)化合物I的化学式为
(3)反应①的离子方程式为
(4)反应②的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他物质已经略去):
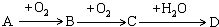
(1)若A是一种金属,C是淡黄色固体,写出C的一种用途_______ ;
(2)若A为淡黄色固体单质,写出D的浓溶液与铜反应的化学方程式______ ;
(3)若A是化合物,C是红棕色气体,则A的化学式为_____________ ;C转化为D的过程中,氧化剂与还原剂的质量比为__________________ 。
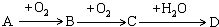
(1)若A是一种金属,C是淡黄色固体,写出C的一种用途
(2)若A为淡黄色固体单质,写出D的浓溶液与铜反应的化学方程式
(3)若A是化合物,C是红棕色气体,则A的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D是四种常见气体单质。E的相对分子质量比F小16,且F为红棕色。有关的转化关系如图所示(反应条件与部分反应的生成物略去)。
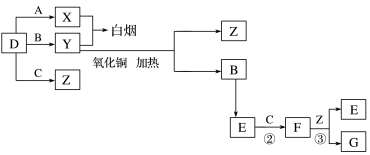
请回答下列问题:
(1)B的电子式为___________ 。
(2)Y与氧化铜反应,每生成1 mol B消耗3 mol氧化铜,该反应的化学方程式为___________ 。
(3)Y与E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为___________ 。
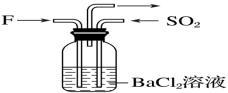
(4)气体F和气体SO2在通常条件下同时通入盛有BaCl2溶液的洗气瓶中(如图所示),洗气瓶中是否有沉淀生成?___________ ,理由是___________ 。

请回答下列问题:
(1)B的电子式为
(2)Y与氧化铜反应,每生成1 mol B消耗3 mol氧化铜,该反应的化学方程式为
(3)Y与E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为
(4)气体F和气体SO2在通常条件下同时通入盛有BaCl2溶液的洗气瓶中(如图所示),洗气瓶中是否有沉淀生成?

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】已知:A为含金属离子的淡黄色固体化合物,E、X为空气中常见气体,A、B、C、D含有相同的金属离子,其转化关系如下图(部分产物已略去)。
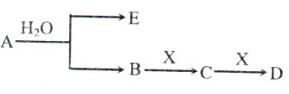
请回答下列问题:
(l)这种金属离子的离子结构示意图为______ ;
(2)X的电子式______ ;
(3)B中所含化学键的类型是______ ;常温常压下,7.8g A与足量的水充分反应放出热量a kJ,写出该反应的热化学方程式______ 。
(4)①C也可转化为B,写出该转化的化学方程式______ ;
②B与D反应的离子方程式为______ 。
(5)将一定量的气体X通入2L B的溶液中,向所得溶液中边逐滴加入稀盐酸边振荡至过量,产生的气体与盐酸物质的量的关系如下图(忽略气体的溶解和HCl的挥发)。
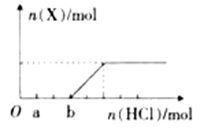
请回答:a点溶液中所含溶质的化学式为________ ,a-b之间的反应的离子方程式_____ 。

请回答下列问题:
(l)这种金属离子的离子结构示意图为
(2)X的电子式
(3)B中所含化学键的类型是
(4)①C也可转化为B,写出该转化的化学方程式
②B与D反应的离子方程式为
(5)将一定量的气体X通入2L B的溶液中,向所得溶液中边逐滴加入稀盐酸边振荡至过量,产生的气体与盐酸物质的量的关系如下图(忽略气体的溶解和HCl的挥发)。

请回答:a点溶液中所含溶质的化学式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学兴趣小组用100mL1mol/LNaOH溶液完全吸收了amolCO2后得到溶液A(液体体积无变化)。为了确定溶液A的溶质成分及a值,该兴趣小组的同学进行了如下实验。请帮助他们完成下列相应实验内容。
[提出假设]
(1)假设I:溶液A的溶质为_____ ;
假设II:溶液A的溶质为Na2CO3;
假设III:溶液A的溶质为Na2CO3、NaHCO3;
假设IV:溶液A的溶质为_____ 。
[实验过程]
(1)甲同学取少量溶液A于试管,再向试管中滴加几滴酚酞溶液,溶液A变红,由此得出假设I成立。
(2)乙同学分析后认为甲同学的实验结论有误。请说明乙同学的判断依据_____ ;他进一步提出,应先取少量溶液,向其中加入足量的_____ 溶液,来检验溶液A是否含_____ ,结果加入检验溶液后观察到溶液A变浑浊。
(3)丙同学为了检验溶液A是否还含其它溶质,他将乙同学所得浑浊溶液进行过滤,并把滤液分为两份,向其中的一份加入稀硫酸,有无色气体生成,则假设_____ 正确。
(4)为准确测定a值,丁同学取了10mL溶液A在锥形瓶中,用滴定管向其中加入某浓度的稀硫酸,记录加入硫酸的体积与生成气体的情况,并绘制成如图:

则a=_____ ,所加硫酸的物质的量浓度为_____ 。
[提出假设]
(1)假设I:溶液A的溶质为
假设II:溶液A的溶质为Na2CO3;
假设III:溶液A的溶质为Na2CO3、NaHCO3;
假设IV:溶液A的溶质为
[实验过程]
(1)甲同学取少量溶液A于试管,再向试管中滴加几滴酚酞溶液,溶液A变红,由此得出假设I成立。
(2)乙同学分析后认为甲同学的实验结论有误。请说明乙同学的判断依据
(3)丙同学为了检验溶液A是否还含其它溶质,他将乙同学所得浑浊溶液进行过滤,并把滤液分为两份,向其中的一份加入稀硫酸,有无色气体生成,则假设
(4)为准确测定a值,丁同学取了10mL溶液A在锥形瓶中,用滴定管向其中加入某浓度的稀硫酸,记录加入硫酸的体积与生成气体的情况,并绘制成如图:

则a=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制备金属钠的工业方法,其反应原理:2NaCl(熔融) 2Na+Cl2↑。根据所学知识回答下列有关问题:
2Na+Cl2↑。根据所学知识回答下列有关问题:
(1)实验室保存金属钠的正确方法是___________(填序号)。
(2)将一小块金属钠放在干燥的坩埚中,用酒精灯加热充分反应,发生反应的化学方程式为___________ ,生成物的颜色为___________ 。
(3)将Na、Na2O、Na2O2、NaOH久置于空气中,最终都是变为___________ (填化学式)。
(4)过氧化钠常用作漂白剂、杀菌消毒剂。某兴趣小组以过氧化钠为对象进行如下探究:“干燥的CO2不能与Na2O2反应”和“CO2在有水存在时才能与Na2O2反应”,设计如下实验装置:
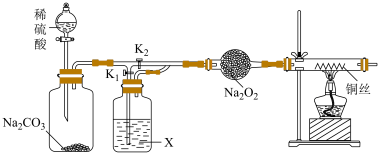
连接装置,检查气密性。在干燥管中装入Na2O2后,打开活塞加入稀硫酸,生成CO2.打开K1,关闭K2,一段时间后再加热铜丝。其中,X中应加入试剂___________ (填名称)。先通一段时间CO2的目的是___________ ,实验观察到铜丝未变化,则得出结论“干燥的CO2不能与Na2O2反应”。若打开K2,关闭K1,出现___________ 现象,可证明“有水时CO2与Na2O2反应”产生了O2。
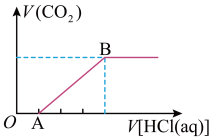
(5)将一定量的CO2通入NaOH溶液中,再向所得溶液中逐滴滴加盐酸,所得气体的体积与加入盐酸的体积关系如图所示,其中OA段发生的离子反应方程式为___________ 。
 2Na+Cl2↑。根据所学知识回答下列有关问题:
2Na+Cl2↑。根据所学知识回答下列有关问题:(1)实验室保存金属钠的正确方法是___________(填序号)。
| A.放在棕色瓶中 | B.放在细沙中 | C.放在水中 | D.放在煤油中 |
(2)将一小块金属钠放在干燥的坩埚中,用酒精灯加热充分反应,发生反应的化学方程式为
(3)将Na、Na2O、Na2O2、NaOH久置于空气中,最终都是变为
(4)过氧化钠常用作漂白剂、杀菌消毒剂。某兴趣小组以过氧化钠为对象进行如下探究:“干燥的CO2不能与Na2O2反应”和“CO2在有水存在时才能与Na2O2反应”,设计如下实验装置:

连接装置,检查气密性。在干燥管中装入Na2O2后,打开活塞加入稀硫酸,生成CO2.打开K1,关闭K2,一段时间后再加热铜丝。其中,X中应加入试剂
(5)将一定量的CO2通入NaOH溶液中,再向所得溶液中逐滴滴加盐酸,所得气体的体积与加入盐酸的体积关系如图所示,其中OA段发生的离子反应方程式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题
(1)已知充分燃烧ag乙炔(C2H2)气体时生成1mol二氧化碳气体和液态水,并放出热量bkJ,则乙炔燃烧的热化学方程式_____
(2)若已知:2H2(g)十O2(g)=2H2O(g)△H1=-Q1kJ·mol-1
2H2(g)十O2(g)=2H2O(l)△H2=-Q2kJ·mol-1
则H2O(g)=H2O(l)的△H=_____ kJ·mol-1(用Q1、Q2表示)
(3)蓄电池是一种反复充电、放电的装置。有一种蓄电池在充电和放电时发生的反应如下:
NiO2+Fe+2H2O Fe(OH)2+Ni(OH)2。
Fe(OH)2+Ni(OH)2。
此蓄电池在充电时,电池负极应与外加电源的_____ 极连接,电极反应式为: _____
(4)已知肼(N2H4)在氧气中完全燃烧生成氮气和水。肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时,负极的电极反应式_____
(5)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。放电时, 移向电池的
移向电池的_____ (填“正”或“负”)极;负极反应为_____ 。
(1)已知充分燃烧ag乙炔(C2H2)气体时生成1mol二氧化碳气体和液态水,并放出热量bkJ,则乙炔燃烧的热化学方程式
(2)若已知:2H2(g)十O2(g)=2H2O(g)△H1=-Q1kJ·mol-1
2H2(g)十O2(g)=2H2O(l)△H2=-Q2kJ·mol-1
则H2O(g)=H2O(l)的△H=
(3)蓄电池是一种反复充电、放电的装置。有一种蓄电池在充电和放电时发生的反应如下:
NiO2+Fe+2H2O
 Fe(OH)2+Ni(OH)2。
Fe(OH)2+Ni(OH)2。此蓄电池在充电时,电池负极应与外加电源的
(4)已知肼(N2H4)在氧气中完全燃烧生成氮气和水。肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时,负极的电极反应式
(5)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。放电时,
 移向电池的
移向电池的
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐2】短周期元素A、B、C、D在周期表中位置如图所示,其中元素D原子最外层有3个电子。请用相应 的化学用语回答:
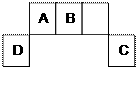
(1)A与氢元素可以形成很多化合物,在这些化合物中都含有_________ (选填“共价”或“离子”)键;与C相邻且最外层电子比C少1个的离子结构示意图为 _________________ 。B在元素周期表中位于____________________ 。B、C、D形成的离子的半径由大到小 依次为 _________________ 。(填相应的离子符号)
(2)元素A形成的最简单氢化物和氧气在KOH溶液中可构成燃料电池,该电池工作时正极 的电极反应式为 ___________________________________ 。
(3)D的最高价氧化物的水化物与NaOH反应的化学 方程式是:
________________________________________ 。
(4)由A与S形成的液态 化合物AS2 0.2mol在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215 kJ。 该反应的热化学方程式为_________________________________ 。
(5)已知298K时,Fe(s) + O2(g) == FeO(s) ; ΔH= -272.0 kJ · mol-1
O2(g) == FeO(s) ; ΔH= -272.0 kJ · mol-1
2D(s) + O2(g) == D2O3(s) ; ΔH= -1675.7 kJ · mol-1
O2(g) == D2O3(s) ; ΔH= -1675.7 kJ · mol-1
写出D单质和FeO反应的热化学方程式是_____________________________________ 。

(1)A与氢元素可以形成很多化合物,在这些化合物中都含有
(2)元素A形成的最简单氢化物和氧气在KOH溶液中可构成燃料电池,该电池工作时
(3)D的最高价氧化物的水化物与NaOH反应的
(4)由A与S形成的
(5)已知298K时,Fe(s) +
 O2(g) == FeO(s) ; ΔH= -272.0 kJ · mol-1
O2(g) == FeO(s) ; ΔH= -272.0 kJ · mol-12D(s) +
 O2(g) == D2O3(s) ; ΔH= -1675.7 kJ · mol-1
O2(g) == D2O3(s) ; ΔH= -1675.7 kJ · mol-1写出D单质和FeO反应的热化学方程式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】Ⅰ、2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。
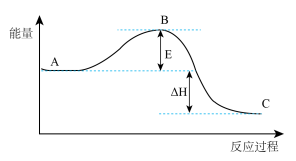
已知1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ·mol-1。请回答下列问题:
(1)E的大小对该反应的反应热_______ (填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点_______ (填“升高”还是“降低”)。
(2)完成SO2氧化为SO3的热化学方程式_______ 。
II、氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,合成氨工业在国民生产中有重要意义。以下是关于合成氨的有关问题,请回答:
(3)若在一容积为2L的密闭容器中加入0.2mol的N2和0.6mol的H2在一定条件下发生反应:N2(g)+3H2(g) 2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)=
2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)=_______ 。平衡时H2的转化率为_______ %。
(4)平衡后,若提高H2的转化率,可以采取的措施有_______ (任写一项)。
(5)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:N2(g)+3H2(g) 2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示。请完成下列问题:
2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示。请完成下列问题:
①试比较K1、K2的大小,K1_______ K2(填“<、>、=”)
②400℃时,反应2NH3(g) N2(g)+3H2(g)的化学平衡常数为
N2(g)+3H2(g)的化学平衡常数为_______ 。当测得NH3、N2和H2物质的量分别为3mol、2mol和1mol时,则该反应的v(N2)正_______ v(N2)逆(填“<、>、=”)。
 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。
已知1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ·mol-1。请回答下列问题:
(1)E的大小对该反应的反应热
(2)完成SO2氧化为SO3的热化学方程式
II、氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,合成氨工业在国民生产中有重要意义。以下是关于合成氨的有关问题,请回答:
(3)若在一容积为2L的密闭容器中加入0.2mol的N2和0.6mol的H2在一定条件下发生反应:N2(g)+3H2(g)
 2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)=
2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)=(4)平衡后,若提高H2的转化率,可以采取的措施有
(5)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:N2(g)+3H2(g)
 2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示。请完成下列问题:
2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示。请完成下列问题:| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
①试比较K1、K2的大小,K1
②400℃时,反应2NH3(g)
 N2(g)+3H2(g)的化学平衡常数为
N2(g)+3H2(g)的化学平衡常数为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】I.回答下列问题:
(1)若在空气中加热MgCl2•6H2O,生成的是Mg(OH)Cl或MgO,写出生成Mg(OH)Cl关反应的化学方程式_______ 。
(2)用电解法制取金属镁时,需要无水氯化镁。需要在干燥的HCl气流中加热MgCl2•6H2O,才能得到无水MgCl2,其原因是_______ 。
II.现有常温下的0.1mol•L-1纯碱溶液。
(3)已知25℃时,Kh1=2×10-4,则当溶液中c(HCO ):c(CO
):c(CO )=2:1时,溶液的pH=
)=2:1时,溶液的pH=_______ 。
(4)0.1mol•L-1Na2CO3溶液中c(OH﹣)﹣c(H+)=_______ [用含c(HCO )、c(H2CO3)的关系式表示]。
)、c(H2CO3)的关系式表示]。
(5)向Na2CO3溶液中加入明矾会产生沉淀和气体,请写出相关的离子方程式_______ 。
(6)在化学分析中,以AgNO3标准溶液滴定溶液中的Cl﹣时,采用K2CrO4为指示剂,利用Ag+与CrO 反应生成砖红色沉淀指示滴定终点。当溶液中的Cl﹣恰好沉淀完全(浓度等于1.0×10-5mol•L﹣1)时,溶液中c(Ag+)=
反应生成砖红色沉淀指示滴定终点。当溶液中的Cl﹣恰好沉淀完全(浓度等于1.0×10-5mol•L﹣1)时,溶液中c(Ag+)=_______ mol•L﹣1,c(CrO )=
)=_______ mol•L﹣1。(已知25°C时Ag2CrO4、AgCl的Ksp分别为2.0×10-12和1.8×10-10)
(1)若在空气中加热MgCl2•6H2O,生成的是Mg(OH)Cl或MgO,写出生成Mg(OH)Cl关反应的化学方程式
(2)用电解法制取金属镁时,需要无水氯化镁。需要在干燥的HCl气流中加热MgCl2•6H2O,才能得到无水MgCl2,其原因是
II.现有常温下的0.1mol•L-1纯碱溶液。
(3)已知25℃时,Kh1=2×10-4,则当溶液中c(HCO
 ):c(CO
):c(CO )=2:1时,溶液的pH=
)=2:1时,溶液的pH=(4)0.1mol•L-1Na2CO3溶液中c(OH﹣)﹣c(H+)=
 )、c(H2CO3)的关系式表示]。
)、c(H2CO3)的关系式表示]。(5)向Na2CO3溶液中加入明矾会产生沉淀和气体,请写出相关的离子方程式
(6)在化学分析中,以AgNO3标准溶液滴定溶液中的Cl﹣时,采用K2CrO4为指示剂,利用Ag+与CrO
 反应生成砖红色沉淀指示滴定终点。当溶液中的Cl﹣恰好沉淀完全(浓度等于1.0×10-5mol•L﹣1)时,溶液中c(Ag+)=
反应生成砖红色沉淀指示滴定终点。当溶液中的Cl﹣恰好沉淀完全(浓度等于1.0×10-5mol•L﹣1)时,溶液中c(Ag+)= )=
)=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)砷酸 分步电离的平衡常数(25℃)为
分步电离的平衡常数(25℃)为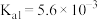 ,
,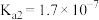 ,
,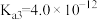 。
。 第一步水解的离子方程式为
第一步水解的离子方程式为___________ ,该步水解的平衡常数(25℃)为___________ 。
(2)以镁铝复合氧化物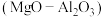 为载体的负载型镍铜双金属催化剂
为载体的负载型镍铜双金属催化剂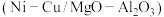 是一种新型高效加氢或脱氢催化剂,其制备流程如下:
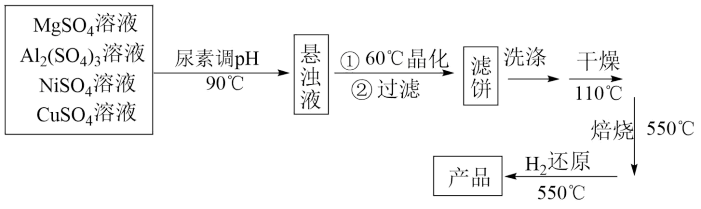
是一种新型高效加氢或脱氢催化剂,其制备流程如下:
已知:常温下,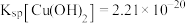 ,
,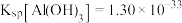 。回答下列问题:
。回答下列问题:
①在加热条件下,尿素 在水中发生水解反应,放出
在水中发生水解反应,放出___________ 和___________ 两种气体(写化学式)。
②“晶化”过程中,需保持恒温60℃,可采用的加热方式为___________
③“洗涤”过程中,检验滤饼是否洗净的方法是___________ 。
④常温下,若“悬浊液”中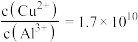 ,则溶液的
,则溶液的
___________ 。
(3)请写出泡沫灭火器灭火的原理___________ (用离子方程式表示)
(1)砷酸
 分步电离的平衡常数(25℃)为
分步电离的平衡常数(25℃)为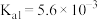 ,
,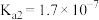 ,
,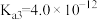 。
。 第一步水解的离子方程式为
第一步水解的离子方程式为(2)以镁铝复合氧化物
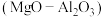 为载体的负载型镍铜双金属催化剂
为载体的负载型镍铜双金属催化剂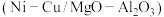 是一种新型高效加氢或脱氢催化剂,其制备流程如下:
是一种新型高效加氢或脱氢催化剂,其制备流程如下:
已知:常温下,
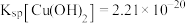 ,
,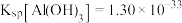 。回答下列问题:
。回答下列问题:①在加热条件下,尿素
 在水中发生水解反应,放出
在水中发生水解反应,放出②“晶化”过程中,需保持恒温60℃,可采用的加热方式为
③“洗涤”过程中,检验滤饼是否洗净的方法是
④常温下,若“悬浊液”中
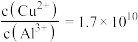 ,则溶液的
,则溶液的
(3)请写出泡沫灭火器灭火的原理
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】在一定条件下,金属单质X和非金属单质Y能够反应,生成化合物Z,Z能与水发生水解反应生成气体G和白色沉淀P(如下框图所示),已知气体G与空气之密度比约为1.17。请填空:

(1)组成单质X和Y的元素分别属第____________ 族和第___________ 族;
(2)Z与水发生水解反应方程式_____________________ ;
(3)每生成1mol的化合物Z,反应中转移_________________ mol的电子。

(1)组成单质X和Y的元素分别属第
(2)Z与水发生水解反应方程式
(3)每生成1mol的化合物Z,反应中转移
您最近一年使用:0次



