A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他物质已经略去):
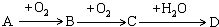
(1)若A是一种金属,C是淡黄色固体,写出C的一种用途_______ ;
(2)若A为淡黄色固体单质,写出D的浓溶液与铜反应的化学方程式______ ;
(3)若A是化合物,C是红棕色气体,则A的化学式为_____________ ;C转化为D的过程中,氧化剂与还原剂的质量比为__________________ 。
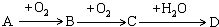
(1)若A是一种金属,C是淡黄色固体,写出C的一种用途
(2)若A为淡黄色固体单质,写出D的浓溶液与铜反应的化学方程式
(3)若A是化合物,C是红棕色气体,则A的化学式为
更新时间:2018-03-02 20:26:52
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A~I分别表示中学化学中常见的一种物质,其中A、I为常见金属,它们之间的相互关系如图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。请填写下列空白:
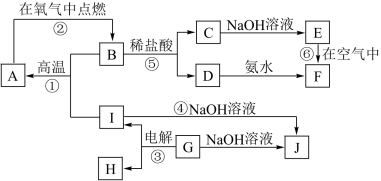
(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中的位置是________ 。
(2)写出C物质的化学式:________ 。
(3)写出①、⑥反应的化学方程式:
①:____________________________ 。
⑥:____________________________ 。
(4)从能量变化的角度看,反应①②③中,属于放热反应的是________ (填序号)。

(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中的位置是
(2)写出C物质的化学式:
(3)写出①、⑥反应的化学方程式:
①:
⑥:
(4)从能量变化的角度看,反应①②③中,属于放热反应的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知A与D均为非金属单质,其中A有多种同素异形体,其转化关系如下图。
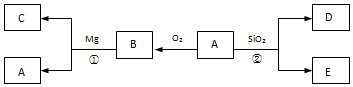
请回答:
(1)反应②为工业制粗硅原理,写出化学方程式:______ 。
(2)反应①可同时产生黑白两种固体的化学方程式为_____ 。

请回答:
(1)反应②为工业制粗硅原理,写出化学方程式:
(2)反应①可同时产生黑白两种固体的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下列物质的转化中,A、X是常见单质,Y在常温下为无色液体,B、C、D均为中学化学中常见的化合物,它们之间的转化关系如图所示(部分产物和反应条件已略去)。
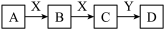
回答下列问题:
(1)若B为能导致酸雨的气体,则D的化学式可能是__ 。
(2)若C为淡黄色固体,D为强碱溶液,则C→D的离子方程式为__ 。
(3)若A为淡黄色固体,D为强酸,则D的浓溶液与碳反应生成气体B的化学方程式为__ 。
(4)若A为黄绿色气体,X为常见金属,则X与B溶液反应的离子方程式为__ 。下列试剂能鉴别B溶液与C溶液的是__ 。(填标号)
A.AgNO3溶液 B.KSCN溶液 C.盐酸 D.NaOH溶液

回答下列问题:
(1)若B为能导致酸雨的气体,则D的化学式可能是
(2)若C为淡黄色固体,D为强碱溶液,则C→D的离子方程式为
(3)若A为淡黄色固体,D为强酸,则D的浓溶液与碳反应生成气体B的化学方程式为
(4)若A为黄绿色气体,X为常见金属,则X与B溶液反应的离子方程式为
A.AgNO3溶液 B.KSCN溶液 C.盐酸 D.NaOH溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某研究小组为了探究硝酸的性质,进行如下实验操作。
(1)从试剂柜中取一瓶浓硝酸,发现其保存在_______ 色试剂瓶中,取少量浓硝酸于试管中,发现其溶液呈“黄色”,其原因是_______ (用化学方程式解释)。该研究小组尝试将显“黄色”的浓硝酸恢复到原本的无色。下列措施合理的是_______ (填字母)。
a.向浓硝酸中加水
b.向浓硝酸中通入适量空气
c.加热浓硝酸
d.向浓硝酸中加入适量的NaOH固体
(2)向浓硝酸中加入稍过量铜片,该小组同学发现,生成的气体开始呈红棕色后逐渐变浅,最终气体变为无色。试写出上述反应中刚开始产生红棕色气体的化学式:_______ ,在上述反应中,硝酸体现的性质为_______ 。
(3)当实验完毕,该小组同学向试管中滴入少量稀 ,发现铜片又逐渐溶解,产生无色气体,试写出上述反应的离子方程式:
,发现铜片又逐渐溶解,产生无色气体,试写出上述反应的离子方程式:_______ 。
(4)该小组同学向浓硝酸中加入少量碳粉,无明显现象,缓慢加热,发现碳粉逐渐溶解,产生红棕色气体,试写出上述反应的化学方程式:_______ ,在该反应中硝酸体现的性质为_______ 。
(1)从试剂柜中取一瓶浓硝酸,发现其保存在
a.向浓硝酸中加水
b.向浓硝酸中通入适量空气
c.加热浓硝酸
d.向浓硝酸中加入适量的NaOH固体
(2)向浓硝酸中加入稍过量铜片,该小组同学发现,生成的气体开始呈红棕色后逐渐变浅,最终气体变为无色。试写出上述反应中刚开始产生红棕色气体的化学式:
(3)当实验完毕,该小组同学向试管中滴入少量稀
 ,发现铜片又逐渐溶解,产生无色气体,试写出上述反应的离子方程式:
,发现铜片又逐渐溶解,产生无色气体,试写出上述反应的离子方程式:(4)该小组同学向浓硝酸中加入少量碳粉,无明显现象,缓慢加热,发现碳粉逐渐溶解,产生红棕色气体,试写出上述反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】下图为铜丝与浓硫酸反应并验证其产物性质的实验装置。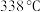 ,酒精灯可加热至
,酒精灯可加热至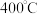 以上;ⅱ.给试管①加热前,先从导管②鼓入一段时间的
以上;ⅱ.给试管①加热前,先从导管②鼓入一段时间的 。
。
(1)试管①中反应的化学方程式是_______ 。
(2)加热一段时间后,试管①中产生了白雾,⑤⑥⑦中溶液均褪色。
ⅰ.试管⑤⑥⑦中的现象,分别说明 的性质:⑤
的性质:⑤_______ ,⑥_______ ,⑦_______ (填字母,下同)。
a.漂白性 b.氧化性 c.还原性 d.酸性氧化物的通性
ⅱ.下列叙述不正确的是_______ 。
a.上下移动铜丝可控制生成 的量
的量
b.上述实验结束后,发现①中试管内有少量白色固体出现,为确认白色固体为另一反应产物 ,可向试管①中加水,观察颜色
,可向试管①中加水,观察颜色
c.反应结束后,从导管②口向装置中通入空气,可使装置中残留气体完全被吸收,避免污染空气
d.导管②的作用为平衡气压
(3)若实验中换为铜片,取一定质量的铜片和一定体积的 的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生认为还有一定量的硫酸剩余,如果向其中加入硝酸钾可以使得剩余铜片溶解,请用离子反应方程式进行解释
的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生认为还有一定量的硫酸剩余,如果向其中加入硝酸钾可以使得剩余铜片溶解,请用离子反应方程式进行解释___ 。

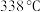 ,酒精灯可加热至
,酒精灯可加热至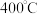 以上;ⅱ.给试管①加热前,先从导管②鼓入一段时间的
以上;ⅱ.给试管①加热前,先从导管②鼓入一段时间的 。
。(1)试管①中反应的化学方程式是
(2)加热一段时间后,试管①中产生了白雾,⑤⑥⑦中溶液均褪色。
ⅰ.试管⑤⑥⑦中的现象,分别说明
 的性质:⑤
的性质:⑤a.漂白性 b.氧化性 c.还原性 d.酸性氧化物的通性
ⅱ.下列叙述不正确的是
a.上下移动铜丝可控制生成
 的量
的量b.上述实验结束后,发现①中试管内有少量白色固体出现,为确认白色固体为另一反应产物
 ,可向试管①中加水,观察颜色
,可向试管①中加水,观察颜色c.反应结束后,从导管②口向装置中通入空气,可使装置中残留气体完全被吸收,避免污染空气
d.导管②的作用为平衡气压
(3)若实验中换为铜片,取一定质量的铜片和一定体积的
 的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生认为还有一定量的硫酸剩余,如果向其中加入硝酸钾可以使得剩余铜片溶解,请用离子反应方程式进行解释
的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生认为还有一定量的硫酸剩余,如果向其中加入硝酸钾可以使得剩余铜片溶解,请用离子反应方程式进行解释
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室利用废弃黄铜(主要成分为Zn和Cu)回收Cu并制备ZnO的部分实验过程如图所示:
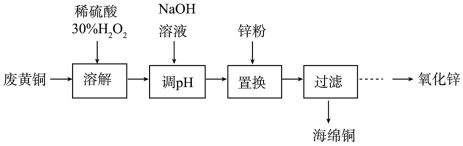
(1)为提高溶解速率,可以采取的措施有_______ (写2种)。
(2)“溶解”操作中一段时间后反应现象突然加剧,同时产生大量气体。
①反应过程中溶液的温度升高,其原因是_______ 。
②产生该现象的原因是(不考虑温度升高的影响)_______ 。
(3)相比用稀硝酸溶解废黄铜,该实验采用稀硫酸和H2O2溶解废黄铜的优点是_______ 。
(4)置换操作置换出铜单质,分离铜和锌。
①加入锌粉发生主要反应的离子方程式为_______ 。
②若没有“调pH”操作,对“置换”操作的影响是_______ 。

(1)为提高溶解速率,可以采取的措施有
(2)“溶解”操作中一段时间后反应现象突然加剧,同时产生大量气体。
①反应过程中溶液的温度升高,其原因是
②产生该现象的原因是(不考虑温度升高的影响)
(3)相比用稀硝酸溶解废黄铜,该实验采用稀硫酸和H2O2溶解废黄铜的优点是
(4)置换操作置换出铜单质,分离铜和锌。
①加入锌粉发生主要反应的离子方程式为
②若没有“调pH”操作,对“置换”操作的影响是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】化学实验是验证假设、推断结论的重要方法。某小组同学学习了氧化还原知识后,对碳与浓硫酸的反应及其产物进行验证,对 的性质进行了探究。
的性质进行了探究。
(1)盛放浓硫酸的仪器名称:_____ 。
(2)写出碳与浓硫酸在加热条件下反应的化学方程式:_____ 。
(3)证明产物中有水生成的实验现象_____ 。
(4)装置④的作用是_____ ,体现 的
的_____ 性(填氧化或漂白或还原)。
(5)装置⑤的作用是_____ 。
(6)证明产物中有 的实验现象是
的实验现象是_____ 。
(7)如何说明装置①的反应产物中有 ?
?_____ 。
(8)如何检验装置①反应后的圆底烧瓶中是否含有 离子?
离子?_____ 。
 的性质进行了探究。
的性质进行了探究。
(1)盛放浓硫酸的仪器名称:
(2)写出碳与浓硫酸在加热条件下反应的化学方程式:
(3)证明产物中有水生成的实验现象
(4)装置④的作用是
 的
的(5)装置⑤的作用是
(6)证明产物中有
 的实验现象是
的实验现象是(7)如何说明装置①的反应产物中有
 ?
?(8)如何检验装置①反应后的圆底烧瓶中是否含有
 离子?
离子?
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知有如图所示转化关系(反应条件略)。已知:
②相对分子质量:甲 乙。
乙。
③将甲的浓溶液露置在空气中一段时间,质量减小浓度降低;将乙的浓溶液露置在空气中一段时间,质量增加浓度降低。
请完成下列空白:
(1)Z是(写分子式):___________ 。
(2)将甲的浓溶液露置在空气中一段时间,质量减小浓度降低,说明甲有___________ 性,甲的浓溶液盛放在棕色试剂瓶中,其原因是___________ (用化学方程式表示)。
(3)在X与Z的反应中,被氧化的X与被还原的X的物质的量之比是___________ 。
(4)W可用于工业制溴过程中吸收潮湿空气中的 。写出该反应的化学方程式:
。写出该反应的化学方程式:___________ 。
(5)欲除去Y中混有的W,下列试剂可供选用的是___________。
(6)工业上运输甲、乙两种浓溶液可选用___________ (金属名称)金属材料的运输罐,所选用的金属能做运输罐的理由是___________ 。
(7)写出M与乙的浓溶液在加热条件下反应的化学方程式:___________ 。

②相对分子质量:甲
 乙。
乙。③将甲的浓溶液露置在空气中一段时间,质量减小浓度降低;将乙的浓溶液露置在空气中一段时间,质量增加浓度降低。
请完成下列空白:
(1)Z是(写分子式):
(2)将甲的浓溶液露置在空气中一段时间,质量减小浓度降低,说明甲有
(3)在X与Z的反应中,被氧化的X与被还原的X的物质的量之比是
(4)W可用于工业制溴过程中吸收潮湿空气中的
 。写出该反应的化学方程式:
。写出该反应的化学方程式:(5)欲除去Y中混有的W,下列试剂可供选用的是___________。
| A.品红溶液 | B.酸性高锰酸钾溶液 | C.氢氧化钠溶液 | D.饱和 溶液 溶液 |
(6)工业上运输甲、乙两种浓溶液可选用
(7)写出M与乙的浓溶液在加热条件下反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】铁是日常生活中用途最广、用量最大的金属材料。
(1)某实验小组利用下图装置验证铁与水蒸气的反应。

①试管中反应的化学方程式是___________ 。
②实验结束后,取出少量反应后的固体于试管中,加入过量盐酸,固体完全溶解,所得溶液中存在的阳离子是___________ (填序号)。
a.一定有Fe2+、H+和Fe3+
b.一定有Fe2+、H+,可能有Fe3+
c.一定有Fe2+、Fe3+,可能有H+
d.一定有Fe3+、H+,可能有Fe2+
(2)另称取一定量的铁钉放入适量的浓硫酸中,加热,充分反应后收集气体。经测定气体中含有SO2、CO2和H2。
①气体中混有CO2的原因是(用化学方程式表示)___________ 。
②将672mL(标准状况)收集到的气体通入足量溴水中,发生反应:SO2+Br2+2H2O=2HBr+H2SO4,然后加入足量BaCl2溶液,经洗涤、干燥得到固体4.66g。由此推知收集到的气体中SO2的体积分数是______ 。
(1)某实验小组利用下图装置验证铁与水蒸气的反应。

①试管中反应的化学方程式是
②实验结束后,取出少量反应后的固体于试管中,加入过量盐酸,固体完全溶解,所得溶液中存在的阳离子是
a.一定有Fe2+、H+和Fe3+
b.一定有Fe2+、H+,可能有Fe3+
c.一定有Fe2+、Fe3+,可能有H+
d.一定有Fe3+、H+,可能有Fe2+
(2)另称取一定量的铁钉放入适量的浓硫酸中,加热,充分反应后收集气体。经测定气体中含有SO2、CO2和H2。
①气体中混有CO2的原因是(用化学方程式表示)
②将672mL(标准状况)收集到的气体通入足量溴水中,发生反应:SO2+Br2+2H2O=2HBr+H2SO4,然后加入足量BaCl2溶液,经洗涤、干燥得到固体4.66g。由此推知收集到的气体中SO2的体积分数是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】I.现有一定量含有Na2O杂质的Na2O2试样,用如图所示的实验装置测定Na2O2试样的纯度(通过CO2与样品反应后生成O2的量测定Na2O2的含量。可供选用的反应物:CaCO3固体、盐酸、硫酸溶液和蒸馏水)。回答下列问题:_______ 。
(2)装置B中除杂反应的离子方程式为_______ 。
(3)装置D中反应的主要化学方程式为_______ 。
(4)装置E中碱石灰的主要作用是______ 。
(5)已知装置D中试样质量为19.5g,装置G中所得O2体积为1120mL(已折算成标准状况下体积,且O2全部逸出)。求试样中Na2O2的质量分数_______ 。
II.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如图:_______ 。
A.先通CO2再通NH3
B.先通NH3再通CO2
(7)请写出反应Ⅰ的化学方程式______ 。
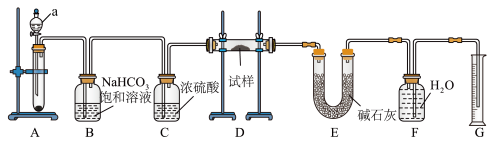
(2)装置B中除杂反应的离子方程式为
(3)装置D中反应的主要化学方程式为
(4)装置E中碱石灰的主要作用是
(5)已知装置D中试样质量为19.5g,装置G中所得O2体积为1120mL(已折算成标准状况下体积,且O2全部逸出)。求试样中Na2O2的质量分数
II.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如图:

A.先通CO2再通NH3
B.先通NH3再通CO2
(7)请写出反应Ⅰ的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室里常用Na2O2与H2O反应快速制取少量的O2,下面装置用来制取O2并演示Na在O2中的燃烧实验。

(1)关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴,直至全部流入试管。试判断装置是否漏气________ (填“漏气”“不漏气”或“无法确定”),判断理由是_______________ 。
(2)写出A装置中反应的化学方程式_____________________________________ 。
(3)D装置中盛放的试剂是_____________ ,作用是_________________________ 。

(1)关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴,直至全部流入试管。试判断装置是否漏气
(2)写出A装置中反应的化学方程式
(3)D装置中盛放的试剂是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选择适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可作供氧剂。
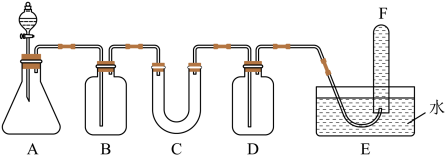
(1)①A是实验室制取CO2的装置。写出A中发生反应的离子方程式________ 。
②B中盛有饱和NaHCO3溶液,其作用是__________ 。
③写出C中发生的反应的化学方程式(有几个写几个)___________ 。
④D装置的目的是用NaOH溶液除去多余的CO2,则D中反应的离子方程式是______ 。
(2)从离子反应的角度判断CuSO4溶液和Na2O2的反应,试写出其总离子反应方程式______ 。

(1)①A是实验室制取CO2的装置。写出A中发生反应的离子方程式
②B中盛有饱和NaHCO3溶液,其作用是
③写出C中发生的反应的化学方程式(有几个写几个)
④D装置的目的是用NaOH溶液除去多余的CO2,则D中反应的离子方程式是
(2)从离子反应的角度判断CuSO4溶液和Na2O2的反应,试写出其总离子反应方程式
您最近一年使用:0次



