如图是人类从海水资源中提取某些重要化工原料的流程示意图:
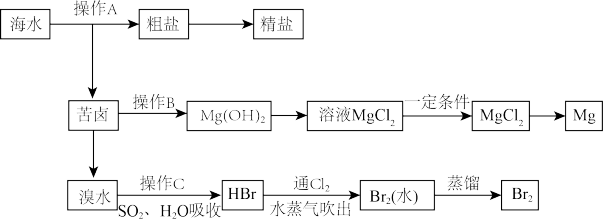
请回答下列问题:
(1)粗盐中含有Ca2+、Mg2+、SO 等杂质,精制时所用试剂为:A.盐酸;B.BaCl2溶液;C.NaOH溶液;D.Na2CO3溶液。加入试剂的顺序是:
等杂质,精制时所用试剂为:A.盐酸;B.BaCl2溶液;C.NaOH溶液;D.Na2CO3溶液。加入试剂的顺序是:____ 。
(2)电解饱和食盐水的化学反应方程式为____ 。
(3)与电源负极相连的电极附近溶液pH____ (填“变大、不变”或“变小”)。
(4)操作B需加入下列试剂中的一种,最合适的是____ (填字母)。
(5)向苦卤中通入Cl2,发生反应的离子方程式是____ 。
(6)溴水中通入二氧化硫和水的反应为SO2+Br2+2H2O=2HBr+H2SO4,请用单线桥标出该反应电子转移的方向和数目____ 。

请回答下列问题:
(1)粗盐中含有Ca2+、Mg2+、SO
 等杂质,精制时所用试剂为:A.盐酸;B.BaCl2溶液;C.NaOH溶液;D.Na2CO3溶液。加入试剂的顺序是:
等杂质,精制时所用试剂为:A.盐酸;B.BaCl2溶液;C.NaOH溶液;D.Na2CO3溶液。加入试剂的顺序是:(2)电解饱和食盐水的化学反应方程式为
(3)与电源负极相连的电极附近溶液pH
(4)操作B需加入下列试剂中的一种,最合适的是
| A.氢氧化钠溶液 | B.澄清石灰水 | C.石灰乳 | D.碳酸钠溶液 |
(6)溴水中通入二氧化硫和水的反应为SO2+Br2+2H2O=2HBr+H2SO4,请用单线桥标出该反应电子转移的方向和数目
更新时间:2022-09-19 22:33:43
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
【推荐1】海水中有丰富的资源,多种多样的海洋动物、植物、矿藏等。如图是从海水中提取某些物质的示意图。已知:海水中含量最高的几种离子的浓度依次为

请根据以上信息回答下列问题:
(1)写出步骤②的操作名称_______ ;实验室中步骤⑤所需的玻璃仪器除烧杯外,还需要的仪器是___________ 。
(2)D具有杀菌消毒的作用,请写出反应④的离子方程式___________ 。
(3)初步提纯后的粗盐中含有等Ca2+、Mg2+、 等杂质,精制得到精盐的步骤顺序为
等杂质,精制得到精盐的步骤顺序为________ 。(用字母序号填空)
a.加适量盐酸;b.加稍过量的氯化钡溶液,再加稍过量的NaOH溶液;c.过滤;d.蒸发结晶;e.加稍过量碳酸钠溶液
(4)____________ (填“能”或“不能”)用 一种试剂替代步骤②中两种试剂,理由是
一种试剂替代步骤②中两种试剂,理由是________ 。
| 微粒种类 | Cl- | Na+ | Mg2+ |  | Ca2+ |
| 微粒浓度 | 0.55mol·L-1 | 0.47mol·L-1 | 0.054mol·L-1 | 0.027mol·L-1 | 0.01mol·L-1 |

请根据以上信息回答下列问题:
(1)写出步骤②的操作名称
(2)D具有杀菌消毒的作用,请写出反应④的离子方程式
(3)初步提纯后的粗盐中含有等Ca2+、Mg2+、
 等杂质,精制得到精盐的步骤顺序为
等杂质,精制得到精盐的步骤顺序为a.加适量盐酸;b.加稍过量的氯化钡溶液,再加稍过量的NaOH溶液;c.过滤;d.蒸发结晶;e.加稍过量碳酸钠溶液
(4)
 一种试剂替代步骤②中两种试剂,理由是
一种试剂替代步骤②中两种试剂,理由是
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】化学科学可以帮助我们安全、合理、有效地开发自然资源和使用各种化学品,为建设美丽家园发挥重要价值。
Ⅰ.工业海水淡化及从海水中提取溴的过程如下:
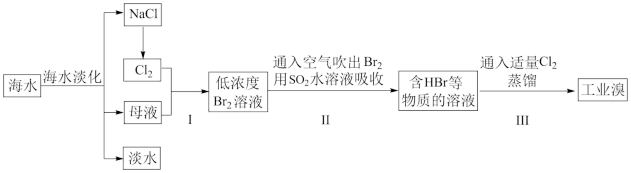
请回答下列问题:
(1)历史最久,技术和工艺也比较成熟,但成本较高的海水淡化的方法是_______ 。法。
(2)从海水中可以得到食盐,为了除去粗盐中的Ca2+、Mg2+、SO ,可将粗盐溶于水,然后进行下列五项操作:①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液。正确的操作顺序是_______。(填字母)。
,可将粗盐溶于水,然后进行下列五项操作:①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液。正确的操作顺序是_______。(填字母)。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是_______ 。
(4)步骤Ⅱ用SO2和水吸收Br2,反应的离子方程式为_______ 。
Ⅱ.亚硝酸钠(NaNO2)是生活中广泛应用的一种化学品,实验室可用如图装置制备(略去部分夹持仪器)。
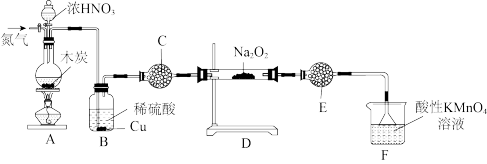
已知:①2NO+Na2O2=2NaNO2
②2NO2+Na2O2=2NaNO3
③酸性条件下,NO、NO2和NO 都能与MnO
都能与MnO 反应生成NO
反应生成NO 和Mn2+
和Mn2+
请回答下列问题:
(5)装置A中发生反应的化学方程式为_______ 。
(6)装置C的作用为_______ ,装置E的作用为_______ 。
(7)装置F中发生反应的离子方程式为_______ 。
(8)为测定亚硝酸钠的含量,进行如下操作:称取3.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,再向锥形瓶中加入0.1000mol·L-1酸性KMnO4溶液16.00mL,两者恰好完全反应。计算所得固体中亚硝酸钠的质量分数为_______ (保留四位有效数字)。
Ⅰ.工业海水淡化及从海水中提取溴的过程如下:

请回答下列问题:
(1)历史最久,技术和工艺也比较成熟,但成本较高的海水淡化的方法是
(2)从海水中可以得到食盐,为了除去粗盐中的Ca2+、Mg2+、SO
 ,可将粗盐溶于水,然后进行下列五项操作:①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液。正确的操作顺序是_______。(填字母)。
,可将粗盐溶于水,然后进行下列五项操作:①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液。正确的操作顺序是_______。(填字母)。| A.⑤④②③① | B.④①②⑤③ | C.②⑤④①③ | D.②④⑤①③ |
(4)步骤Ⅱ用SO2和水吸收Br2,反应的离子方程式为
Ⅱ.亚硝酸钠(NaNO2)是生活中广泛应用的一种化学品,实验室可用如图装置制备(略去部分夹持仪器)。

已知:①2NO+Na2O2=2NaNO2
②2NO2+Na2O2=2NaNO3
③酸性条件下,NO、NO2和NO
 都能与MnO
都能与MnO 反应生成NO
反应生成NO 和Mn2+
和Mn2+请回答下列问题:
(5)装置A中发生反应的化学方程式为
(6)装置C的作用为
(7)装置F中发生反应的离子方程式为
(8)为测定亚硝酸钠的含量,进行如下操作:称取3.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,再向锥形瓶中加入0.1000mol·L-1酸性KMnO4溶液16.00mL,两者恰好完全反应。计算所得固体中亚硝酸钠的质量分数为
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】查阅资料知:Br2的沸点为58.8 ℃,密度为3.119 g·cm-3,微溶于水,有毒。
Ⅰ.(1)常温下,单质溴通常呈________ 态,保存时通常在盛溴的试剂瓶中加入少量________ 。
Ⅱ.工业生产中,海水提取溴常用热空气吹出法。其生产流程如下:

某化学实验小组模拟该法设计了如下实验装置(夹持装置略去)从浓缩的海水中提取液溴。实验步骤如下:
①关闭活塞b、d,打开活塞a、c,向A中缓慢通入Cl2至反应结束;
②关闭a、c,打开b、d,向A中鼓入足量热空气;
③关闭b,打开a,再通过A向B中通入足量的Cl2;
④将B中所得液体进行蒸馏,收集液溴。

(2)当观察到A中液面上方出现________ (实验现象)时即可判断步骤①中反应已经结束。
(3)X试剂可以是________ (填字母,下同),尾气处理选用________ 。
a.H2O b.饱和食盐水 c.氢氧化钠溶液 d.饱和Na2SO3溶液
B中X试剂发生反应的离子方程式为________________________________ 。
(4)蒸馏时应该选择______ (填序号),操作中应控制的关键实验条件为____________ 。
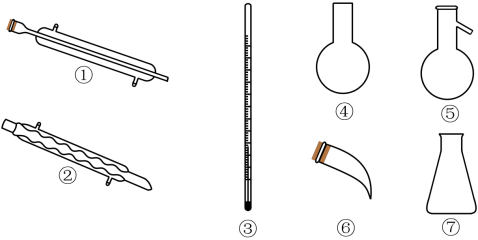
Ⅲ.该实验小组利用制得的单质溴研究H2与Br2生成HBr的反应,实验装置如下:

(5)E装置可用来检验反应产物HBr,则D装置的作用是_______ 。若要检验E中收集的HBr,图示装置检验HBr还不够完善,请结合原有实验装置予以改进:__________ 。
Ⅰ.(1)常温下,单质溴通常呈
Ⅱ.工业生产中,海水提取溴常用热空气吹出法。其生产流程如下:

某化学实验小组模拟该法设计了如下实验装置(夹持装置略去)从浓缩的海水中提取液溴。实验步骤如下:
①关闭活塞b、d,打开活塞a、c,向A中缓慢通入Cl2至反应结束;
②关闭a、c,打开b、d,向A中鼓入足量热空气;
③关闭b,打开a,再通过A向B中通入足量的Cl2;
④将B中所得液体进行蒸馏,收集液溴。

(2)当观察到A中液面上方出现
(3)X试剂可以是
a.H2O b.饱和食盐水 c.氢氧化钠溶液 d.饱和Na2SO3溶液
B中X试剂发生反应的离子方程式为
(4)蒸馏时应该选择

Ⅲ.该实验小组利用制得的单质溴研究H2与Br2生成HBr的反应,实验装置如下:

(5)E装置可用来检验反应产物HBr,则D装置的作用是
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】海洋资源的利用具有广阔前景。
(1)下列不属于海水淡化的方法________ (填序号)。
A.蒸馏法 B.离子交换法
C.过滤法 D.电渗析法
(2)如图是从海水中提取镁的简单流程。

①试剂B是________ (填化学式)。
②由无水MgCl2制取Mg的化学方程式是__________________________________________
(3)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:
海带 海带灰
海带灰 海带灰悬浊液
海带灰悬浊液 含I-溶液
含I-溶液 含I2水溶液
含I2水溶液 含I2苯溶液
含I2苯溶液 单质I2
单质I2
Ⅰ.下列不属于步骤①操作所用的仪器是________ (填序号)。
A.酒精灯 B.漏斗
C.坩埚 D.泥三角
Ⅱ.步骤③的实验操作名称是________ 。
Ⅲ.④步骤反应的离子方程式____________________________________________________
(1)下列不属于海水淡化的方法
A.蒸馏法 B.离子交换法
C.过滤法 D.电渗析法
(2)如图是从海水中提取镁的简单流程。

①试剂B是
②由无水MgCl2制取Mg的化学方程式是
(3)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:
海带
 海带灰
海带灰 海带灰悬浊液
海带灰悬浊液 含I-溶液
含I-溶液 含I2水溶液
含I2水溶液 含I2苯溶液
含I2苯溶液 单质I2
单质I2Ⅰ.下列不属于步骤①操作所用的仪器是
A.酒精灯 B.漏斗
C.坩埚 D.泥三角
Ⅱ.步骤③的实验操作名称是
Ⅲ.④步骤反应的离子方程式
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】请分析海水提镁、海带提碘的主要过程,按要求回答下列问题。
(1)海水提镁
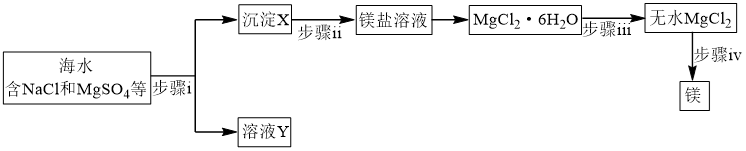
① 在周期表中位于
在周期表中位于_______ 区。
②步骤ⅰ所需试剂属于(填“强酸”、“强碱”或“可溶盐”)_______ 溶液。
③步骤ⅱ反应的离子方程式为_______ 。
④步骤ⅲ系列操作中需在 氛围中进行原因为
氛围中进行原因为_______ 。
⑤步骤ⅳ惰性电极电解熔融 时,在
时,在_______ 极每产生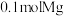 时,电路中转移电子数目为
时,电路中转移电子数目为_______ 。
(2)海带提碘(碘元素在海带中碘化物形式存在,碘为微溶于水的紫黑色固体)
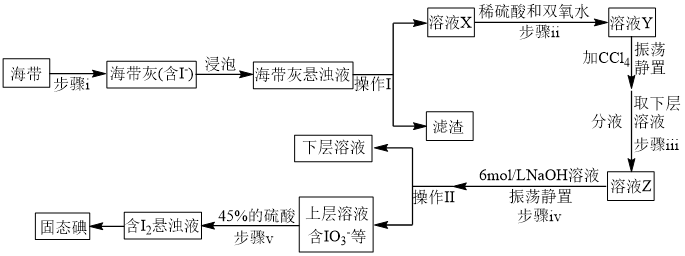
①步骤ⅰ不会用到下列仪器中的_______ (填字母)
a.酒精灯 b.漏斗 c.坩埚 d.泥三角
②操作Ⅰ、Ⅱ的名称依次为_______ 、_______ 。
③步骤ⅱ反应的离子方程式为_______ 。
④步骤ⅲ到步骤Ⅴ的目的是_______ 。
⑤步骤Ⅴ中 参与反应的离子方程式为
参与反应的离子方程式为_______ 。
(1)海水提镁

①
 在周期表中位于
在周期表中位于②步骤ⅰ所需试剂属于(填“强酸”、“强碱”或“可溶盐”)
③步骤ⅱ反应的离子方程式为
④步骤ⅲ系列操作中需在
 氛围中进行原因为
氛围中进行原因为⑤步骤ⅳ惰性电极电解熔融
 时,在
时,在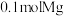 时,电路中转移电子数目为
时,电路中转移电子数目为(2)海带提碘(碘元素在海带中碘化物形式存在,碘为微溶于水的紫黑色固体)

①步骤ⅰ不会用到下列仪器中的
a.酒精灯 b.漏斗 c.坩埚 d.泥三角
②操作Ⅰ、Ⅱ的名称依次为
③步骤ⅱ反应的离子方程式为
④步骤ⅲ到步骤Ⅴ的目的是
⑤步骤Ⅴ中
 参与反应的离子方程式为
参与反应的离子方程式为
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】海水是巨大的资源宝库,海水淡化及其综合利用具有重要意义。
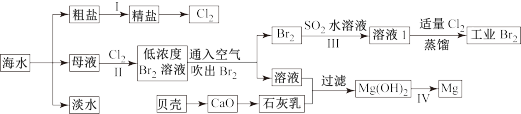
请回答下列问题:
Ⅰ.(1)步骤1中,粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,粗盐精制过程中要使用Na2CO3溶液,请写出加入Na2CO3溶液后相关化学反应的离子方程式_________________ 。
(2)海水提溴,制得1mol Br2需要消耗_________ mol Cl2。步骤Ⅱ中需要向母液中加入稀硫酸酸化,其作用是___________________________ 。步骤Ⅲ若用Na2SO3水溶液吸收Br2,有关反应的离子方程式为_______________________________ 。
(3)为了从工业Br2中提纯溴,除去产物中残留的少量Cl2,可向其中加入__________ 溶液。
Ⅱ.(1)Mg在元素周期表中的位置:_____________ ,Mg(OH)2的电子式:____________ ,Mg(OH)2中所含元素的简单离子半径由小到大的顺序是____________________________ 。
(2)步骤Ⅳ由Mg(OH)2得到单质Mg,以下方法最合适的是_______________ (填序号)。
A.Mg(OH)2→MgCl2 Mg B. Mg(OH)2
Mg B. Mg(OH)2 MgO
MgO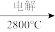 Mg
Mg
C. Mg(OH)2 MgO
MgO  Mg D. Mg(OH)2
Mg D. Mg(OH)2 无水MgCl2
无水MgCl2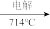 Mg
Mg
(3)判断Mg(OH)2是否洗涤干净的操作是__________________ 。
Ⅲ. 用Mg制成的格氏试剂(RMgBr)常用于有机合成,例如制备醇类化合物的合成路线如下:
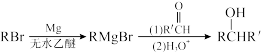 (R:烃基: R':烃基或H)依据上述信息,写出制备
(R:烃基: R':烃基或H)依据上述信息,写出制备 所需溴代烃的可能结构简式:
所需溴代烃的可能结构简式: ___________ 。

请回答下列问题:
Ⅰ.(1)步骤1中,粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,粗盐精制过程中要使用Na2CO3溶液,请写出加入Na2CO3溶液后相关化学反应的离子方程式
(2)海水提溴,制得1mol Br2需要消耗
(3)为了从工业Br2中提纯溴,除去产物中残留的少量Cl2,可向其中加入
Ⅱ.(1)Mg在元素周期表中的位置:
(2)步骤Ⅳ由Mg(OH)2得到单质Mg,以下方法最合适的是
A.Mg(OH)2→MgCl2
 Mg B. Mg(OH)2
Mg B. Mg(OH)2 MgO
MgO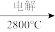 Mg
MgC. Mg(OH)2
 MgO
MgO  Mg D. Mg(OH)2
Mg D. Mg(OH)2 无水MgCl2
无水MgCl2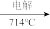 Mg
Mg(3)判断Mg(OH)2是否洗涤干净的操作是
Ⅲ. 用Mg制成的格氏试剂(RMgBr)常用于有机合成,例如制备醇类化合物的合成路线如下:
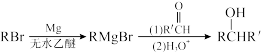 (R:烃基: R':烃基或H)依据上述信息,写出制备
(R:烃基: R':烃基或H)依据上述信息,写出制备 所需溴代烃的可能结构简式:
所需溴代烃的可能结构简式:
您最近半年使用:0次



