高锰酸钾为紫黑色、细长的棱形结晶或颗粒,是一种强氧化剂,可溶于水,常用作消毒剂、水净化剂、氧化剂、漂白剂、毒气吸收剂等。
Ⅰ.制备KMnO4
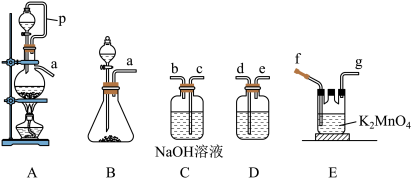
(1)若实验室选用A装置制备Cl2,导管P的作用为_______ 。
(2)若实验室选用B装置制备氯气,当锥形瓶中放置的药品为漂粉精,则对应的化学反应方程式为_______ 。
(3)用氯气氧化K2MnO4制备KMnO4,则其接口顺序为a→_______ (按气流方向从左到右,用小写字母表示)。
(4)工业上采用惰性电极隔膜法电解,可制得KMnO4.装置如图:
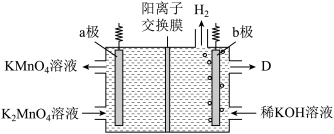
写出电解总反应的化学方程式:_______ 。
Ⅱ.测定KMnO4产品的纯度
称取2.400 0 g样品溶于水,加入硫酸酸化后配成100.00 mL溶液,用移液管取20.00 mL置于锥形瓶中,用0.500 0 mol·L-1标准(NH4)2Fe(SO4)2溶液进行滴定。
(5)滴定终点的现象是_______ 。
(6)数据处理。将三次实验消耗(NH4)2Fe(SO4)2溶液体积取平均值为30.00 mL。计算该KMnO4产品的质量分数为_______ %(保留小数点后两位)。
(7)进一步分析发现,测定结果偏高,其原因可能是_______(填标号)。
Ⅰ.制备KMnO4

(1)若实验室选用A装置制备Cl2,导管P的作用为
(2)若实验室选用B装置制备氯气,当锥形瓶中放置的药品为漂粉精,则对应的化学反应方程式为
(3)用氯气氧化K2MnO4制备KMnO4,则其接口顺序为a→
(4)工业上采用惰性电极隔膜法电解,可制得KMnO4.装置如图:

写出电解总反应的化学方程式:
Ⅱ.测定KMnO4产品的纯度
称取2.400 0 g样品溶于水,加入硫酸酸化后配成100.00 mL溶液,用移液管取20.00 mL置于锥形瓶中,用0.500 0 mol·L-1标准(NH4)2Fe(SO4)2溶液进行滴定。
(5)滴定终点的现象是
(6)数据处理。将三次实验消耗(NH4)2Fe(SO4)2溶液体积取平均值为30.00 mL。计算该KMnO4产品的质量分数为
(7)进一步分析发现,测定结果偏高,其原因可能是_______(填标号)。
| A.洗涤后,锥形瓶未干燥直接加入待测的KMnO4溶液 |
| B.装液前,滴定管水洗后没有用标准液润洗 |
| C.滴定前仰视读数,滴定后俯视读数 |
| D.标准(NH4)2Fe(SO4)2溶液部分氧化变质 |
22-23高三上·河南·阶段练习 查看更多[4]
河南省顶级名校2022-2023学年高三上学期第一次月考化学试题河南省濮阳市南乐县第一高级中学2022-2023学年高三上学期10月月考化学试题湖南省长沙市第一中学2022-2023学年高三上学期月考(一)化学试题(已下线)回归教材重难点11 熟记“五气体”制备实验、“两定量”测定实验-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)
更新时间:2022-09-30 10:25:48
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】 可用于制备补铁剂。以磁铁矿(主要成分为
可用于制备补铁剂。以磁铁矿(主要成分为 ,含
,含 和
和 等杂质)为原料制取
等杂质)为原料制取 的工艺流程如下图:
的工艺流程如下图:

回答下列问题:
(1)将磁铁矿制成粉的目的是___________ 。
(2)滤渣1的成分是___________ (填化学式)。
(3)“转化”工序加入Fe的作用是___________ 。
(4)“调pH”时发生反应的离子方程式为___________ 。
(5)“沉铁”过程得到的“X溶液”中的主要溶质为___________ (填化学式)。
(6)①产品 在空气中煅烧可制备铁红,写出反应的化学方程式:
在空气中煅烧可制备铁红,写出反应的化学方程式:___________ 。
②在实验室中完成本操作需使用到的实验仪器(除泥三角外)有___________ (填标号)。
A.蒸发皿 B.试管 C.坩埚 D.三脚架 E.坩埚钳 F.酒精灯
③若起始时 的质量为ag,最终制得bg
的质量为ag,最终制得bg ,则
,则 产率为
产率为___________ (用含a和b的代数式表示)。
 可用于制备补铁剂。以磁铁矿(主要成分为
可用于制备补铁剂。以磁铁矿(主要成分为 ,含
,含 和
和 等杂质)为原料制取
等杂质)为原料制取 的工艺流程如下图:
的工艺流程如下图:
回答下列问题:
(1)将磁铁矿制成粉的目的是
(2)滤渣1的成分是
(3)“转化”工序加入Fe的作用是
(4)“调pH”时发生反应的离子方程式为
(5)“沉铁”过程得到的“X溶液”中的主要溶质为
(6)①产品
 在空气中煅烧可制备铁红,写出反应的化学方程式:
在空气中煅烧可制备铁红,写出反应的化学方程式:②在实验室中完成本操作需使用到的实验仪器(除泥三角外)有
A.蒸发皿 B.试管 C.坩埚 D.三脚架 E.坩埚钳 F.酒精灯
③若起始时
 的质量为ag,最终制得bg
的质量为ag,最终制得bg ,则
,则 产率为
产率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】一种制备氢氧化镁产品的生产流程如图所示,MgCl2和NaOH按恰好完全反应的比例加料。

(1)写出步骤c中发生反应的化学方程式:_____ 。
(2)x=_____ 。
(3)在反应池中进行步骤c,历时10分钟,得到的产品质量是_________ 。
(4)如图流程中若用下列物质代替氢氧化钠,也能制得氢氧化镁的是_____ 。
①盐酸 ②氯化钙 ③氨水 ④硫酸镁

(1)写出步骤c中发生反应的化学方程式:
(2)x=
(3)在反应池中进行步骤c,历时10分钟,得到的产品质量是
(4)如图流程中若用下列物质代替氢氧化钠,也能制得氢氧化镁的是
①盐酸 ②氯化钙 ③氨水 ④硫酸镁
您最近一年使用:0次
【推荐3】黄铜矿(CuFeS2)是一种铜铁硫化物矿物,常含微量的金、银等。黄铜矿是冶炼铜及制备铁氧化物的重要矿藏。以黄铜矿为主要原料生产铜、铁红(氧化铁)的工艺流程如下所示:
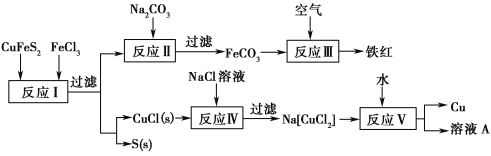
已知:CuFeS2中Cu为+2价。
请回答下列问题:
(1)CuFeS2中Fe的化合价为____________ 。
(2)写出反应Ⅰ的离子方程式:_______________________________ ,该反应的氧化剂是________ 。
(3)CuCl难溶于水,但可与过量的Cl-反应生成可溶于水的[CuCl2]-。该反应的离子方程式为__________________ 。
(4)反应Ⅰ~Ⅳ 4个反应中属于非氧化还原反应的是反应________ (选填“Ⅰ~Ⅳ”)。
(5)反应Ⅴ中Na[CuCl2]既是氧化剂,又是还原剂,由此可推知“溶液A”中的溶质为___ (写出化学式)。

已知:CuFeS2中Cu为+2价。
请回答下列问题:
(1)CuFeS2中Fe的化合价为
(2)写出反应Ⅰ的离子方程式:
(3)CuCl难溶于水,但可与过量的Cl-反应生成可溶于水的[CuCl2]-。该反应的离子方程式为
(4)反应Ⅰ~Ⅳ 4个反应中属于非氧化还原反应的是反应
(5)反应Ⅴ中Na[CuCl2]既是氧化剂,又是还原剂,由此可推知“溶液A”中的溶质为
您最近一年使用:0次



