在2L密闭容器中,在一定条件下进行合成氨的反应3H2+N2 2NH3,先加入H2和N2各2mol,反应经2min钟后,测得N2的物质的量浓度为0.8mol/L,H2的物质的量浓度为0.4mol/L,NH3的物质的量浓度为0.4mol/L。求此反应的化学反应速率是多少
2NH3,先加入H2和N2各2mol,反应经2min钟后,测得N2的物质的量浓度为0.8mol/L,H2的物质的量浓度为0.4mol/L,NH3的物质的量浓度为0.4mol/L。求此反应的化学反应速率是多少____ ?
 2NH3,先加入H2和N2各2mol,反应经2min钟后,测得N2的物质的量浓度为0.8mol/L,H2的物质的量浓度为0.4mol/L,NH3的物质的量浓度为0.4mol/L。求此反应的化学反应速率是多少
2NH3,先加入H2和N2各2mol,反应经2min钟后,测得N2的物质的量浓度为0.8mol/L,H2的物质的量浓度为0.4mol/L,NH3的物质的量浓度为0.4mol/L。求此反应的化学反应速率是多少
更新时间:2022-09-19 23:13:37
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】I.碳元素广泛存在于自然界中,对人类生命和生活具有重要意义。含碳化合物在工业生产和国防建设中有广泛的应用。
(1)碳元素原子核外有_____ 个未成对电子,最外层有_____ 种能量不同的电子。CH4 分子的空间构型为_____ ,是_____ 分子。(填“极性”或“非极性”)
(2)碳和硅是同主族元素,下列能说明二者非金属性相对强弱的是_____ (填编号)
a.CH4的稳定性比SiH4强 b.SiH4的沸点比CH4高
c.碳酸是强酸,硅酸是弱酸 d.碳原子半径比硅原子小
II.氮化硅(Si3N4)是一种重要的陶瓷材料,可用石英与焦炭在800℃氮气气氛下合成:3SiO2(s)+6C(s)+2N2(g) Si3N4(s)+6CO(g)
Si3N4(s)+6CO(g)
(1)该反应的平衡常数表达式K_____ 。已知平衡常数:K(800℃)>K(850℃),则正反应是__________ 反应(填“放热”或“吸热”)
(2)任写两种能提高二氧化硅转化率的措施_____ 、_____ 。
(3)一定温度下,在2 L密闭容器内,充入一定量的反应物,5分钟时达到平衡,测得容器内气体增加了0.4mol,用CO表示该反应时间内的反应速率为_____ 。
(1)碳元素原子核外有
(2)碳和硅是同主族元素,下列能说明二者非金属性相对强弱的是
a.CH4的稳定性比SiH4强 b.SiH4的沸点比CH4高
c.碳酸是强酸,硅酸是弱酸 d.碳原子半径比硅原子小
II.氮化硅(Si3N4)是一种重要的陶瓷材料,可用石英与焦炭在800℃氮气气氛下合成:3SiO2(s)+6C(s)+2N2(g)
 Si3N4(s)+6CO(g)
Si3N4(s)+6CO(g)(1)该反应的平衡常数表达式K
(2)任写两种能提高二氧化硅转化率的措施
(3)一定温度下,在2 L密闭容器内,充入一定量的反应物,5分钟时达到平衡,测得容器内气体增加了0.4mol,用CO表示该反应时间内的反应速率为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】在一定条件下,将2 mol SO2(g)和1 mol O2(g)置于1L密闭容器中,发生反应:2SO2(g)+ O2(g) 2SO3 (g) ,经5min反应达到平衡,此时密闭容器中SO2还有1 mol,则:
2SO3 (g) ,经5min反应达到平衡,此时密闭容器中SO2还有1 mol,则:
(1)平衡时v(正)_______ v(逆)(填“<”、“=”或“>”);
(2)5min 内,用SO2表示该反应的平均速率为_________ mol· L—1·min—1。
(3)若减少SO2(g),则该化学反应的反应速率_______ (填“增大”、“减少”或“不变”)
 2SO3 (g) ,经5min反应达到平衡,此时密闭容器中SO2还有1 mol,则:
2SO3 (g) ,经5min反应达到平衡,此时密闭容器中SO2还有1 mol,则:(1)平衡时v(正)
(2)5min 内,用SO2表示该反应的平均速率为
(3)若减少SO2(g),则该化学反应的反应速率
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】CO2催化加氢制甲醇(CH3OH)是实现碳达峰、碳中和的途径之一,其反应可表示为 。
。
(1)该反应分两步进行,反应过程能量变化如图所示,所有物质均为气态。

总反应
___________ 。第①步反应的热化学方程式为___________ 。
(2)一定条件下,向体积为1L的恒容密闭容器中通入2molCO2和6molH2发生反应生成甲醇,每次反应10分钟,测得CO2转化率随温度变化关系如图所示。
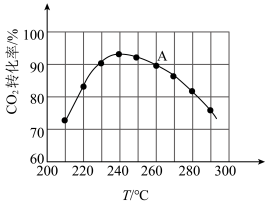
①CO2催化加氢制甲醇的平衡常数表达式K=___________ 。
②已知A点为平衡状态。260℃时从反应开始到恰好平衡CO2的平均反应速率v(CO2)=___________ 。该温度下的平衡常数
___________  。
。
③260℃时,某时刻反应混合物中CO2、H2、CH3OH、H2O的浓度分别为0.1mol/L、0.3mol/L、1mol/L、1mol/L,此时反应进行的方向为___________ (填“正反应方向”“逆反应方向”或“平衡状态”)。
(3)210℃~240℃时,CO2的转化率逐渐增大的原因是___________ 。
 。
。(1)该反应分两步进行,反应过程能量变化如图所示,所有物质均为气态。

总反应

(2)一定条件下,向体积为1L的恒容密闭容器中通入2molCO2和6molH2发生反应生成甲醇,每次反应10分钟,测得CO2转化率随温度变化关系如图所示。

①CO2催化加氢制甲醇的平衡常数表达式K=
②已知A点为平衡状态。260℃时从反应开始到恰好平衡CO2的平均反应速率v(CO2)=

 。
。③260℃时,某时刻反应混合物中CO2、H2、CH3OH、H2O的浓度分别为0.1mol/L、0.3mol/L、1mol/L、1mol/L,此时反应进行的方向为
(3)210℃~240℃时,CO2的转化率逐渐增大的原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】某温度时,在容积为2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化的曲线如图所示。

分析图中数据,回答下列问题:
(1)该反应的化学方程式为___________ 。
(2)X在0~2min间的平均反应速率为___________ 。

分析图中数据,回答下列问题:
(1)该反应的化学方程式为
(2)X在0~2min间的平均反应速率为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题
(1)在恒温条件下将一定量X和Y的混合气体通入容积为2L的密闭容器中,X和Y两物质的浓度随时间的变化情况如下图所示。

①该反应的化学方程式为(反应物或生成物用符号X、Y表示):_______ 。
②a、b、c、d四个点中,表示化学反应处于平衡状态的点是_______ 。
(2)如下图所示是可逆反应 的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是_______。
的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是_______。

(3)t℃时,将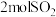 和
和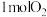 通入体积为2L的恒温恒容密闭容器中,发生如下反应:
通入体积为2L的恒温恒容密闭容器中,发生如下反应: ,
, 时反应达到平衡,此时测得反应物
时反应达到平衡,此时测得反应物 还剩余
还剩余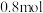 。从反应开始到化学平衡,生成
。从反应开始到化学平衡,生成 的平均反应速率为
的平均反应速率为_______ ;平衡时 的转化率为
的转化率为_______ 。若将物质的量之比为 的
的 和
和 混合气体通入一个恒温恒压的密闭容器中,反应达到平衡时,混合气体体积减少了20%。
混合气体通入一个恒温恒压的密闭容器中,反应达到平衡时,混合气体体积减少了20%。 的转化率为
的转化率为_______ 。
(1)在恒温条件下将一定量X和Y的混合气体通入容积为2L的密闭容器中,X和Y两物质的浓度随时间的变化情况如下图所示。

①该反应的化学方程式为(反应物或生成物用符号X、Y表示):
②a、b、c、d四个点中,表示化学反应处于平衡状态的点是
(2)如下图所示是可逆反应
 的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是_______。
的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是_______。
| A.t1时,只有正方向反应在进行 |
| B.t2时,反应达到最大限度 |
C. ,反应不再进行 ,反应不再进行 |
D. ,各物质的浓度不再发生变化 ,各物质的浓度不再发生变化 |
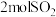 和
和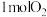 通入体积为2L的恒温恒容密闭容器中,发生如下反应:
通入体积为2L的恒温恒容密闭容器中,发生如下反应: ,
, 时反应达到平衡,此时测得反应物
时反应达到平衡,此时测得反应物 还剩余
还剩余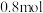 。从反应开始到化学平衡,生成
。从反应开始到化学平衡,生成 的平均反应速率为
的平均反应速率为 的转化率为
的转化率为 的
的 和
和 混合气体通入一个恒温恒压的密闭容器中,反应达到平衡时,混合气体体积减少了20%。
混合气体通入一个恒温恒压的密闭容器中,反应达到平衡时,混合气体体积减少了20%。 的转化率为
的转化率为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】以天然气为原料合成尿素的生产中,主要反应之一为
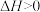 。请根据题目要求回答下列问题;
。请根据题目要求回答下列问题;
(1)在一定条件下,将0.05mol 和0.10mol
和0.10mol  放入容积为2L的密闭容器中,20s时有0.01mol CO生成,则
放入容积为2L的密闭容器中,20s时有0.01mol CO生成,则 的化学反应速率为
的化学反应速率为______ 。
(2)在其他条件不变的情况下降低温度,则逆反应速率______ (填“增大”“减小”或“不变”,下同);在其他条件不变的情况下升高温度,则正反应速率______ 。

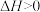 。请根据题目要求回答下列问题;
。请根据题目要求回答下列问题;(1)在一定条件下,将0.05mol
 和0.10mol
和0.10mol  放入容积为2L的密闭容器中,20s时有0.01mol CO生成,则
放入容积为2L的密闭容器中,20s时有0.01mol CO生成,则 的化学反应速率为
的化学反应速率为(2)在其他条件不变的情况下降低温度,则逆反应速率
您最近一年使用:0次



