下列判断正确的是
| A.因为共价键有饱和性和方向性,所以原子晶体不遵循“紧密堆积”原理 |
| B.稳定性按 HF、HCl、HBr、HI 逐渐减弱,根本原因是 F、Cl、Br、I 非金属性减弱 |
| C.晶体中一定存在化学键,金属晶体熔点一定很高 |
| D.固体 SiO2 一定是晶体 |
更新时间:2022-09-18 18:53:23
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】下列关于化合价的叙述:
①化合价是元素的一种性质,因此称为元素的化合价,而不应称为原子的化合价。
②化合物中化合价有正价和负价,其数值由元素的一个原子得失电子的数目或形成共用电子对的数目决定的。
③一种元素只有一种化合价。
④在化合物中非金属元素的化合价为负值。
其中正确的是
①化合价是元素的一种性质,因此称为元素的化合价,而不应称为原子的化合价。
②化合物中化合价有正价和负价,其数值由元素的一个原子得失电子的数目或形成共用电子对的数目决定的。
③一种元素只有一种化合价。
④在化合物中非金属元素的化合价为负值。
其中正确的是
| A.①② | B.①③ | C.②③④ | D.① |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】生活中的化学无处不在,下列关于生活中的化学描述错误的是
| A.电视和电脑的液晶显示器使用的液晶材料属于晶体,能体现晶体的各向异性 |
| B.在霓虹灯的灯管里存在等离子体 |
| C.可以用光谱分析的方法来确定太阳的组成元素是否含氦 |
| D.我国科学家近期成功构筑了一类超分子金属配位笼,超分子具有分子识别和自组装特征 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列有关碱金属元素、卤素结构和性质的描述正确的有
①卤素按F、Cl、Br、I的顺序,其非金属性逐渐减弱的主要原因是随着核电荷数增加,电子层数增多,原子半径增大
②F、Cl、Br、I的最外层电子数都是7,次外层电子数都是8
③碱金属单质的金属性很强,均易与氧气发生反应,加热时生成的氧化物为R2O
④根据同族元素性质的递变规律推测,At2与H2化合较难,砹化银也难溶于水
⑤根据Cl、Br、I的非金属性递减,可推出HCl、HBr、HI的酸性依次增强,而热稳定性依次减弱
⑥碱金属都应保存在煤油中
①卤素按F、Cl、Br、I的顺序,其非金属性逐渐减弱的主要原因是随着核电荷数增加,电子层数增多,原子半径增大
②F、Cl、Br、I的最外层电子数都是7,次外层电子数都是8
③碱金属单质的金属性很强,均易与氧气发生反应,加热时生成的氧化物为R2O
④根据同族元素性质的递变规律推测,At2与H2化合较难,砹化银也难溶于水
⑤根据Cl、Br、I的非金属性递减,可推出HCl、HBr、HI的酸性依次增强,而热稳定性依次减弱
⑥碱金属都应保存在煤油中
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列元素的最高价氧化物对应的水化物中碱性最强的是
| A.Ca | B.Li | C.Na | D.K |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】北斗导航系统上使用的原子钟是世界上最准确的原子钟——2000万年相差一秒,该原子钟上使用的核素是 ,已知铯是第ⅠA族元素,下列说法错误的是
,已知铯是第ⅠA族元素,下列说法错误的是
 ,已知铯是第ⅠA族元素,下列说法错误的是
,已知铯是第ⅠA族元素,下列说法错误的是A. 元素的相对原子质量为137 元素的相对原子质量为137 | B. 溶液能溶解 溶液能溶解 |
C. 与 与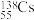 核外电子层结构相同 核外电子层结构相同 | D.酚酞遇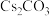 溶液变红色 溶液变红色 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】教材是教与学的依据,也是我们高三复习最重要的资料,下列有关说法不正确的是
| A.催化剂之所以能改变化学反应速率,是因为它能改变反应历程,改变反应的活化能 |
B. 是含极性键的弱极性分子,它在 是含极性键的弱极性分子,它在 中的溶解度高于在水中的溶解度 中的溶解度高于在水中的溶解度 |
| C.区别晶体和非晶体最可靠的科学方法是对固体进行X射线衍射实验 |
| D.中和热测定实验中,测量体系温度时一定要将NaOH溶液分步缓缓加入量热计的内筒,以确保酸碱充分反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列说法正确的是
| A.SiO2是由极性键构成的非极性分子 |
| B.酸性:三氟乙酸(CF3COOH)>乙酸(CH3COOH)>丙酸(CH3CH2COOH) |
| C.晶体的自范性,能使破损的晶体在固态时自动变成规则的多面体 |
| D.区分晶体和非晶体最可靠的科学方法是测定熔点 |
您最近一年使用:0次



