下列说法中正确的是
| A.非自发反应在任何条件下都不能实现 |
| B.ΔH>0,ΔS>0的反应在任何条件都可以实际发生 |
| C.金属单质导电属于物理变化,电解质溶液导电是化学变化 |
D.O2(g)+2SO2(g) 2SO3(g)在298K时的平衡常数K=7.0×1022,说明在该温度下反应速率很快 2SO3(g)在298K时的平衡常数K=7.0×1022,说明在该温度下反应速率很快 |
更新时间:2022-09-25 13:43:19
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法中不正确的有
①将硫酸钡放入水中不能导电,所以硫酸钡是非电解质;
②氨溶于水得到的溶液能导电,所以NH3是电解质;
③液态HCl不导电,所以属于非电解质;
④NaHSO4电离时生成的阳离子有氢离子,但不属于酸;
⑤电解质放在水中一定能导电,非电解质放在水中一定不导电。
⑥强电解质的导电能力比弱电解质强
①将硫酸钡放入水中不能导电,所以硫酸钡是非电解质;
②氨溶于水得到的溶液能导电,所以NH3是电解质;
③液态HCl不导电,所以属于非电解质;
④NaHSO4电离时生成的阳离子有氢离子,但不属于酸;
⑤电解质放在水中一定能导电,非电解质放在水中一定不导电。
⑥强电解质的导电能力比弱电解质强
| A.4个 | B.5个 | C.6个 | D.全部 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在两份相同的 溶液中,分别滴入相同浓度的
溶液中,分别滴入相同浓度的 、
、 溶液(相同体积内所含
溶液(相同体积内所含 、
、 的数目相同),其导电能力随滴入溶液的体积变化曲线如图所示。下列说法不正确的是
的数目相同),其导电能力随滴入溶液的体积变化曲线如图所示。下列说法不正确的是

 溶液中,分别滴入相同浓度的
溶液中,分别滴入相同浓度的 、
、 溶液(相同体积内所含
溶液(相同体积内所含 、
、 的数目相同),其导电能力随滴入溶液的体积变化曲线如图所示。下列说法不正确的是
的数目相同),其导电能力随滴入溶液的体积变化曲线如图所示。下列说法不正确的是
A.②代表滴加 溶液的变化曲线 溶液的变化曲线 |
B.b点前发生的离子反应为: |
| C.a、b两点溶液均呈中性 |
D.c点对应的溶液中可大量存在的离子: 、 、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】向一定体积的Ba(OH)2溶液中逐滴加入H2SO4溶液,测得混合溶液的导电能力随时间的变化曲线如图所示。下列说法正确的是
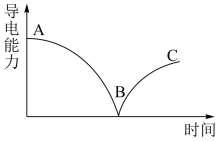

| A.AB段溶液的导电能力不断减弱,说明产物BaSO4是非电解质 |
B.AB段反应的离子方程式为Ba2++2OH-+2H++ =BaSO4↓+2H2O =BaSO4↓+2H2O |
| C.BC段溶液的导电能力不断增强,说明过量的Ba(OH)2发生电离 |
D.BC段溶液中,Al3+、Na+、 不能大量共存 不能大量共存 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
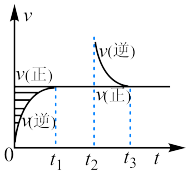
【推荐1】某恒温密闭容器发生可逆反应Z(?)+W(?) X(g)+Y(?),t1时刻达到平衡,t2时刻缩小容器体积,t3时刻再次达到平衡后未再改变条件,如图所示。下列说法正确的是
X(g)+Y(?),t1时刻达到平衡,t2时刻缩小容器体积,t3时刻再次达到平衡后未再改变条件,如图所示。下列说法正确的是
 X(g)+Y(?),t1时刻达到平衡,t2时刻缩小容器体积,t3时刻再次达到平衡后未再改变条件,如图所示。下列说法正确的是
X(g)+Y(?),t1时刻达到平衡,t2时刻缩小容器体积,t3时刻再次达到平衡后未再改变条件,如图所示。下列说法正确的是
| A.Z和W在该条件下至少有一种为气态 |
| B.t1~ t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等 |
| C.若在该温度下此反应平衡常数表达式为K=c(X),则t1~ t2时间段与t3时刻后的X浓度不相等 |
| D.若该反应只在某温度T以上自发进行,则该反应的平衡常数K随温度升高而增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】对于气相反应,用某组分(B)的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数(记作Kp)。已知反应CH4(g)+2H2O(g) CO2(g)+4H2(g),在t℃时的平衡常数Kp=a,则下列说法正确的是( )
CO2(g)+4H2(g),在t℃时的平衡常数Kp=a,则下列说法正确的是( )
 CO2(g)+4H2(g),在t℃时的平衡常数Kp=a,则下列说法正确的是( )
CO2(g)+4H2(g),在t℃时的平衡常数Kp=a,则下列说法正确的是( )A.Kp= |
| B.升高温度,若Kp增大,则该反应为放热反应 |
| C.该反应达到平衡状态后,增大压强,平衡向左移动,Kp不变 |
D.t℃时,反应 CH4(g)+H2O(g) CH4(g)+H2O(g)  CO2(g)+2H2(g)的平衡常数Kp= CO2(g)+2H2(g)的平衡常数Kp= a a |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】2022年6月5日,我国长征二号运载火箭搭载神舟十四号载人飞船顺利升空,其动力燃料是偏二甲肼,火箭发射时只要将其和四氧化二氮在发动机燃烧室混合即可,核心反应为: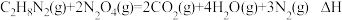 。对于该反应下列说法不正确的是
。对于该反应下列说法不正确的是
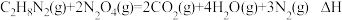 。对于该反应下列说法不正确的是
。对于该反应下列说法不正确的是A.用 表示键能之和,该反应 表示键能之和,该反应 (反应物) (反应物) (生成物) (生成物) |
B.由该热化学反应方程式可知,偏二甲肼的燃烧热为 |
| C.该反应物的总能量大于生成物总能量 |
D.该反应的 , , ,反应在任意条件下均能自发进行 ,反应在任意条件下均能自发进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关反应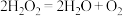 的说法中
的说法中不正确 的是
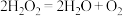 的说法中
的说法中A.生成标准状况下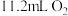 转移 转移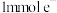 |
B. 溶液能催化该反应 溶液能催化该反应 |
C.该反应的熵变 |
| D.该反应在任意温度下均能自发进行 |
您最近一年使用:0次
【推荐1】我国科研人员在新型纳米催化剂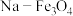 和
和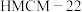 的表面将
的表面将 转化为烷烃,其过程如图所示:
转化为烷烃,其过程如图所示:

图中 转化为
转化为 的反应①为
的反应①为
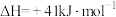
已知反应②: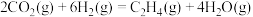
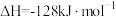
下列说法错误的是
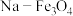 和
和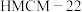 的表面将
的表面将 转化为烷烃,其过程如图所示:
转化为烷烃,其过程如图所示:
图中
 转化为
转化为 的反应①为
的反应①为
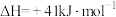
已知反应②:
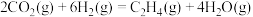
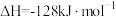
下列说法错误的是
| A.反应②在较低温度下能自发进行 |
B. 、 、 和 和 键能分别为 键能分别为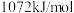 、 、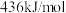 和 和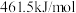 ,则 ,则 键键能为 键键能为 |
C.催化剂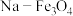 和 和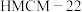 的使用降低了反应的活化能,也改变了反应的 的使用降低了反应的活化能,也改变了反应的 |
D.由反应①②可推知 转化为 转化为 的热化学方程式为 的热化学方程式为 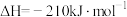 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】利用CH4消除NO2污染,反应原理为CH4(g)+2NO2(g) N2(g)+CO(g)+2H2O(g)。在1 L密闭容器中,分别加入0.50 mol CH4和1.20 mol NO2,测得控制不同温度,n(CH4)(单位:mol)随时间变化的有关实验数据如表所示,下列说法正确的是
N2(g)+CO(g)+2H2O(g)。在1 L密闭容器中,分别加入0.50 mol CH4和1.20 mol NO2,测得控制不同温度,n(CH4)(单位:mol)随时间变化的有关实验数据如表所示,下列说法正确的是
 N2(g)+CO(g)+2H2O(g)。在1 L密闭容器中,分别加入0.50 mol CH4和1.20 mol NO2,测得控制不同温度,n(CH4)(单位:mol)随时间变化的有关实验数据如表所示,下列说法正确的是
N2(g)+CO(g)+2H2O(g)。在1 L密闭容器中,分别加入0.50 mol CH4和1.20 mol NO2,测得控制不同温度,n(CH4)(单位:mol)随时间变化的有关实验数据如表所示,下列说法正确的是| 组别 | 温度/K | 时间/min物质的量/mol | 0 | 10 | 20 | 40 | 50 |
| ① | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| ② | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | M | 0.15 |
| A.T1温度下,该反应进行40 min时,2v正(NO2)=v逆(CO) |
| B.T1温度下,前20 min内NO2的降解速率为0.0125 mol/(L·min) |
| C.T2温度下,若容器内气体平均摩尔质量不变则处于平衡状态 |
| D.该反应在高温下才能自发进行 |
您最近一年使用:0次

 CO2(g)+2H2O(l) △H<0。在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述正确的是
CO2(g)+2H2O(l) △H<0。在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述正确的是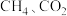 和
和 转化为
转化为 催化反应的研究,反应历程分别如甲、乙两图所示。
催化反应的研究,反应历程分别如甲、乙两图所示。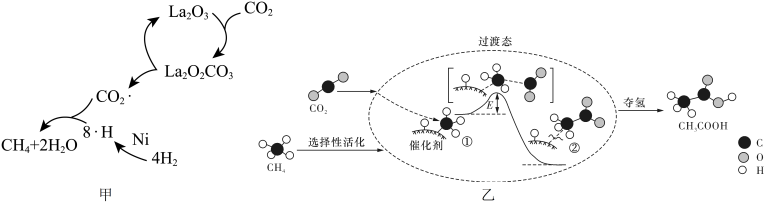
 经过Ni活性中心裂解产生活化态H·的过程中
经过Ni活性中心裂解产生活化态H·的过程中
 作催化剂可以降低反应的焓变,从而提高化学反应速率
作催化剂可以降低反应的焓变,从而提高化学反应速率 过程中,有C—H键发生断裂,①→②放出热量并形成了C—C键
过程中,有C—H键发生断裂,①→②放出热量并形成了C—C键 2CO2+N2△H
2CO2+N2△H

