完成下列填空:
(1)1.204×1024个氯气分子的物质的量是_______ ,0.5mol的 中含有的电子数为
中含有的电子数为_______ 。
(2)同温同压下,同体积的甲烷(CH4)和CO2物质的量之比为_______ ,密度之比为_______ 。
(3)3.1gNa2X含有Na+0.1mol,则Na2X的摩尔质量为_______ ,X的相对原子质量为_______ 。
(4)在标准状况下,CO和CO2的混合气体共6.72L,质量为12g,则混合气体的平均摩尔质量为_______ 。
(1)1.204×1024个氯气分子的物质的量是
 中含有的电子数为
中含有的电子数为(2)同温同压下,同体积的甲烷(CH4)和CO2物质的量之比为
(3)3.1gNa2X含有Na+0.1mol,则Na2X的摩尔质量为
(4)在标准状况下,CO和CO2的混合气体共6.72L,质量为12g,则混合气体的平均摩尔质量为
更新时间:2022-10-10 20:34:17
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)在标准状况下,1.7g氨气所占的体积为__________ L,它与标准状况下__________ L硫化氢含有相同数目的氢原子。
(2)某气态氧化物的化学式为 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为__________ ,R的相对原子质量为__________ 。
(3)已知CO、 混合气体的质量为16.0g,标准状况下体积为8.96L,则可推知该混合气体中含CO
混合气体的质量为16.0g,标准状况下体积为8.96L,则可推知该混合气体中含CO__________ g,所含 在标准状况下的体积为
在标准状况下的体积为__________ L。
(4)同温同压下, 与氦气的密度之比为
与氦气的密度之比为________ ;若质量相同,两种气体的体积之比为______ 。
(2)某气态氧化物的化学式为
 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为(3)已知CO、
 混合气体的质量为16.0g,标准状况下体积为8.96L,则可推知该混合气体中含CO
混合气体的质量为16.0g,标准状况下体积为8.96L,则可推知该混合气体中含CO 在标准状况下的体积为
在标准状况下的体积为(4)同温同压下,
 与氦气的密度之比为
与氦气的密度之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】有机物A和B都含C:40%,H:6.7%,O:53.3%,在标准状况下,A蒸气密度为1.34克/升,B的相对分子量为60,A易溶于水,其水溶液能发生银镜反应。B溶液显酸性。试写出A、B的结构简式及名称。_________________ (要求计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】I.现有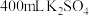 和
和 的混合溶液,将其分为两等份,向其中一份中加入
的混合溶液,将其分为两等份,向其中一份中加入 溶液,至恰好不再产生沉淀,消耗
溶液,至恰好不再产生沉淀,消耗 ,将沉淀过滤、洗涤、干燥,称其质量为
,将沉淀过滤、洗涤、干燥,称其质量为 ;向另一份溶液中加入铁片,充分反应后,取出铁片,洗涤、烘干,称其质量比原来减轻了
;向另一份溶液中加入铁片,充分反应后,取出铁片,洗涤、烘干,称其质量比原来减轻了 。试计算:
。试计算:
(1)
_______ 。
(2)则原溶液中 的物质的量浓度为
的物质的量浓度为_______ 
II.某化工厂以某种黄铁矿(含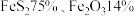 、不反应杂质
、不反应杂质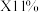 )为原料生产硫酸。黄铁矿与氧气反应的方程式为
)为原料生产硫酸。黄铁矿与氧气反应的方程式为 。若该厂每天煅烧这种矿石100吨,煅烧后得到固体75吨。试计算:
。若该厂每天煅烧这种矿石100吨,煅烧后得到固体75吨。试计算:
(1)假设生产过程中硫的损失为零,理论上每天可以制得98%的浓硫酸_______ 吨。
(2)假设煅烧后得到的固体只含有 和不反应杂质X,若用来炼铁,理论上每天能得到含碳4%的生铁
和不反应杂质X,若用来炼铁,理论上每天能得到含碳4%的生铁_______ 吨。(写出计算过程)
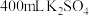 和
和 的混合溶液,将其分为两等份,向其中一份中加入
的混合溶液,将其分为两等份,向其中一份中加入 溶液,至恰好不再产生沉淀,消耗
溶液,至恰好不再产生沉淀,消耗 ,将沉淀过滤、洗涤、干燥,称其质量为
,将沉淀过滤、洗涤、干燥,称其质量为 ;向另一份溶液中加入铁片,充分反应后,取出铁片,洗涤、烘干,称其质量比原来减轻了
;向另一份溶液中加入铁片,充分反应后,取出铁片,洗涤、烘干,称其质量比原来减轻了 。试计算:
。试计算:(1)

(2)则原溶液中
 的物质的量浓度为
的物质的量浓度为
II.某化工厂以某种黄铁矿(含
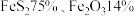 、不反应杂质
、不反应杂质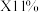 )为原料生产硫酸。黄铁矿与氧气反应的方程式为
)为原料生产硫酸。黄铁矿与氧气反应的方程式为 。若该厂每天煅烧这种矿石100吨,煅烧后得到固体75吨。试计算:
。若该厂每天煅烧这种矿石100吨,煅烧后得到固体75吨。试计算:(1)假设生产过程中硫的损失为零,理论上每天可以制得98%的浓硫酸
(2)假设煅烧后得到的固体只含有
 和不反应杂质X,若用来炼铁,理论上每天能得到含碳4%的生铁
和不反应杂质X,若用来炼铁,理论上每天能得到含碳4%的生铁
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】火法炼铜的一种方法是用 与氧气在高温条件下反应生成铜与
与氧气在高温条件下反应生成铜与 。欲用该方法生产
。欲用该方法生产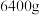 铜单质,请计算同时产生的
铜单质,请计算同时产生的 的体积(标准状况下)
的体积(标准状况下)___________ 。
 与氧气在高温条件下反应生成铜与
与氧气在高温条件下反应生成铜与 。欲用该方法生产
。欲用该方法生产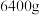 铜单质,请计算同时产生的
铜单质,请计算同时产生的 的体积(标准状况下)
的体积(标准状况下)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】(1)0.3molNH3分子中所含氢原子数与___ 个H2O分子中所含氢原子数相等。
(2)含0.4molFe3+的Fe2(SO4)3中所含的SO42-的物质的量是___ 。
(3)已知16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为____ 。
(4)2.3gNa中含___ mole-,在反应中生成Na+共失去___ mole-。
(5)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是(设NA为阿伏加 德罗常数)____ 。
(2)含0.4molFe3+的Fe2(SO4)3中所含的SO42-的物质的量是
(3)已知16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为
(4)2.3gNa中含
(5)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是(设NA为阿伏加 德罗常数)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】填空。
(1)标准状况下11.2LH2S气体的质量为_______ ;
(2)已知3.01×1023个X气体分子的质量为8g,则X气体的摩尔质量是_______ ;
(3)与0.1molOH-含有相同电子数的NH3在标准状况下的体积为_______ ;
(4)同质量的NH3和H2S中氢原子的个数比为_______ 。
(1)标准状况下11.2LH2S气体的质量为
(2)已知3.01×1023个X气体分子的质量为8g,则X气体的摩尔质量是
(3)与0.1molOH-含有相同电子数的NH3在标准状况下的体积为
(4)同质量的NH3和H2S中氢原子的个数比为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】16gSO2的物质的量为____ ,所含分子个数为_____ ,在标准状况下所占的体积约为_____ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)2 mol CO(NH2)2中含________ mol H,所含氧原子跟________ mol H2O所含氧原子个数相等。
(2) 2 mol O3和3 mol O2的质量之比为________ ,同温同压下的密度之比为________ ,含氧原子数之比为________ 。
(3)在9.5 g某二价金属的氯化物中含有0.2 mol Cl-,此氯化物的摩尔质量为__________ ,该金属元素的相对原子质量为____________ 。
(4)6.72 L CO(标准状况)与一定量的Fe2O3恰好完全反应(生成Fe与CO2)后,生成Fe的质量为________ g。
(1)2 mol CO(NH2)2中含
(2) 2 mol O3和3 mol O2的质量之比为
(3)在9.5 g某二价金属的氯化物中含有0.2 mol Cl-,此氯化物的摩尔质量为
(4)6.72 L CO(标准状况)与一定量的Fe2O3恰好完全反应(生成Fe与CO2)后,生成Fe的质量为
您最近一年使用:0次



