中国的能源特点是“多煤、少油、缺气”,因此“煤制合成天然气(SNG)”合成技术对我国资源合理利用、节能减排具有重要意义。
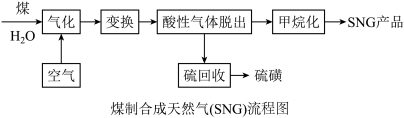
(1)煤主要由碳、氢、氧、硫等元素组成,下列碳及其化合物的性质与用途具有对应关系的是_______
(2)煤、石油、天然气均属于化石燃料,是不可再生资源。下列关于化石燃料的说法不正确 的是_______
(3)已知:几种物质的标准燃烧热如下表所示
①写出能表示 标准燃烧热的热化学方程式:
标准燃烧热的热化学方程式:_______ 。
②燃烧等质量的上述几种物质,放出热量最多得是_______ 。
③气化过程中,需向炭层交替喷入空气和水蒸气,请从能量利用的角度分析喷入空气的目的是_______ 。
(4)一种“酸性气体脱出”并回收硫的技术如下:
第一步,用 溶液吸收
溶液吸收 ;
;
第二步,在 时,用
时,用 溶液氧化NaHS回收单质硫,同时产生
溶液氧化NaHS回收单质硫,同时产生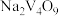 。
。
①第二步发生的反应离子方程式为_______ 。
②脱出 速度主要取决于第二步反应的速率,则反应速率:
速度主要取决于第二步反应的速率,则反应速率: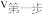
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。

(1)煤主要由碳、氢、氧、硫等元素组成,下列碳及其化合物的性质与用途具有对应关系的是_______
| A.炭能燃烧,可用作除味剂 | B.CO具有还原性,可用于铁的冶炼 |
C. 易溶于水,可用于去除油污 易溶于水,可用于去除油污 | D. 能与碱反应,可用于烘焙糕点 能与碱反应,可用于烘焙糕点 |
| A.甲烷是天然气的主要成分,它是一种高效而洁净的燃料 |
| B.石油的分馏是化学变化 |
| C.石油通过催化裂化过程可获得汽油、煤油等轻质油 |
| D.煤的气化是把煤转化为可燃性气体的过程,该过程属于化学变化 |
 |  |  | |
标准燃烧热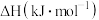 | -393.5 | -283 | -285.8 |
①写出能表示
 标准燃烧热的热化学方程式:
标准燃烧热的热化学方程式:②燃烧等质量的上述几种物质,放出热量最多得是
③气化过程中,需向炭层交替喷入空气和水蒸气,请从能量利用的角度分析喷入空气的目的是
(4)一种“酸性气体脱出”并回收硫的技术如下:
第一步,用
 溶液吸收
溶液吸收 ;
;第二步,在
 时,用
时,用 溶液氧化NaHS回收单质硫,同时产生
溶液氧化NaHS回收单质硫,同时产生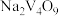 。
。①第二步发生的反应离子方程式为
②脱出
 速度主要取决于第二步反应的速率,则反应速率:
速度主要取决于第二步反应的速率,则反应速率: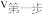
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
更新时间:2022-10-01 21:42:04
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)丙烷(C3H8)热值较高,污染较小,是一种优良的气态燃料。如图是一定量丙烷完全燃烧生成CO2和1molH2O(l)过程中的能量变化图,写出表示丙烷燃烧热的热化学方程式:___ 。

(2)已知:C(s,石墨)+O2(g)=CO2(g) △H1=-393kJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H2=-572kJ·mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H3=-2598kJ·mol-1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1molC2H2(g)反应的焓变:△H=__ 。
(3)已知25℃、101kpa时,一些物质的燃烧热为:
完成CO和H2生成CH3OH的热化学方程式__ 。
(4)已知3.6g碳在6.4g的氧气中燃烧,至反应物耗尽,放出xkJ热量。已知单质碳的燃烧热为ykJ/mol,则1molC与O2反应生成CO的反应热△H为__ kJ•mol-1。
(1)丙烷(C3H8)热值较高,污染较小,是一种优良的气态燃料。如图是一定量丙烷完全燃烧生成CO2和1molH2O(l)过程中的能量变化图,写出表示丙烷燃烧热的热化学方程式:

(2)已知:C(s,石墨)+O2(g)=CO2(g) △H1=-393kJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H2=-572kJ·mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H3=-2598kJ·mol-1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1molC2H2(g)反应的焓变:△H=
(3)已知25℃、101kpa时,一些物质的燃烧热为:
| 化学式 | CO(g) | H2(g) | CH3OH(l) |
| △H/(kJ/mol) | -283.0 | -285.8 | -726.5 |
完成CO和H2生成CH3OH的热化学方程式
(4)已知3.6g碳在6.4g的氧气中燃烧,至反应物耗尽,放出xkJ热量。已知单质碳的燃烧热为ykJ/mol,则1molC与O2反应生成CO的反应热△H为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】写出下列反应的热化学方程式。
(1)1mol葡萄糖晶体在氧气中完全氧化生成二氧化碳气体和液态水时放出 热量:
热量:_______ 。
(2)32 g铜粉在足量氧气中反应生成氧化铜固体时放出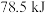 热量:
热量:_____ 。
(3)标准状况下,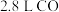 气体在氧气中完全燃烧生成二氧化碳气体时放出
气体在氧气中完全燃烧生成二氧化碳气体时放出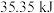 热量:
热量:_______ 。
(4)一氧化碳气体还原赤铁矿得到1 mol单质铁时放出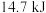 热量:
热量:_______ 。
(5)写出稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式_______ 。
(1)1mol葡萄糖晶体在氧气中完全氧化生成二氧化碳气体和液态水时放出
 热量:
热量:(2)32 g铜粉在足量氧气中反应生成氧化铜固体时放出
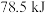 热量:
热量:(3)标准状况下,
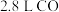 气体在氧气中完全燃烧生成二氧化碳气体时放出
气体在氧气中完全燃烧生成二氧化碳气体时放出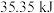 热量:
热量:(4)一氧化碳气体还原赤铁矿得到1 mol单质铁时放出
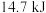 热量:
热量:(5)写出稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式
您最近一年使用:0次
【推荐1】氢元素单质及其化合物是人类赖以生活的重要能源。盖斯定律认为:不管化学过程是一步完成或分多步完成,整个过程的总热效应相同。试运用盖斯定律回答下列问题:
(1)反应A+B→C(△H<0)分两步进行:(i)A+B→X(△H>0);(ii)X→C(△H<0)。下列示意图中,能正确表示总反应过程中能量变化的是_______ (填字母)。

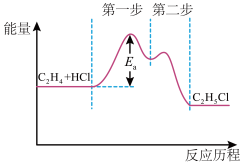
(2)①乙烯与HCl气体催化加成反应的能量与反应历程的关系如图所示,下列说法正确的是_______ 。
A.第二步反应比第一步的快 B.第一步的逆反应活化能比第二步的小
C.两步反应的 均小于0 D.增大压强可以使该反应的
均小于0 D.增大压强可以使该反应的 增大
增大
②乙烯与HCl生成C2H5Cl的总反应是_______ 反应(填“放热”或“吸热”)。
(3)已知:H2O(g)=H2O(l) △H1=-Q1kJ·mol-1
C2H5OH(g)=C2H5OH(1) △H2=-Q2kJ·mol-1
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) △H3=-Q3kJ·mol-1
则C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)的△H=_______ kJ·mol-1;若将23g液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为_______ 。
(1)反应A+B→C(△H<0)分两步进行:(i)A+B→X(△H>0);(ii)X→C(△H<0)。下列示意图中,能正确表示总反应过程中能量变化的是

(2)①乙烯与HCl气体催化加成反应的能量与反应历程的关系如图所示,下列说法正确的是

A.第二步反应比第一步的快 B.第一步的逆反应活化能比第二步的小
C.两步反应的
 均小于0 D.增大压强可以使该反应的
均小于0 D.增大压强可以使该反应的 增大
增大②乙烯与HCl生成C2H5Cl的总反应是
(3)已知:H2O(g)=H2O(l) △H1=-Q1kJ·mol-1
C2H5OH(g)=C2H5OH(1) △H2=-Q2kJ·mol-1
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) △H3=-Q3kJ·mol-1
则C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)的△H=
您最近一年使用:0次
【推荐2】回答下列问题
(1)二氟卡宾(:CF2)作为一种活性中间体,一直受到有机氟化学研究工作者的高度关注。硫单质与二氟卡宾可以形成S=CF2,反应历程如图所示:
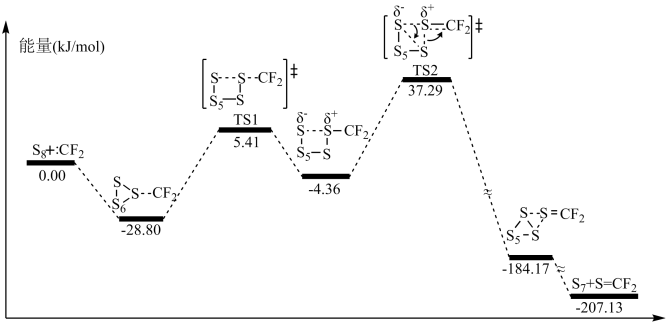
①由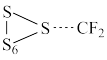 生成
生成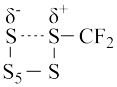 的活化能为
的活化能为__________________ ;
②决定反应速率的基元反应的活化能为______________________ 。
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g) 2NH3(g)反应的影响。实验结果如图所示:(图中T表示温度,n表示物质的量)
2NH3(g)反应的影响。实验结果如图所示:(图中T表示温度,n表示物质的量)
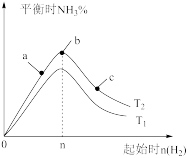
①图象中T2和T1的关系是:T2___________ T1(填“高于”、“低于”、 “等于”或“无法确定”)。
②比较在a、b、c三点所处的平衡状态中,反应物N 2的转化率最高的是_______________ (填字母)。
③在起始体系中n(N2):n(H2)= 1:3时,反应后氨的百分含量最大;若容器容积为1 L, n=3 mol反应达到平衡时H2的转化率为60%,则此条件下(T2),反应的平衡常数K=__________________ 。
(1)二氟卡宾(:CF2)作为一种活性中间体,一直受到有机氟化学研究工作者的高度关注。硫单质与二氟卡宾可以形成S=CF2,反应历程如图所示:

①由
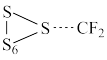 生成
生成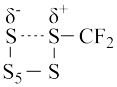 的活化能为
的活化能为②决定反应速率的基元反应的活化能为
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g)
 2NH3(g)反应的影响。实验结果如图所示:(图中T表示温度,n表示物质的量)
2NH3(g)反应的影响。实验结果如图所示:(图中T表示温度,n表示物质的量) 
①图象中T2和T1的关系是:T2
②比较在a、b、c三点所处的平衡状态中,反应物N 2的转化率最高的是
③在起始体系中n(N2):n(H2)= 1:3时,反应后氨的百分含量最大;若容器容积为1 L, n=3 mol反应达到平衡时H2的转化率为60%,则此条件下(T2),反应的平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】反应速率v和反应物浓度的关系是用实验方法测定的。化学反应 包含下列两步:①
包含下列两步:① (慢)、②
(慢)、②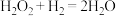 (快),第一步反应的速率表达式为
(快),第一步反应的速率表达式为 ,式中k为常数,m、n值可用下表中数据确定。T℃时测得有关实验数据如下:
,式中k为常数,m、n值可用下表中数据确定。T℃时测得有关实验数据如下:
(1)m=___________ ,n=___________
(2)分步反应的活化能①___________ ②(填“>”“<”或“=”)
(3)相同条件下,浓度对反应速率的影响H2___________ NO(填“>”“<”或“=”)
 包含下列两步:①
包含下列两步:① (慢)、②
(慢)、②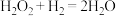 (快),第一步反应的速率表达式为
(快),第一步反应的速率表达式为 ,式中k为常数,m、n值可用下表中数据确定。T℃时测得有关实验数据如下:
,式中k为常数,m、n值可用下表中数据确定。T℃时测得有关实验数据如下:| 序号 | c(NO)/(mol/L) | c(H2)/(mol/L) | 速率/(mol/(L·min)) |
| Ⅰ | 0.0060 | 0.0010 | 1.8×10-4 |
| Ⅱ | 0.0060 | 0.0020 | 3.6×10-4 |
| Ⅲ | 0.0010 | 0.0060 | 3.0×10-5 |
| Ⅳ | 0.0020 | 0.0060 | 1.2×10-4 |
(2)分步反应的活化能①
(3)相同条件下,浓度对反应速率的影响H2
您最近一年使用:0次
【推荐1】现有直馏汽油和裂化汽油各一瓶。已知:裂化汽油主要成分为烷烃、烯烃,直馏汽油主要成分为烷烃、环烷烃、芳香烃。
(1)请从下列试剂中选择最合理的试剂区别上述两种汽油。所选试剂是_______ (填字母)。
A.酸性 溶液 B.乙醇 C.溴水
溶液 B.乙醇 C.溴水
(2)加入所选试剂后,直馏汽油中观察到的现象是_______ ;裂化汽油中观察到的现象是_______ 。
(1)请从下列试剂中选择最合理的试剂区别上述两种汽油。所选试剂是
A.酸性
 溶液 B.乙醇 C.溴水
溶液 B.乙醇 C.溴水(2)加入所选试剂后,直馏汽油中观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】乙烯是一种重要的石油化工原料,以乙烯为原料在不同条件下可合成下列物质。
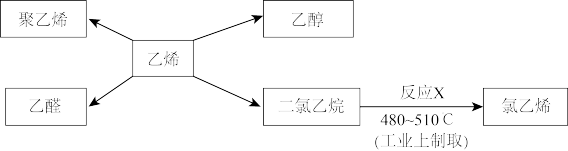
完成下列填空。
(1)工业上从石油制取乙烯的方法是_______(填编号)
(2)下列关于聚乙烯的说法正确的是_______(填编号)
(3)写出乙烯制乙醇的化学方程式:_______ 。
(4)写出反应X的化学方程式:_______ ,该反应类型为_______ 。
(5)若乙烯分子中两个氢原子被氯原子取代,写出所有可能的同分异构体(包括立体异构体)_______

完成下列填空。
(1)工业上从石油制取乙烯的方法是_______(填编号)
| A.干馏 | B.分馏 | C.裂化 | D.裂解 |
| A.聚乙烯是混合物 | B.聚乙烯与乙烯互为同系物 |
| C.聚乙烯中含有碳碳双键 | D.聚乙烯不可用作食品塑料袋 |
(4)写出反应X的化学方程式:
(5)若乙烯分子中两个氢原子被氯原子取代,写出所有可能的同分异构体(包括立体异构体)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】填空
(1)煤的气化——用来制取___________
①定义:___________
②反应方程式:___________
(2)煤的液化
①定义:___________
②反应方程式:___________
(3)煤的干馏
①定义:___________
②主要产物:___________
【科学史话】苯的发现之旅
(4)1825年,英国科学家法拉第在煤气灯中首先发现苯,并测得其含碳量,确定其最简式为CH;1834年,德国科学家米希尔里希制得苯,并将其命名为苯;之后,法国化学家日拉尔等确定其分子量为78,苯分子式为___________ 。
(1)煤的气化——用来制取
①定义:
②反应方程式:
(2)煤的液化
①定义:
②反应方程式:
(3)煤的干馏
①定义:
②主要产物:
【科学史话】苯的发现之旅
(4)1825年,英国科学家法拉第在煤气灯中首先发现苯,并测得其含碳量,确定其最简式为CH;1834年,德国科学家米希尔里希制得苯,并将其命名为苯;之后,法国化学家日拉尔等确定其分子量为78,苯分子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】城市使用的燃料,现大多用煤气、液化石油气。煤气的主要成分是一氧化碳和氢气的混合气,它由煤炭与水(蒸气)反应制得,故又称水煤气。
(1)试写出制取水煤气的主要化学方程式___________________ 。
(2)液化石油气的主要成分是丙烷,丙烷燃烧的热化学方程式为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-2 220.0 kJ•mol−1。已知CO气体燃烧的热化学方程式为:CO(g)+1/2O2(g)=CO2(g) ΔH=-283.0 kJ•mol−1。试比较相同物质的量的C3H8和CO燃烧,产生的热量比值约为_________ 。
(3)已知氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ•mol−1。试比较同质量的氢气和丙烷燃烧,产生的热量比值约为______ 。
(4)氢气是未来的能源,除产生的热量大之外,还具有的优点是___________________ 。
(1)试写出制取水煤气的主要化学方程式
(2)液化石油气的主要成分是丙烷,丙烷燃烧的热化学方程式为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-2 220.0 kJ•mol−1。已知CO气体燃烧的热化学方程式为:CO(g)+1/2O2(g)=CO2(g) ΔH=-283.0 kJ•mol−1。试比较相同物质的量的C3H8和CO燃烧,产生的热量比值约为
(3)已知氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ•mol−1。试比较同质量的氢气和丙烷燃烧,产生的热量比值约为
(4)氢气是未来的能源,除产生的热量大之外,还具有的优点是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】能源是经济增长与社会发展的重要物质基础,美国马奇蒂博士对世界一次能源替代趋势曾作如下预测:

回答下列问题:
(1)上图化石能源中属于较清洁的能源是_________ 。
(2)核电厂的燃料一般由0.71%235U、99.28%238U及0.0058%234U组成
①235U、238U、234U三种核素之间的关系是______________ 。
②235g核素 发生裂变反应:
发生裂变反应:  ,净产生的中子
,净产生的中子 数为
数为_______ 。
(3)下图是氢能的制备及利用的途径之一,涉及能量转化方式有___________ 。(填代号)

a光能→化学能 b电能→化学能 c化学能→电能
(4)目前实现煤的综合利用的主要途径是煤的干馏、煤的气化和液化。
①煤的干馏属于变化______________ 。(填物理或化学)
②煤的气化过程发生的主要反应是____________ 。
(5)可燃冰属于新能源,我国是全球第一个成功稳定开采可燃冰的国家。某种可燃冰(甲烷水合物)晶体中,平均每46个水分子构成8个分子笼,每个分子笼可容纳1个甲烷分子或水分子,若这8个分子笼中有6个容纳的是甲烷分子,另外2个被水分子填充,则这种可燃冰的平均组成可表示为____________ 。

回答下列问题:
(1)上图化石能源中属于较清洁的能源是
(2)核电厂的燃料一般由0.71%235U、99.28%238U及0.0058%234U组成
①235U、238U、234U三种核素之间的关系是
②235g核素
 发生裂变反应:
发生裂变反应:  ,净产生的中子
,净产生的中子 数为
数为(3)下图是氢能的制备及利用的途径之一,涉及能量转化方式有

a光能→化学能 b电能→化学能 c化学能→电能
(4)目前实现煤的综合利用的主要途径是煤的干馏、煤的气化和液化。
①煤的干馏属于变化
②煤的气化过程发生的主要反应是
(5)可燃冰属于新能源,我国是全球第一个成功稳定开采可燃冰的国家。某种可燃冰(甲烷水合物)晶体中,平均每46个水分子构成8个分子笼,每个分子笼可容纳1个甲烷分子或水分子,若这8个分子笼中有6个容纳的是甲烷分子,另外2个被水分子填充,则这种可燃冰的平均组成可表示为
您最近一年使用:0次




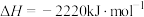
 的燃烧热为
的燃烧热为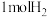 和
和 组成的混合气体完全燃烧释放的热量为
组成的混合气体完全燃烧释放的热量为
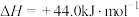 ,试写出丙烷燃烧生成
,试写出丙烷燃烧生成 和水蒸气时的热化学方程式:
和水蒸气时的热化学方程式:

