化学变化过程中均存在物质变化与能量变化,某化学兴趣小组进行如图所示实验,以验证此结论。
(1)进行实验时,温度计中水银液面变化:②_______ (填“升高”或“降低”)。
(2)下列化学反应中的能量变化关系与③相符合的是_______(填序号)。
(3)将①中涉及的反应设计成如图所示的原电池。电极材料X不能是_______(填序号)。
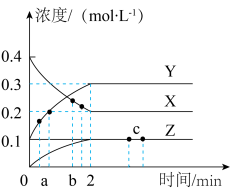
(4)在300℃时,X、Y、Z三种气体在恒容密闭容器中反应时的浓度变化如图所示:_______ ,0~2min内的反应速率V(X)=_______ 。
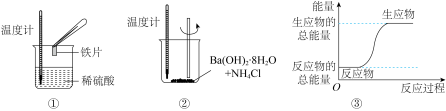
(1)进行实验时,温度计中水银液面变化:②
(2)下列化学反应中的能量变化关系与③相符合的是_______(填序号)。
A.H2+Cl2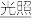 2HCl 2HCl | B.C+CO2 2CO 2CO |
C. +Ba2+=BaSO4↓ +Ba2+=BaSO4↓ | D.NH3•H2O+HCl=NH4Cl+H2O |
(3)将①中涉及的反应设计成如图所示的原电池。电极材料X不能是_______(填序号)。
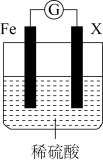
| A.Cu | B.Zn | C.Pb | D.石墨 |
(4)在300℃时,X、Y、Z三种气体在恒容密闭容器中反应时的浓度变化如图所示:
更新时间:2022-10-04 10:11:02
|
相似题推荐
解答题-实验探究题
|
容易
(0.94)
名校
解题方法
【推荐1】某化学实验小组设计了如图三套实验装置探究化学能与热能的转化关系(装置中夹持仪器已略去)。回答下列问题:
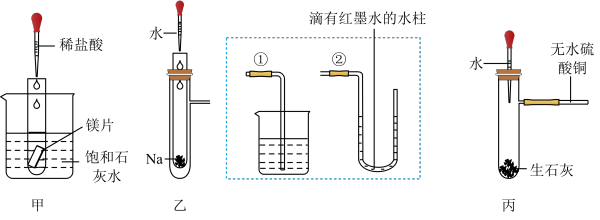
(1)观察到甲装置中的实验现象是____ ;产生该现象的原因是____ 。
(2)将乙装置中外层具支试管的支管与虚线框内的①连接,实验现象是____ ;支管与②连接,实验现象是____ 。钠与水的总能量____ (填“大于”或“小于”)生成物的能量。
(3)装置丙中将胶头滴管内的水滴到生石灰上,支管处的白色粉末(无水硫酸铜)变为蓝色,其原因_____ 。
(4)上述三个实验方案均验证了以上三个反应的反应物化学键断裂吸收的能量____ (填“高于”或“低于”)生成物化学键形成放出的能量;物质中的化学能通过____ 转化成____ 释放出来。

(1)观察到甲装置中的实验现象是
(2)将乙装置中外层具支试管的支管与虚线框内的①连接,实验现象是
(3)装置丙中将胶头滴管内的水滴到生石灰上,支管处的白色粉末(无水硫酸铜)变为蓝色,其原因
(4)上述三个实验方案均验证了以上三个反应的反应物化学键断裂吸收的能量
您最近一年使用:0次
解答题-原理综合题
|
容易
(0.94)
【推荐1】填空。
(1)下列反应中,属于吸热反应的是___________(填字母)。
(2)化学反应过程中,不仅有物质的变化,还伴随有能量的变化。根据下图写出反应的热化学方程式___________ 。

(3)化学反应速率和化学平衡是化学反应原理的重要组成成分。将4.0molPCl3和2.0molCl2充入10L恒容密闭容器中,在一定条件下发生反应PCl3(g)+Cl2(g)⇌PCl5(g),经2min达到平衡时,PCl5为0.4mol。
①在0~2min内,用Cl2表示的反应速率为v(Cl2)=___________ mol/(L·min)
②达到平衡时,PCl3的转化率为___________ 。
(1)下列反应中,属于吸热反应的是___________(填字母)。
| A.Na2O与水反应 | B.甲烷的燃烧反应 | C.CaCO3受热分解 | D.锌与盐酸反应 |

(3)化学反应速率和化学平衡是化学反应原理的重要组成成分。将4.0molPCl3和2.0molCl2充入10L恒容密闭容器中,在一定条件下发生反应PCl3(g)+Cl2(g)⇌PCl5(g),经2min达到平衡时,PCl5为0.4mol。
①在0~2min内,用Cl2表示的反应速率为v(Cl2)=
②达到平衡时,PCl3的转化率为
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
解题方法
【推荐2】某化学实验小组设计了如图三套实验装置探究化学能与热能的转化关系(装置中夹持仪器已略去)。回答下列问题:

(1)观察到甲装置中的实验现象是____ ;产生该现象的原因是____ 。
(2)将乙装置中外层具支试管的支管与虚线框内的①连接,实验现象是____ ;支管与②连接,实验现象是____ 。钠与水的总能量____ (填“大于”或“小于”)生成物的能量。
(3)装置丙中将胶头滴管内的水滴到生石灰上,支管处的白色粉末(无水硫酸铜)变为蓝色,其原因_____ 。
(4)上述三个实验方案均验证了以上三个反应的反应物化学键断裂吸收的能量____ (填“高于”或“低于”)生成物化学键形成放出的能量;物质中的化学能通过____ 转化成____ 释放出来。

(1)观察到甲装置中的实验现象是
(2)将乙装置中外层具支试管的支管与虚线框内的①连接,实验现象是
(3)装置丙中将胶头滴管内的水滴到生石灰上,支管处的白色粉末(无水硫酸铜)变为蓝色,其原因
(4)上述三个实验方案均验证了以上三个反应的反应物化学键断裂吸收的能量
您最近一年使用:0次
【推荐3】50mL0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液在图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热,回答下列问题:_______ 。
(2)实验中改用60mL0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量_____________ (填“相等”、“不相等”),所求中和热_____________ ,(填“相等”、“不相等”),简述理由________________________ 。
(3)化学反应中的能量变化,通常主要表现为热量的变化。下列反应中,属于放热反应的是___________ (填序号)。
a. Ba(OH)2·8H2O与NH4Cl混合搅拌
b. 高温煅烧石灰石
c. 铝与盐酸反应
(4) 已知N2(g)+2O2(g)=2 NO2(g) △H=+67.7 kJ·mol-1, N2H4(g)+O2(g)= N2(g)+2H2O (g) △H=-534 kJ·mol-1,根据盖斯定律写出肼与NO2完全反应生成氮气和气态水的热化学方程式________________ 。
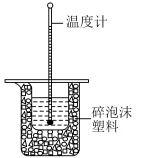
(2)实验中改用60mL0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量
(3)化学反应中的能量变化,通常主要表现为热量的变化。下列反应中,属于放热反应的是
a. Ba(OH)2·8H2O与NH4Cl混合搅拌
b. 高温煅烧石灰石
c. 铝与盐酸反应
(4) 已知N2(g)+2O2(g)=2 NO2(g) △H=+67.7 kJ·mol-1, N2H4(g)+O2(g)= N2(g)+2H2O (g) △H=-534 kJ·mol-1,根据盖斯定律写出肼与NO2完全反应生成氮气和气态水的热化学方程式
您最近一年使用:0次
解答题-原理综合题
|
容易
(0.94)
解题方法
【推荐1】回答下列问题。
(1)一定条件下,在 密闭容器中充入
密闭容器中充入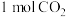 和
和 ,发生反应:
,发生反应: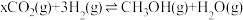 。测得
。测得 和
和 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。
___________ ; 内
内 的平均反应速率
的平均反应速率
___________ 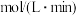 ,平衡时
,平衡时 的转化率为
的转化率为___________ 。
(2)下列措施能提高正反应速率的是___________(填正确答案的字母)。
(3)工业上常以水煤气( 和
和 )为原料合成甲醇。已知:
)为原料合成甲醇。已知: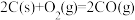
 ;
;
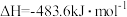 ,则
,则 与
与 制备水煤气的热化学方程式为
制备水煤气的热化学方程式为___________ 。
(1)一定条件下,在
 密闭容器中充入
密闭容器中充入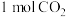 和
和 ,发生反应:
,发生反应: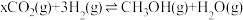 。测得
。测得 和
和 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。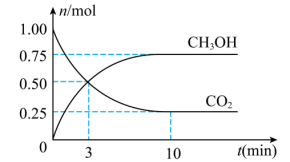

 内
内 的平均反应速率
的平均反应速率
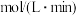 ,平衡时
,平衡时 的转化率为
的转化率为(2)下列措施能提高正反应速率的是___________(填正确答案的字母)。
| A.降低温度 | B.增加 的量 的量 | C.使用催化剂 | D.及时分离出甲醇 |
 和
和 )为原料合成甲醇。已知:
)为原料合成甲醇。已知: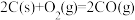
 ;
;
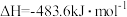 ,则
,则 与
与 制备水煤气的热化学方程式为
制备水煤气的热化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
容易
(0.94)
名校
解题方法
【推荐2】在一定条件下,二氧化硫和氧气发生反应:2SO2(g)+O2(g) 2SO3(g)。
2SO3(g)。
(1)降低温度,化学反应速率___ (填“增大”“减小”或“不变”)。
(2)600℃时,在一容积为2L的密闭容器中,将二氧化硫和氧气混合,在反应进行至10min和20min时,分别改变了影响反应的一个条件,反应过程中SO2、O2、SO3物质的量变化如图所示,反应前15min用SO3表示的平均反应速率为___ 。
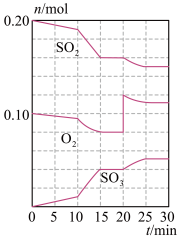
(3)已知0-15min反应放出的总热量为QkJ,写出该反应的热化学方程式____ 。
(4)根据如图判断,10min时改变的反应条件可能是___ (填编号,下同);20min时改变的反应条件可能是____ 。
a.加入催化剂 b.缩小容器容积
c.降低温度 d.增加O2的物质的量
 2SO3(g)。
2SO3(g)。(1)降低温度,化学反应速率
(2)600℃时,在一容积为2L的密闭容器中,将二氧化硫和氧气混合,在反应进行至10min和20min时,分别改变了影响反应的一个条件,反应过程中SO2、O2、SO3物质的量变化如图所示,反应前15min用SO3表示的平均反应速率为

(3)已知0-15min反应放出的总热量为QkJ,写出该反应的热化学方程式
(4)根据如图判断,10min时改变的反应条件可能是
a.加入催化剂 b.缩小容器容积
c.降低温度 d.增加O2的物质的量
您最近一年使用:0次
解答题-原理综合题
|
容易
(0.94)
解题方法
【推荐3】 Ⅰ. 已知某反应:A(g)+ 3B(g)  C(s)+ 4D(g)(A,B,C,D为四种相对分子质量不同的物质)。一定温度下,向恒容密闭容器中充入一定量的A和B。测得各物质的浓度随时间变化如下表所示。
C(s)+ 4D(g)(A,B,C,D为四种相对分子质量不同的物质)。一定温度下,向恒容密闭容器中充入一定量的A和B。测得各物质的浓度随时间变化如下表所示。
(1)t1 h时,c(D) ___________ mol/L。
(2)0-t2 h内,以A的浓度变化表示反应的平均速率:v(A)___________ mol·L-1·h-1。
(3)下列能说明该反应达到平衡状态的是___________(填标号)。
Ⅱ.
(4)合成氨反应中,温度越低,氨的产率越高,但在生产中选定的反应温度为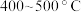 ,原因是
,原因是_________________________ 。
(5)合成氨反应可能的微观历程如图所示:
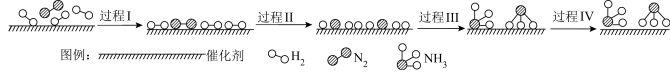
吸附在催化剂表面的物质用*标注。已知过程Ⅱ可以表示为 ,则过程Ⅲ可以表示为
,则过程Ⅲ可以表示为___________ 。
 C(s)+ 4D(g)(A,B,C,D为四种相对分子质量不同的物质)。一定温度下,向恒容密闭容器中充入一定量的A和B。测得各物质的浓度随时间变化如下表所示。
C(s)+ 4D(g)(A,B,C,D为四种相对分子质量不同的物质)。一定温度下,向恒容密闭容器中充入一定量的A和B。测得各物质的浓度随时间变化如下表所示。浓度/( ) ) | c(A) | c(B) | c(D) |
| 0 | 1.0 | 3.0 | 0 |
 h h | 0.8 | ||
 h h | 2.1 |
(2)0-t2 h内,以A的浓度变化表示反应的平均速率:v(A)
(3)下列能说明该反应达到平衡状态的是___________(填标号)。
| A.容器中的压强不随时间变化 | B.气体密度不再变化 |
| C.B和D的浓度之比为3:4 | D.消耗0.3 mol B的同时生成0.4 mol D |
Ⅱ.
(4)合成氨反应中,温度越低,氨的产率越高,但在生产中选定的反应温度为
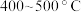 ,原因是
,原因是(5)合成氨反应可能的微观历程如图所示:

吸附在催化剂表面的物质用*标注。已知过程Ⅱ可以表示为
 ,则过程Ⅲ可以表示为
,则过程Ⅲ可以表示为
您最近一年使用:0次
解答题-原理综合题
|
容易
(0.94)
【推荐1】反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势如图所示:
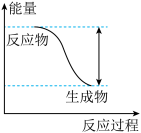
(1)该反应为_________ (填“吸热”或“放热”)反应。
(2)若要使该反应的反应速率增大,下列措施可行的是_________ (填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度 D.使用催化剂
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为:_________ (填“正”或“负”)极,该极上发生的电极反应为:_________ ,外电路中电子移动方向为:_________ 。

(1)该反应为
(2)若要使该反应的反应速率增大,下列措施可行的是
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度 D.使用催化剂
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为:
您最近一年使用:0次



