分类法是进行化学研究的重要方法。不同的标准可以把物质及化学反应分为不同的类别。现有以下物质:①固体氢氧化钠②熔化的铁块③CaCO3④Fe(OH)3胶体⑤NaHSO4溶液⑥干冰⑦盐酸⑧蔗糖
(1)以上物质中能导电的是_______ (填序号,下同),属于电解质是_______ 。
(2)④⑤的微观本质区别是_______ 。
(3)如图为离子反应、氧化还原反应和置换反应三者之间的关系,采用的分类方法名称是_______ ,其中表示离子反应的是_______ (填字母)。
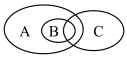
(4)有同学认为所有强酸、强碱之间的中和反应均可表示为OH-+H+=H2O,请举个例子反驳上述观点(用离子方程式表示)_______ 。
(5)将过量的⑥放入①的溶液中充分反应,然后将反应后的溶液分成两等份,分别加入足量的硝酸、氢氧化钙溶液。请分别写出发生反应的离子方程式:①_______ 。②_______ 。
(1)以上物质中能导电的是
(2)④⑤的微观本质区别是
(3)如图为离子反应、氧化还原反应和置换反应三者之间的关系,采用的分类方法名称是

(4)有同学认为所有强酸、强碱之间的中和反应均可表示为OH-+H+=H2O,请举个例子反驳上述观点(用离子方程式表示)
(5)将过量的⑥放入①的溶液中充分反应,然后将反应后的溶液分成两等份,分别加入足量的硝酸、氢氧化钙溶液。请分别写出发生反应的离子方程式:①
更新时间:2022-10-12 13:35:27
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.某课外活动小组进行 胶体的制备实验并检验其性质。
胶体的制备实验并检验其性质。
现有甲、乙、丙三名同学分别进行 胶体的制备实验。
胶体的制备实验。
甲同学:向 的
的 溶液中加入少量NaOH溶液。
溶液中加入少量NaOH溶液。
乙同学:直接加热饱和 溶液。
溶液。
丙同学:向25mL沸水中逐滴加入5~6滴饱和 溶液,继续煮沸至溶液呈红褐色,停止加热;
溶液,继续煮沸至溶液呈红褐色,停止加热;
试回答下列问题
(1)其中操作正确的同学是___________ ;
(2)写出生成 胶体的化学方程式:
胶体的化学方程式:___________ ;
(3)证明有 胶体生成的实验操作与现象是
胶体生成的实验操作与现象是___________ ;
Ⅱ.丁同学利用所制得的 胶体进行实验:
胶体进行实验:
(4)取少量制得的 胶体加入试管中,然后加入
胶体加入试管中,然后加入 溶液,现象是
溶液,现象是___________ 。
(5)将其装入U形管内,用石墨作电极,通电一段时间后发现阴极区附近的颜色逐渐变深,这表明 胶体粒子带
胶体粒子带___________ (填“正”或“负”)电荷。
(6)用___________ 的方法精制 胶体。请设计实验证明胶体和
胶体。请设计实验证明胶体和 两者已完全分离:
两者已完全分离:___________ 。
(7)戊同学则认为用该方法很难完全分离除尽 胶体中的
胶体中的 ,请说明理由
,请说明理由________ 。
 胶体的制备实验并检验其性质。
胶体的制备实验并检验其性质。现有甲、乙、丙三名同学分别进行
 胶体的制备实验。
胶体的制备实验。甲同学:向
 的
的 溶液中加入少量NaOH溶液。
溶液中加入少量NaOH溶液。乙同学:直接加热饱和
 溶液。
溶液。丙同学:向25mL沸水中逐滴加入5~6滴饱和
 溶液,继续煮沸至溶液呈红褐色,停止加热;
溶液,继续煮沸至溶液呈红褐色,停止加热;试回答下列问题
(1)其中操作正确的同学是
(2)写出生成
 胶体的化学方程式:
胶体的化学方程式:(3)证明有
 胶体生成的实验操作与现象是
胶体生成的实验操作与现象是Ⅱ.丁同学利用所制得的
 胶体进行实验:
胶体进行实验:(4)取少量制得的
 胶体加入试管中,然后加入
胶体加入试管中,然后加入 溶液,现象是
溶液,现象是(5)将其装入U形管内,用石墨作电极,通电一段时间后发现阴极区附近的颜色逐渐变深,这表明
 胶体粒子带
胶体粒子带(6)用
 胶体。请设计实验证明胶体和
胶体。请设计实验证明胶体和 两者已完全分离:
两者已完全分离:(7)戊同学则认为用该方法很难完全分离除尽
 胶体中的
胶体中的 ,请说明理由
,请说明理由
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】(1)15.6gNa2X中含Na+0.4mol,则Na2X的摩尔质量是____________ 。
(2)设NA为阿伏加 德罗常数的数值,如果a g氧气中含有的分子数为b,则c g氧气在标准状况下的体积约是_________________ (用含NA的式子表示)。
(3)某溶液由Mg2+、Al3+、Cl-、SO42- 4种离子组成,测得其中Al3+、SO42-、Cl-的物质的量浓度之比为3:1:13,则溶液中Mg2+、Al3+、SO42-的物质的量浓度之比为___________ 。
(4)标况下,密度为1.25g/L的CO2与CH4组成的混合气体中,CO2的体积分数为______ 。
(5)将标准状况下体积为aL的HCl气体溶于1000g水中,得到盐酸的密度为b g/cm3,则 该盐酸的物质的量浓度为______________ mol/L。
(6)下列各项与胶体性质无关的有______________________ 。
①卤水点豆腐 ②明矾净水 ③静电除尘 ④油水分离 ⑤血液透析 ⑥三角洲形成 ⑦酸碱中和 ⑧雨后彩虹和海市蜃楼 ⑨臭氧消毒
(2)设NA为阿伏加 德罗常数的数值,如果a g氧气中含有的分子数为b,则c g氧气在标准状况下的体积约是
(3)某溶液由Mg2+、Al3+、Cl-、SO42- 4种离子组成,测得其中Al3+、SO42-、Cl-的物质的量浓度之比为3:1:13,则溶液中Mg2+、Al3+、SO42-的物质的量浓度之比为
(4)标况下,密度为1.25g/L的CO2与CH4组成的混合气体中,CO2的体积分数为
(5)将标准状况下体积为aL的HCl气体溶于1000g水中,得到盐酸的密度为b g/cm3,则 该盐酸的物质的量浓度为
(6)下列各项与胶体性质无关的有
①卤水点豆腐 ②明矾净水 ③静电除尘 ④油水分离 ⑤血液透析 ⑥三角洲形成 ⑦酸碱中和 ⑧雨后彩虹和海市蜃楼 ⑨臭氧消毒
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】无水氯化铝在生产、生活中应用广泛。
(1)氯化铝在水中形成具有净水作用的氢氧化铝胶体,其反应的离子方程式为___________ 。
(2)工业上用铝土矿(主要成分为Al2O3,含有Fe2O3、SiO2等杂质)制取无水氯化铝的一种工艺流程示意如下:
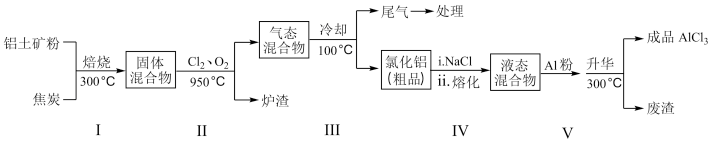
已知:
①步骤Ⅰ中焙烧使固体水分挥发、气孔数目增多,其作用是_____ (只要求写出一种)。
②步骤Ⅱ中若不通入氯气和氧气,则反应生成相对原子质量比硅大的单质是_____ 。
③步骤Ⅲ的尾气经冷却至室温后,气体用足量的NaOH冷溶液吸收,生成的盐主要有3种,其化学式分别为_________________________ 。
④结合流程及相关数据分析,步骤Ⅴ中加入铝粉的目的是_________ 。
(1)氯化铝在水中形成具有净水作用的氢氧化铝胶体,其反应的离子方程式为
(2)工业上用铝土矿(主要成分为Al2O3,含有Fe2O3、SiO2等杂质)制取无水氯化铝的一种工艺流程示意如下:

已知:
| 物质 | SiCl4 | AlCl3 | FeCl3 | FeCl2 |
| 沸点/℃ | 57.6 | 180(升华) | 300(升华) | 1023 |
②步骤Ⅱ中若不通入氯气和氧气,则反应生成相对原子质量比硅大的单质是
③步骤Ⅲ的尾气经冷却至室温后,气体用足量的NaOH冷溶液吸收,生成的盐主要有3种,其化学式分别为
④结合流程及相关数据分析,步骤Ⅴ中加入铝粉的目的是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】现有下列10种物质:
①冰水混合物 ②碱石灰 ③Mg ④ ⑤熔融KOH ⑥
⑤熔融KOH ⑥ 溶液⑦
溶液⑦ ⑧硫酸 ⑨
⑧硫酸 ⑨ ⑩固体
⑩固体 。回答下列问题。
。回答下列问题。
(1)属于混合物的是____________ 填编号,下同),属于强电解质且能导电的是___________ ,属于非电解质的是___________ 。
(2)将⑥和⑩均配成0.1mol/L的溶液按下表中的不同配比进行混合:
a.按丁方式混合后,所得溶液显___________ (填“酸”“碱”“中”)性;
b.按乙方式混合时,反应的离子方程式为___________ 。
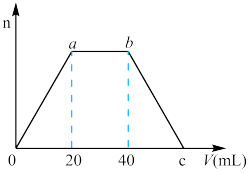
(3)向⑤和⑥制成混合溶液中通入足量的④气体,生成沉淀的物质的量(n)和通入气体体积(V)的关系如图所示,则c点的气体体积是___________ mL;混合溶液中KOH和 的物质的量之比为
的物质的量之比为___________ ;写出ab段发生的离子方程式_________ 。
①冰水混合物 ②碱石灰 ③Mg ④
 ⑤熔融KOH ⑥
⑤熔融KOH ⑥ 溶液⑦
溶液⑦ ⑧硫酸 ⑨
⑧硫酸 ⑨ ⑩固体
⑩固体 。回答下列问题。
。回答下列问题。(1)属于混合物的是
(2)将⑥和⑩均配成0.1mol/L的溶液按下表中的不同配比进行混合:
| 甲 | 乙 | 丙 | 丁 | 戊 | |
0.1mol/L  溶液的体积/mL 溶液的体积/mL | 10 | 10 | 10 | 10 | 10 |
0.1mol/L  溶液的体积/mL 溶液的体积/mL | 5 | 10 | 15 | 20 | 25 |
b.按乙方式混合时,反应的离子方程式为
(3)向⑤和⑥制成混合溶液中通入足量的④气体,生成沉淀的物质的量(n)和通入气体体积(V)的关系如图所示,则c点的气体体积是
 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。下表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是__________ 。
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸
(2)在溶液配制过程中,下列操作正确且对配制结果没有影响的是__________ 。
A.将药品放入容量瓶中加蒸馏水溶解
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(3)配制上述500mL“鲜花保鲜剂”所需的玻璃仪器有:烧杯、玻璃棒、_____________ 、__________ 。(在横线上填写所缺仪器的名称)
(4)鲜花保鲜剂中K+(蔗糖、阿司匹林中不含K+) 的物质的量浓度为______ mol/L。
| 成分 | 质量(g) | 摩尔质量(g/mol) |
| 蔗糖 | 50.00 | 342 |
| 硫酸钾 | 0.87 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.158 | 158 |
| 硝酸银 | 0.04 | 170 |
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸
(2)在溶液配制过程中,下列操作正确且对配制结果没有影响的是
A.将药品放入容量瓶中加蒸馏水溶解
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(3)配制上述500mL“鲜花保鲜剂”所需的玻璃仪器有:烧杯、玻璃棒、
(4)鲜花保鲜剂中K+(蔗糖、阿司匹林中不含K+) 的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】海洋约占地球表面积的71%,其中水资源和其他化学资源具有巨大的开发潜力。海水中含NaCl等多种盐类。目前,通过海水晒盐可制得 和苦卤,食盐精制后可制成饱和
和苦卤,食盐精制后可制成饱和 用以生产
用以生产 、
、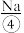 、
、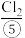 等。苦卤经过氯气氧化,热空气吹出、
等。苦卤经过氯气氧化,热空气吹出、 吸收等一系列操作可获得
吸收等一系列操作可获得 。
。
(1)上述编号①—⑥的6种物质中,属于电解质的是_____ (填编号,下同),能导电的是______ 。
(2)实验室现有一瓶浓盐酸,其瓶上标签如图所示:
则该盐酸中溶质物质的量浓度为______ 。100mL该浓盐酸与足量的 反应,实际生成的气体体积(标准状况下)
反应,实际生成的气体体积(标准状况下)_____ 6.72L(填“>”、“<”或“=”)。
(3)实验室需要 的稀盐酸。若利用如图所示浓盐酸进行配制,需要用量筒量取浓盐酸的体积为
的稀盐酸。若利用如图所示浓盐酸进行配制,需要用量筒量取浓盐酸的体积为_____ 。所需仪器除烧杯、量筒、玻璃棒、胶头滴管外,还必须用到的一种玻璃仪器为______ 。
(4)下列操作会使配制的溶液物质的量浓度偏低的是_____。
 和苦卤,食盐精制后可制成饱和
和苦卤,食盐精制后可制成饱和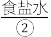 用以生产
用以生产 、
、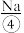 、
、 等。苦卤经过氯气氧化,热空气吹出、
等。苦卤经过氯气氧化,热空气吹出、 吸收等一系列操作可获得
吸收等一系列操作可获得 。
。(1)上述编号①—⑥的6种物质中,属于电解质的是
(2)实验室现有一瓶浓盐酸,其瓶上标签如图所示:
| 盐酸 | |
| 分子式 | HCl |
| 相对分子质量 | 36.5 |
| 密度 | 1.2g/cm3 |
| HCl的质量分数 | 36.5% |
 反应,实际生成的气体体积(标准状况下)
反应,实际生成的气体体积(标准状况下)(3)实验室需要
 的稀盐酸。若利用如图所示浓盐酸进行配制,需要用量筒量取浓盐酸的体积为
的稀盐酸。若利用如图所示浓盐酸进行配制,需要用量筒量取浓盐酸的体积为(4)下列操作会使配制的溶液物质的量浓度偏低的是_____。
| A.定容时俯视刻度线 | B.转移前,容量瓶内有蒸馏水 |
| C.转移过程中有液体洒出 | D.定容时水加多了用胶头滴管吸出 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】导电性实验可以作为研究电解质电离本质及反应机理的有效方法。
(1)在如下图所示的装置里,若灯泡亮,广口瓶内的物质A可以是________ (填序号)。
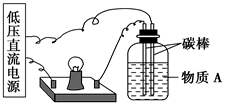
①干燥的氯化钠晶体 ②干燥的氢氧化钠晶体 ③蔗糖晶体 ④酒精 ⑤氯化钠溶液 ⑥氢氧化钠溶液 ⑦稀盐酸 ⑧硫酸铜溶液
(2)在电解质溶液的导电性装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是________ 。
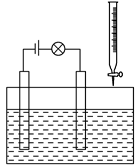
A.盐酸中逐滴加入食盐溶液
B.硫酸中逐滴加入氢氧化钠溶液
C.石灰乳中滴加稀盐酸
D.硫酸中逐滴加入氢氧化钡溶液
(1)在如下图所示的装置里,若灯泡亮,广口瓶内的物质A可以是

①干燥的氯化钠晶体 ②干燥的氢氧化钠晶体 ③蔗糖晶体 ④酒精 ⑤氯化钠溶液 ⑥氢氧化钠溶液 ⑦稀盐酸 ⑧硫酸铜溶液
(2)在电解质溶液的导电性装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是

A.盐酸中逐滴加入食盐溶液
B.硫酸中逐滴加入氢氧化钠溶液
C.石灰乳中滴加稀盐酸
D.硫酸中逐滴加入氢氧化钡溶液
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.有下列物质①氢氧化钠固体;②铜丝;③氯化氢气体;④盐酸;⑤二氧化碳气体;⑥氨水;⑦碳酸钠粉末;⑧蔗糖晶体;⑨熔融氯化钠;请用序号填空:
(1)上述状态下可导电的是___________ ;
(2)属于电解质的是___________ ;
(3)属于非电解质的是___________ ;
(4)属于电解质,但在上述状态下不能导电的是___________ 。
Ⅱ.某工厂甲、乙两车间,分别排放的污水中含有大量的Ag+、Ba2+、Fe3+、Na+、Cl-、SO 、NO
、NO 、OH-中的四种。若各自单独排放会造成较大污染,如果混合后再排放,则会大大降低污染程度。现测得甲车间排放的污水呈碱性。则
、OH-中的四种。若各自单独排放会造成较大污染,如果混合后再排放,则会大大降低污染程度。现测得甲车间排放的污水呈碱性。则
(5)甲车间污水中含有的四种离子可能是___________ 。
(6)乙车间污水中含有的四种离子可能是___________ 。
(1)上述状态下可导电的是
(2)属于电解质的是
(3)属于非电解质的是
(4)属于电解质,但在上述状态下不能导电的是
Ⅱ.某工厂甲、乙两车间,分别排放的污水中含有大量的Ag+、Ba2+、Fe3+、Na+、Cl-、SO
 、NO
、NO 、OH-中的四种。若各自单独排放会造成较大污染,如果混合后再排放,则会大大降低污染程度。现测得甲车间排放的污水呈碱性。则
、OH-中的四种。若各自单独排放会造成较大污染,如果混合后再排放,则会大大降低污染程度。现测得甲车间排放的污水呈碱性。则(5)甲车间污水中含有的四种离子可能是
(6)乙车间污水中含有的四种离子可能是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知氟、氯、溴、碘在元素周期表中位于同一纵行,都是典型的非金属元素,都能与大多数金属化合生成盐,故统称为卤素。卤素单质都具有氧化性,其氧化性强弱顺序是F2>Cl2>Br2>I2,它们都能与H2、H2O等反应。
(1)若用X2表示卤素单质,则X2与H2化合的化学方程式是_______ ,其反应条件难易规律是_______ 。
(2)氧化性强的卤素单质(如Cl2)能把氧化性弱的卤素从其卤化物(如NaBr或KI)中置换出来。请写出将氯气通入碘化钾溶液中的化学方程式________ 。
(3)已知氯化铝的熔点为190℃(2.202×l05Pa),但它在180℃即开始升华。
①氯化铝是_______ 。(填“离子化合物”或“共价化合物”)
②在500 K和1.01×105 Pa时,它的蒸气密度(换算为标准状况时)为11.92 g·L-1,试确定氯化铝在蒸气状态时的化学式为_______ 。
③设计一个可靠的实验,判断氧化铝是离子化合物还是共价化合物。你设计的实验是_______ 。
(1)若用X2表示卤素单质,则X2与H2化合的化学方程式是
(2)氧化性强的卤素单质(如Cl2)能把氧化性弱的卤素从其卤化物(如NaBr或KI)中置换出来。请写出将氯气通入碘化钾溶液中的化学方程式
(3)已知氯化铝的熔点为190℃(2.202×l05Pa),但它在180℃即开始升华。
①氯化铝是
②在500 K和1.01×105 Pa时,它的蒸气密度(换算为标准状况时)为11.92 g·L-1,试确定氯化铝在蒸气状态时的化学式为
③设计一个可靠的实验,判断氧化铝是离子化合物还是共价化合物。你设计的实验是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】硫酰氯(SO2Cl2)熔点-54.1℃、沸点69.2℃,在染料、药品、除草剂和农用杀虫剂的生产过程中有重要作用。
(1)SO2Cl2中S的化合价为_______ ,SO2Cl2在潮湿空气中因水解“发烟”的化学方程式为________________ 。
(2)现拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯,实验装置如图所示(夹持装置未画出)。
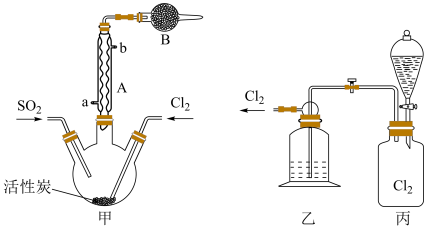
①仪器A的名称为___________ ,装置乙中装入的试剂_____________ ,装置B的作用是_______________________ 。
②装置丙分液漏斗中盛装的最佳试剂是________ (选填字母)。
A.蒸馏水 B.10.0 mol/L浓盐酸
C.浓氢氧化钠溶液 D.饱和食盐水
(3)探究硫酰氯在催化剂作用下加热分解的产物,实验装置如图所示(部分夹持装置未画出)。
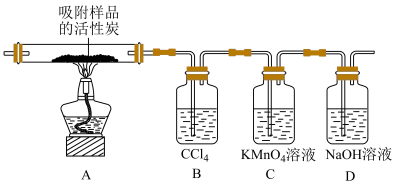
①加热时A中试管出现黄绿色,装置B的作用是____________ 。
②装置C中的现象是___________ ,反应的离子方程式为___________________ 。
(1)SO2Cl2中S的化合价为
(2)现拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯,实验装置如图所示(夹持装置未画出)。

①仪器A的名称为
②装置丙分液漏斗中盛装的最佳试剂是
A.蒸馏水 B.10.0 mol/L浓盐酸
C.浓氢氧化钠溶液 D.饱和食盐水
(3)探究硫酰氯在催化剂作用下加热分解的产物,实验装置如图所示(部分夹持装置未画出)。

①加热时A中试管出现黄绿色,装置B的作用是
②装置C中的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】二氯化硫(SCl2)是一种红棕色液体,可用作于制造杀虫剂。 与水反应可生成
与水反应可生成 、
、 和
和 。为验证
。为验证 与水反应的产物,某小组设计如下图所示装置进行实验:
与水反应的产物,某小组设计如下图所示装置进行实验:
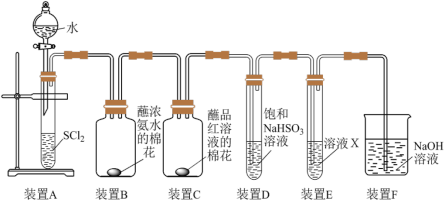
(1)SCl2分子中,各原子均满足最外层8电子稳定结构。 的电子式为
的电子式为___________ 。
(2)SCl2与水反应的化学方程式为___________ 。
(3)装置B、C中的实验现象分别为___________ 和___________ 。
(4)若溶液X为 ,实验中可观察到的现象是
,实验中可观察到的现象是___________ ,该现象表现了 的
的___________ 性。
(5)若溶液 为Ba(NO3)2溶液,写出该反应的离子方程式
为Ba(NO3)2溶液,写出该反应的离子方程式___________ 。
(6)工业上有多种方法可用于SO2的脱除。其中之一是用NaClO溶液作为吸收剂,调pH至5.5时吸收SO2,反应离子方程式是___________ 。
 与水反应可生成
与水反应可生成 、
、 和
和 。为验证
。为验证 与水反应的产物,某小组设计如下图所示装置进行实验:
与水反应的产物,某小组设计如下图所示装置进行实验:
(1)SCl2分子中,各原子均满足最外层8电子稳定结构。
 的电子式为
的电子式为(2)SCl2与水反应的化学方程式为
(3)装置B、C中的实验现象分别为
(4)若溶液X为
 ,实验中可观察到的现象是
,实验中可观察到的现象是 的
的(5)若溶液
 为Ba(NO3)2溶液,写出该反应的离子方程式
为Ba(NO3)2溶液,写出该反应的离子方程式(6)工业上有多种方法可用于SO2的脱除。其中之一是用NaClO溶液作为吸收剂,调pH至5.5时吸收SO2,反应离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下列编号代表元素周期表中的一部分元素,用化学用语回答下列问题:
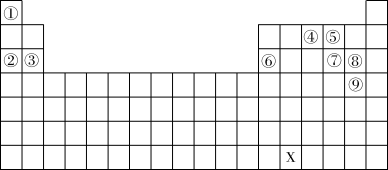
(1)①④形成的化合物的化学键类型为_______ 。③⑧形成的化合物的电子式为:_______ 。
(2)②、⑥的最高价氧化物的水化物发生反应的离子方程式为_______ 。⑧的单质通入①⑨形成化合物的溶液中反应,写出反应的离子方程式_______ 。
(3)⑧⑨简单氢化物的稳定性较强的是_______ ,⑤单质的氧化性比⑦的强,请从原子结构的角度解释其原因:_______ 。
(4)写出能证明②的金属性强于③的化学事实_______ (任写一条)。
(5)元素X的原子结构示意图为_______ 。

(1)①④形成的化合物的化学键类型为
(2)②、⑥的最高价氧化物的水化物发生反应的离子方程式为
(3)⑧⑨简单氢化物的稳定性较强的是
(4)写出能证明②的金属性强于③的化学事实
(5)元素X的原子结构示意图为
您最近一年使用:0次



