某氮肥厂氨氮废水中的氮元素多以NH3•H2O和 的形式存在,该废水的处理流程如下:
的形式存在,该废水的处理流程如下:
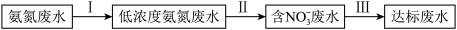
(1)步骤I的操作如下:加NaOH溶液,调节pH至9后,升温至30℃,通空气将氨赶出并回收。NH3•H2O的分解反应属于___________ (填“吸热”或“放热”)反应。
(2)步骤II:在微生物作用下, 经过连续两步反应被氧化成
经过连续两步反应被氧化成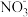 两步反应的能量变化示意图如下:
两步反应的能量变化示意图如下:
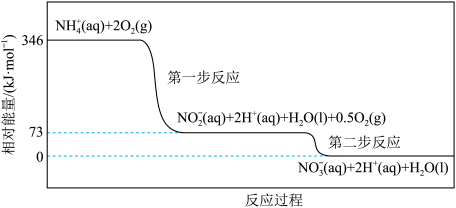
两步反应的反应热分别记为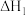 、
、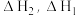
___________ 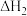 ,(填“>”或“<”);第一步反应是
,(填“>”或“<”);第一步反应是___________ (填“放热”或“吸热”)反应,热化学方程式是___________ 。
(3)步骤III:—定条件下,向废水中加入CH3OH,将HNO3还原成N2,该反应的 ,由此判断氧化还原反应一定是放热反应,对吗?
,由此判断氧化还原反应一定是放热反应,对吗?___________ (填“对”或“不对”),请举例说明理由:___________ 。
 的形式存在,该废水的处理流程如下:
的形式存在,该废水的处理流程如下: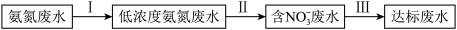
(1)步骤I的操作如下:加NaOH溶液,调节pH至9后,升温至30℃,通空气将氨赶出并回收。NH3•H2O的分解反应属于
(2)步骤II:在微生物作用下,
 经过连续两步反应被氧化成
经过连续两步反应被氧化成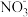 两步反应的能量变化示意图如下:
两步反应的能量变化示意图如下:
两步反应的反应热分别记为
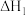 、
、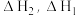
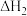 ,(填“>”或“<”);第一步反应是
,(填“>”或“<”);第一步反应是(3)步骤III:—定条件下,向废水中加入CH3OH,将HNO3还原成N2,该反应的
 ,由此判断氧化还原反应一定是放热反应,对吗?
,由此判断氧化还原反应一定是放热反应,对吗?
更新时间:2022-10-24 15:51:38
|
相似题推荐
填空题
|
适中
(0.65)
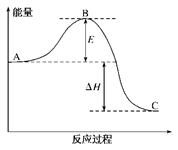
【推荐1】2SO2(g)+O2(g)==2SO3(g)反应过程中的能量变化如下图所示。
已知1mol SO2(g)氧化为1mol SO3(g)的ΔH=-99 kJ·mol-1
请回答下列问题:
(1)图中A、C分别表示__________ 的能量、___________ 的能量;
(2)图中ΔH=______________________ ;
(3)已知单质硫的燃烧热为-296 kJ·mol-1,计算由S(s)生成3mol SO3(g)ΔH=___________ ;
(4)化学反应的焓变与反应物和生成物的键能有关。
已知:①H2(g)+Cl2(g)=2HCl(g) ΔH=-185 kJ·mol-1
②H—H键能为436kJ·mol-1,Cl—Cl键能为247kJ·mol-1。则H—Cl键能为____________________ 。
已知1mol SO2(g)氧化为1mol SO3(g)的ΔH=-99 kJ·mol-1
请回答下列问题:
(1)图中A、C分别表示
(2)图中ΔH=
(3)已知单质硫的燃烧热为-296 kJ·mol-1,计算由S(s)生成3mol SO3(g)ΔH=
(4)化学反应的焓变与反应物和生成物的键能有关。
已知:①H2(g)+Cl2(g)=2HCl(g) ΔH=-185 kJ·mol-1
②H—H键能为436kJ·mol-1,Cl—Cl键能为247kJ·mol-1。则H—Cl键能为
您最近一年使用:0次
【推荐2】化学反应在发生物质变化的同时伴随有能量的变化,是人类获取能量的重要途径,而许多能量的利用与化学反应中的能量变化密切相关。回答下列问题:
(1)已知CH3OH(l)的燃烧热ΔH=−238.6kJ·mol−1,CH3OH(l)+ O2(g)=CO2(g)+2H2O(g) ΔH=−akJ·mol−1,则a
O2(g)=CO2(g)+2H2O(g) ΔH=−akJ·mol−1,则a_______ (填“>”“<”或“=”)238.6。
(2)已知:H2(g)+ O2(g)⇌H2O(g) ΔH=−241.8kJ·mol−1,该反应的活化能为167.2kJ·mol−1,则其逆反应的活化能为
O2(g)⇌H2O(g) ΔH=−241.8kJ·mol−1,该反应的活化能为167.2kJ·mol−1,则其逆反应的活化能为_______ 。
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料:4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) ΔH=−1176kJ·mol−1,则反应过程中,每转移1mol电子放出的热量为_______ kJ。
(4)SO2和H2S是大气污染物,这两种气体的转化研究对资源综合利用和环境保护有重要意义。已知:
①2H2(g)+SO2(g)=S(l)+2H2O(g) ΔH1=+45.4kJ·mol-1
②2CO(g)+SO2(g)=S(l)+2CO2(g) ΔH2=-37.0kJ·mol-1
写出CO(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式_______ ;若该反应在恒温恒容体系中进行,则其达到平衡的标志为_______ (填字母)。
A.单位时间内,生成nmolCO的同时生成nmolCO2
B.混合气体的平均摩尔质量保持不变
C.混合气体的总压强保持不变
D.CO2(g)与H2(g)的体积比保持不变
(1)已知CH3OH(l)的燃烧热ΔH=−238.6kJ·mol−1,CH3OH(l)+
 O2(g)=CO2(g)+2H2O(g) ΔH=−akJ·mol−1,则a
O2(g)=CO2(g)+2H2O(g) ΔH=−akJ·mol−1,则a(2)已知:H2(g)+
 O2(g)⇌H2O(g) ΔH=−241.8kJ·mol−1,该反应的活化能为167.2kJ·mol−1,则其逆反应的活化能为
O2(g)⇌H2O(g) ΔH=−241.8kJ·mol−1,该反应的活化能为167.2kJ·mol−1,则其逆反应的活化能为(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料:4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) ΔH=−1176kJ·mol−1,则反应过程中,每转移1mol电子放出的热量为
(4)SO2和H2S是大气污染物,这两种气体的转化研究对资源综合利用和环境保护有重要意义。已知:
①2H2(g)+SO2(g)=S(l)+2H2O(g) ΔH1=+45.4kJ·mol-1
②2CO(g)+SO2(g)=S(l)+2CO2(g) ΔH2=-37.0kJ·mol-1
写出CO(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式
A.单位时间内,生成nmolCO的同时生成nmolCO2
B.混合气体的平均摩尔质量保持不变
C.混合气体的总压强保持不变
D.CO2(g)与H2(g)的体积比保持不变
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】作为一种绿色消毒剂, 在公共卫生事业中发挥了重要的作用。已知反应:
在公共卫生事业中发挥了重要的作用。已知反应: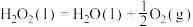
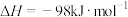
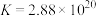
(1) 的强氧化性使其对大多数致病菌和病毒具有消杀功能。用
的强氧化性使其对大多数致病菌和病毒具有消杀功能。用 医用
医用 对传染病房喷洒消毒时,地板上有气泡冒出,该气体是
对传染病房喷洒消毒时,地板上有气泡冒出,该气体是___________ 。
(2)纯 可作为民用驱雹火箭推进剂。在火箭喷口铂网催化下,
可作为民用驱雹火箭推进剂。在火箭喷口铂网催化下, 剧烈分解:
剧烈分解: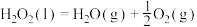 ,放出大量气体,驱动火箭升空。每消耗
,放出大量气体,驱动火箭升空。每消耗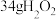 ,理论上
,理论上___________ (填“放出”或“吸收”)热量___________ 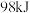 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。
(3)纯 相对稳定,实验表明在
相对稳定,实验表明在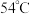 下恒温贮存2周,浓度仍能保持
下恒温贮存2周,浓度仍能保持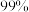 ,原因是
,原因是 分解反应的
分解反应的___________ (填编号)。
a.速率比较小 b. 不解大 c.
不解大 c. 比较小 d.活化能比较大
比较小 d.活化能比较大
(4) 的一种衍生物
的一种衍生物 ,阴离子结构式如图,用“□”标识出
,阴离子结构式如图,用“□”标识出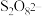 中体现强氧化性的基团:
中体现强氧化性的基团:___________ 。 溶液加热至沸后,溶液
溶液加热至沸后,溶液 降低,用离子方程式表明原因:
降低,用离子方程式表明原因:___________ 。

(5)用惰性电极电解 和硫酸混合溶液生产
和硫酸混合溶液生产 。电解过程中有
。电解过程中有 生成,阳极发生的电极反应可表示为:
生成,阳极发生的电极反应可表示为:___________ 。在无离子交换膜的条件下,通过一定的电量,电解后溶液中不含 ,测得
,测得 含量低于理论值,可能原因是
含量低于理论值,可能原因是___________ 。(忽略电阻且不考虑 的分解)
的分解)
 在公共卫生事业中发挥了重要的作用。已知反应:
在公共卫生事业中发挥了重要的作用。已知反应: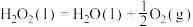
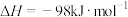
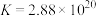
(1)
 的强氧化性使其对大多数致病菌和病毒具有消杀功能。用
的强氧化性使其对大多数致病菌和病毒具有消杀功能。用 医用
医用 对传染病房喷洒消毒时,地板上有气泡冒出,该气体是
对传染病房喷洒消毒时,地板上有气泡冒出,该气体是(2)纯
 可作为民用驱雹火箭推进剂。在火箭喷口铂网催化下,
可作为民用驱雹火箭推进剂。在火箭喷口铂网催化下, 剧烈分解:
剧烈分解: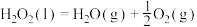 ,放出大量气体,驱动火箭升空。每消耗
,放出大量气体,驱动火箭升空。每消耗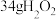 ,理论上
,理论上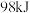 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。(3)纯
 相对稳定,实验表明在
相对稳定,实验表明在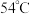 下恒温贮存2周,浓度仍能保持
下恒温贮存2周,浓度仍能保持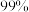 ,原因是
,原因是 分解反应的
分解反应的a.速率比较小 b.
 不解大 c.
不解大 c. 比较小 d.活化能比较大
比较小 d.活化能比较大(4)
 的一种衍生物
的一种衍生物 ,阴离子结构式如图,用“□”标识出
,阴离子结构式如图,用“□”标识出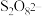 中体现强氧化性的基团:
中体现强氧化性的基团: 溶液加热至沸后,溶液
溶液加热至沸后,溶液 降低,用离子方程式表明原因:
降低,用离子方程式表明原因:
(5)用惰性电极电解
 和硫酸混合溶液生产
和硫酸混合溶液生产 。电解过程中有
。电解过程中有 生成,阳极发生的电极反应可表示为:
生成,阳极发生的电极反应可表示为: ,测得
,测得 含量低于理论值,可能原因是
含量低于理论值,可能原因是 的分解)
的分解)
您最近一年使用:0次
【推荐1】(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g)⇌NH2COONH4(s) ΔH1
反应Ⅱ:NH2COONH4(s)⇌CO(NH2)2(s)+H2O(g) ΔH2=+72.49 kJ·mol-1
总反应:2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g) ΔH3=-86.98 kJ·mol-1
则反应Ⅰ的ΔH1=________ kJ·mol-1。
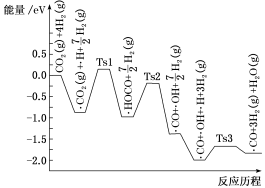
(2)氢气可将CO2还原为甲烷,反应为CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)。ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示,其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会_____ (填“放出热量”或“吸收热量”);反应历程中最小能垒(活化能)步骤的化学方程式为____ 。
(3)已知CO(g)、CH4(g)、CH3CHO(l)的燃烧热分别为283.0 kJ·mol-1、890.31 kJ·mol-1、1 167.9 kJ·mol-1,则乙醛的分解反应CH3CHO(l)⇌CH4(g)+CO(g)的ΔH=________ 。
反应Ⅰ:2NH3(g)+CO2(g)⇌NH2COONH4(s) ΔH1
反应Ⅱ:NH2COONH4(s)⇌CO(NH2)2(s)+H2O(g) ΔH2=+72.49 kJ·mol-1
总反应:2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g) ΔH3=-86.98 kJ·mol-1
则反应Ⅰ的ΔH1=
(2)氢气可将CO2还原为甲烷,反应为CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)。ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示,其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会

(3)已知CO(g)、CH4(g)、CH3CHO(l)的燃烧热分别为283.0 kJ·mol-1、890.31 kJ·mol-1、1 167.9 kJ·mol-1,则乙醛的分解反应CH3CHO(l)⇌CH4(g)+CO(g)的ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
【推荐2】镁化合物具有广泛用途,请回答有关镁的下列问题:
(1)单质镁在空气中燃烧的主要产物是白色的__ ,还生成少量的__ (填化学式)。
(2)CH3MgCl是一种重要的有机合成剂,其中镁的化合价是___ ,该化合物水解的化学方程式为___ 。
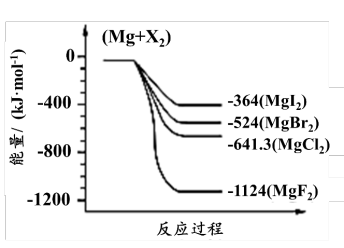
(3)如图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。
下列选项中正确的是__ (填序号)。
①MgI2中Mg2+与I-间的作用力小于MgF2中Mg2+与F-间的作用力
②Mg与F2的反应是放热反应
③MgBr2与Cl2反应的△H<0
④化合物的热稳定性顺序为MgI2>MgBr2>MgCl2>MgF2
⑤MgF2(s)+Br2(l)=MgBr2(s)+F2(g)△H=+600kJ·mol-1
(1)单质镁在空气中燃烧的主要产物是白色的
(2)CH3MgCl是一种重要的有机合成剂,其中镁的化合价是
(3)如图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。

下列选项中正确的是
①MgI2中Mg2+与I-间的作用力小于MgF2中Mg2+与F-间的作用力
②Mg与F2的反应是放热反应
③MgBr2与Cl2反应的△H<0
④化合物的热稳定性顺序为MgI2>MgBr2>MgCl2>MgF2
⑤MgF2(s)+Br2(l)=MgBr2(s)+F2(g)△H=+600kJ·mol-1
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氢气,二甲醚,乙醇都是极具发展潜力的绿色清洁能源。
Ⅰ.关于氢能,根据要求回答问题:
制备氢气常采用以下方法:①电解水法: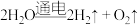
②水煤气法: ,
,
③太阳能光催化分解水法:
(1)三种方法中最节能的是_______ (填标号)。
(2)已知拆开1mol H-H、1mol O=O和1mol H-O分别需要的能量依次为436kJ、498kJ和463kJ,则理论上每 完全分解,需
完全分解,需_______ (填“放出”或“吸收”能量_______ kJ。下列能正确表示该过程的能量变化示意图的是_______ (填标号)。
A.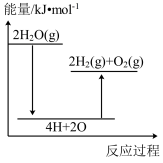 B.
B.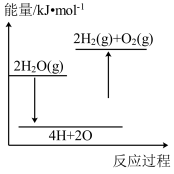
C.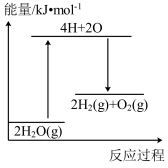 D.
D.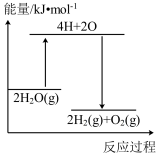
Ⅱ.二甲醚 气体是一种可再生绿色新能源,被誉为“21世纪的清洁燃料”。
气体是一种可再生绿色新能源,被誉为“21世纪的清洁燃料”。
(3)写出二甲醚一种同分异构体的结构简式:_______ 。
(4)工业上可用水煤气合成二甲醚: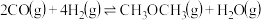
①测得CO和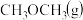 的浓度随时间变化如图所示,则反应开始至平衡时的
的浓度随时间变化如图所示,则反应开始至平衡时的 平均反应速率
平均反应速率
_______ 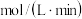 。
。

②若该反应在恒容密闭容器中进行,下列叙述中正确的是_______ 。
A.及时分离出 ,可以加快化学反应速率
,可以加快化学反应速率
B.恒容时,充入He增大压强,化学反应速率不变
C.容器内压强不再变化,说明该反应已达到最大的限度
D. ,说明该反应已达到平衡状态
,说明该反应已达到平衡状态
Ⅰ.关于氢能,根据要求回答问题:
制备氢气常采用以下方法:①电解水法:
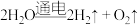
②水煤气法:
 ,
,
③太阳能光催化分解水法:

(1)三种方法中最节能的是
(2)已知拆开1mol H-H、1mol O=O和1mol H-O分别需要的能量依次为436kJ、498kJ和463kJ,则理论上每
 完全分解,需
完全分解,需A.
 B.
B.
C.
 D.
D.
Ⅱ.二甲醚
 气体是一种可再生绿色新能源,被誉为“21世纪的清洁燃料”。
气体是一种可再生绿色新能源,被誉为“21世纪的清洁燃料”。(3)写出二甲醚一种同分异构体的结构简式:
(4)工业上可用水煤气合成二甲醚:
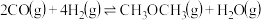
①测得CO和
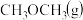 的浓度随时间变化如图所示,则反应开始至平衡时的
的浓度随时间变化如图所示,则反应开始至平衡时的 平均反应速率
平均反应速率
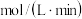 。
。
②若该反应在恒容密闭容器中进行,下列叙述中正确的是
A.及时分离出
 ,可以加快化学反应速率
,可以加快化学反应速率B.恒容时,充入He增大压强,化学反应速率不变
C.容器内压强不再变化,说明该反应已达到最大的限度
D.
 ,说明该反应已达到平衡状态
,说明该反应已达到平衡状态
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)在一定条件下,氢气在氯气中燃烧的热化学方程式:H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6kJ·mol-1;该反应属于___________ (填“热吸”或“放热”)反应。
(2)常温常压下,1mol乙醇(C2H5OH)完全燃烧生成CO2气体和液态水放出的热量为1367kJ,写出表示乙醇燃烧热的热化学方程式:___________ 。
(3)根据盖斯定律计算:
P4(白磷,s)+5O2(g)=P4O10(s) ΔH=-2983.2kJ·mol-1 ①
P(红磷,s)+ O2(g)=
O2(g)= P4O10(s) ΔH=-738.5kJ·mol-1 ②
P4O10(s) ΔH=-738.5kJ·mol-1 ②
则白磷转化为红磷的热化学方程式为___________ 。
(4)已知破坏1mol H−H键、1mol I−I键、1 mol H−I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由氢气和碘单质反应生成2 mol HI需要放出___________ kJ的热量。
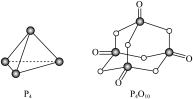
(5)白磷与氧可发生如下反应:P4+5O2=P4O10,已知断裂下列化学键需要吸收的能量分别为:P−P键 a kJ·mol-1、P−O键bkJ·mol-1、P=O键ckJ·mol-1、O=O键dkJ·mol-1。根据图示的分子结构和有关数据计算该反应的反应热为___________ 。
(1)在一定条件下,氢气在氯气中燃烧的热化学方程式:H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6kJ·mol-1;该反应属于
(2)常温常压下,1mol乙醇(C2H5OH)完全燃烧生成CO2气体和液态水放出的热量为1367kJ,写出表示乙醇燃烧热的热化学方程式:
(3)根据盖斯定律计算:
P4(白磷,s)+5O2(g)=P4O10(s) ΔH=-2983.2kJ·mol-1 ①
P(红磷,s)+
 O2(g)=
O2(g)= P4O10(s) ΔH=-738.5kJ·mol-1 ②
P4O10(s) ΔH=-738.5kJ·mol-1 ②则白磷转化为红磷的热化学方程式为
(4)已知破坏1mol H−H键、1mol I−I键、1 mol H−I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由氢气和碘单质反应生成2 mol HI需要放出
(5)白磷与氧可发生如下反应:P4+5O2=P4O10,已知断裂下列化学键需要吸收的能量分别为:P−P键 a kJ·mol-1、P−O键bkJ·mol-1、P=O键ckJ·mol-1、O=O键dkJ·mol-1。根据图示的分子结构和有关数据计算该反应的反应热为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】依据事实,写出下列反应的热化学方程式。
(1)N2(g)与H2(g)反应,生成1molNH3(g)时放出46.1kJ的热量:___________ 。
(2)2molN2(g)与2molO2(g)充分反应,生成NO(g)并吸收136kJ的热量:___________ 。
(3)卫星发射可用肼(N2H4)作燃料,2molN2H4(g)在足量O2(g)中燃烧,生成N2(g)和H2O(l)并放出1244kJ的热量:___________ 。
(4)已知N2(g)+2O2(g)=2NO2(g)ΔH=+67.7kJ·mol-1,N2H4(g)+O2(g)=N2(g)+2H2O(g)ΔH=—534kJ·mol-1,根据盖斯定律写出肼与NO2完全反应生成氮气和气态水的热化学方程式________ 。
(1)N2(g)与H2(g)反应,生成1molNH3(g)时放出46.1kJ的热量:
(2)2molN2(g)与2molO2(g)充分反应,生成NO(g)并吸收136kJ的热量:
(3)卫星发射可用肼(N2H4)作燃料,2molN2H4(g)在足量O2(g)中燃烧,生成N2(g)和H2O(l)并放出1244kJ的热量:
(4)已知N2(g)+2O2(g)=2NO2(g)ΔH=+67.7kJ·mol-1,N2H4(g)+O2(g)=N2(g)+2H2O(g)ΔH=—534kJ·mol-1,根据盖斯定律写出肼与NO2完全反应生成氮气和气态水的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求填空:
(1)已知化学方程式:H2(g)+ O2(g)=
O2(g)= H2O(g),该反应的活化能为167.2kJ/mol,其逆反应的活化能为409.0kJ/mol,写出该反应的热化学方程式:
H2O(g),该反应的活化能为167.2kJ/mol,其逆反应的活化能为409.0kJ/mol,写出该反应的热化学方程式:_____ 。
(2)常温常压下,1gCH4完全燃烧生成CO2和H2O时,放出QkJ的热量。写出此反应的热化学方程式:_____ 。
(3)已知2mol氢气燃烧生成液态水时放出572kJ的热量,反应方程式是2H2(g)+O2(g)=2H2O(l)。请回答下列问题:
①该反应的生成物能量总和_____ (填“大于”、“小于”或“等于”)反应物能量总和。
②若2mol氢气完全燃烧生成水蒸气,则放出的热量_____ (填“>”、<’或“=”1)572kJ。
(4)FeS2焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时:
2SO2(g)+O2(g) 2SO3(g) △H1=-197kJ•mol-1
2SO3(g) △H1=-197kJ•mol-1
H2O(g)=H2O(l) △H2=-44kJ•mol-1
2SO2(g)+O2(g)+2H2O(g) 2H2SO4(l) △H3=-545kJ•mol-1
2H2SO4(l) △H3=-545kJ•mol-1
则SO3(g)与H2O(l)反应的热化学方程式是____ 。
(1)已知化学方程式:H2(g)+
 O2(g)=
O2(g)= H2O(g),该反应的活化能为167.2kJ/mol,其逆反应的活化能为409.0kJ/mol,写出该反应的热化学方程式:
H2O(g),该反应的活化能为167.2kJ/mol,其逆反应的活化能为409.0kJ/mol,写出该反应的热化学方程式:(2)常温常压下,1gCH4完全燃烧生成CO2和H2O时,放出QkJ的热量。写出此反应的热化学方程式:
(3)已知2mol氢气燃烧生成液态水时放出572kJ的热量,反应方程式是2H2(g)+O2(g)=2H2O(l)。请回答下列问题:
①该反应的生成物能量总和
②若2mol氢气完全燃烧生成水蒸气,则放出的热量
(4)FeS2焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时:
2SO2(g)+O2(g)
 2SO3(g) △H1=-197kJ•mol-1
2SO3(g) △H1=-197kJ•mol-1H2O(g)=H2O(l) △H2=-44kJ•mol-1
2SO2(g)+O2(g)+2H2O(g)
 2H2SO4(l) △H3=-545kJ•mol-1
2H2SO4(l) △H3=-545kJ•mol-1则SO3(g)与H2O(l)反应的热化学方程式是
您最近一年使用:0次



