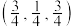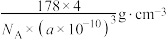下面的排序不正确的是
| A.沸点的高低:乙醇>丙烷 | B.硬度由大到小:金刚石>碳化硅>晶体硅 |
| C.熔点由高到低:Na>Mg>Al | D.第一电离能由大到小:F>N>O |
更新时间:2022-10-02 08:33:17
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.某微粒核外电子排布为2、8、8结构,则该微粒一定是氩原子 |
| B.最外层电子达稳定结构的微粒只能是稀有气体的原子 |
| C.F-、Na+、Mg2+、Al3+是与Ne原子具有相同电子层结构的离子 |
| D.NH4+与OH-具有相同的质子数和电子数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列四种元素中,其单质氧化性最强的是
| A.原子含有未成对电子最多的第2周期元素 |
| B.位于周期表第3周期ⅢA族的元素 |
| C.原子最外电子层排布式为3s23p5的元素 |
| D.原子最外电子层排布式为2s22p6的元素 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】离子键的强弱主要决定于离子半径和离子电荷值。一般规律是:离子半径越小,电荷值越大,则离子键越强。试分析:①K2O ②CaO ③MgO 的离子键由强到弱的顺序是
| A.①②③ | B.③①② | C.②①③ | D.③②① |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
| A.同一周期中,随着核电荷数的增加,元素的第一电离能逐渐增大 |
| B.基态原子21Sc电子排布式1s22s22p63s23p63d3违反了泡利原理 |
| C.二氯甲烷(CH2Cl2)分子的中心原子采取sp3杂化,键角均为109°28′ |
| D.ABn型分子的中心原子最外层满足8电子结构,而ABn不一定是非极性分子 |
您最近一年使用:0次

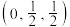 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。下列说法正确的是
。下列说法正确的是
 周围距离最近且相等的
周围距离最近且相等的 个数是6
个数是6