实验室需要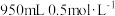 的稀硫酸和
的稀硫酸和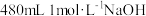 溶液进行实验,请你用98%的浓硫酸
溶液进行实验,请你用98%的浓硫酸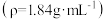 和
和 固体进行配制。回答下列问题:
固体进行配制。回答下列问题:
(1)配制稀硫酸时需要使用的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管、_______ (写仪器名称)。
(2)配制稀硫酸时,量取所需98%浓硫酸的体积,应选用下列量器中的_______(填字母)。
(3)要完成本实验应使用托盘天平准确称量
_______ g。
(4)对所配制的稀硫酸进行测定,发现其浓度为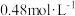 ,下列各项操作可能引起该误差的是
,下列各项操作可能引起该误差的是_______ (填字母)。
A.用量筒量取浓硫酸读数时仰视刻度线
B.转移稀释的硫酸后未洗涤烧杯和玻璃棒
C.浓硫酸稀释后未经冷却即转移到容量瓶中
D.转移前,容量瓶中含有少量蒸馏水
E.配制稀硫酸定容后摇匀溶液,发现液面低于刻度线,再加入少量水使液面与刻度线相平
(5)某同学在实验室配制 溶液的过程如图所示,其中有错误的操作是
溶液的过程如图所示,其中有错误的操作是_______ (填序号)。
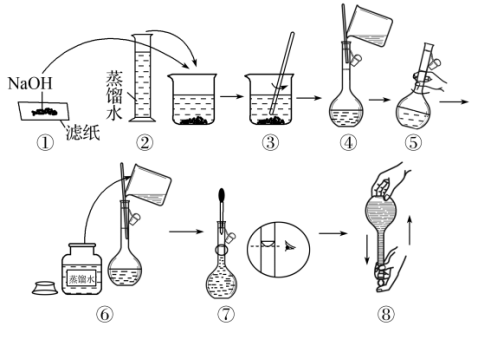
(6)下列对容量瓶及其使用方法描述正确的是_______ (填字母)。
A.容量瓶上标有容积,温度和浓度
B.容量瓶用蒸馏水洗净后必须烘干
C.容量瓶使用前需要检查是否漏水
D.容量瓶可以用来加热溶解固体溶质
E.容量瓶可以用来测量容量瓶规格以下的任意体积的溶液
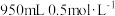 的稀硫酸和
的稀硫酸和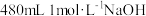 溶液进行实验,请你用98%的浓硫酸
溶液进行实验,请你用98%的浓硫酸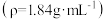 和
和 固体进行配制。回答下列问题:
固体进行配制。回答下列问题:(1)配制稀硫酸时需要使用的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管、
(2)配制稀硫酸时,量取所需98%浓硫酸的体积,应选用下列量器中的_______(填字母)。
A. 量筒 量筒 | B. 量筒 量筒 | C.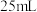 量筒 量筒 | D. 量筒 量筒 |

(4)对所配制的稀硫酸进行测定,发现其浓度为
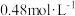 ,下列各项操作可能引起该误差的是
,下列各项操作可能引起该误差的是A.用量筒量取浓硫酸读数时仰视刻度线
B.转移稀释的硫酸后未洗涤烧杯和玻璃棒
C.浓硫酸稀释后未经冷却即转移到容量瓶中
D.转移前,容量瓶中含有少量蒸馏水
E.配制稀硫酸定容后摇匀溶液,发现液面低于刻度线,再加入少量水使液面与刻度线相平
(5)某同学在实验室配制
 溶液的过程如图所示,其中有错误的操作是
溶液的过程如图所示,其中有错误的操作是
(6)下列对容量瓶及其使用方法描述正确的是
A.容量瓶上标有容积,温度和浓度
B.容量瓶用蒸馏水洗净后必须烘干
C.容量瓶使用前需要检查是否漏水
D.容量瓶可以用来加热溶解固体溶质
E.容量瓶可以用来测量容量瓶规格以下的任意体积的溶液
更新时间:2022-10-14 12:09:26
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】化学是一门以实验为基础的自然科学,化学实验在化学学习中具有重要作用,请填写下列空白。
(一)可用于分离或提纯物质的方法有:a.过滤;b.结晶;c.蒸馏;d.加热;e.分液。
(1)请将相应分离提纯物质方法的序号填入空白处:
①除去澄清石灰水中悬浮的CaCO3颗粒:____ 。
②除去CaO中混有的CaCO3:____ 。
③分离酒精和水的混合物:____ 。
④分离水和CCl4的混合物:____ 。
⑤分离NaCl和KNO3的混合物:____ 。
(二)某学校实验室从化学试剂商店买回18.4mol•L-1的硫酸,现用该浓硫酸配制100mL1mol•L-1的稀硫酸。
(2)将下列实验步骤补充完整。
①用量筒量取____ mL的18.4mol•L-1的浓硫酸;
②将____ 沿烧杯内壁慢慢注入盛有少量____ 的烧杯中;
③将已冷却至室温的硫酸溶液沿玻璃棒注入____ mL的容量瓶中;
④用少量蒸馏水洗涤烧杯2~3次,并将洗涤液也全部转移到容量瓶中;
⑤继续向容量瓶中加蒸馏水,直至液面接近刻度线____ 处;
⑥改用____ 逐滴加蒸馏水,使溶液凹液面恰好与刻度线相切;
⑦盖好容量瓶塞,反复颠倒,摇匀;
⑧将配好的稀硫酸倒入试剂瓶中,贴好标签。
(3)由于操作不当,会引起实验误差。下列情况对所配制的H2SO4溶液的物质的量浓度有何影响?(用“偏大”“偏小”或“无影响”填写)
①用量筒量取浓硫酸时仰视读数____ 。
②摇匀后,发现溶液的液面低于刻度线,又加水至刻度线_____ 。
③溶解后的溶液未经冷却直接转移至容量瓶中_____ 。
④容量瓶用蒸馏水洗涤后残留有少量的水_____ 。
(一)可用于分离或提纯物质的方法有:a.过滤;b.结晶;c.蒸馏;d.加热;e.分液。
(1)请将相应分离提纯物质方法的序号填入空白处:
①除去澄清石灰水中悬浮的CaCO3颗粒:
②除去CaO中混有的CaCO3:
③分离酒精和水的混合物:
④分离水和CCl4的混合物:
⑤分离NaCl和KNO3的混合物:
(二)某学校实验室从化学试剂商店买回18.4mol•L-1的硫酸,现用该浓硫酸配制100mL1mol•L-1的稀硫酸。
(2)将下列实验步骤补充完整。
①用量筒量取
②将
③将已冷却至室温的硫酸溶液沿玻璃棒注入
④用少量蒸馏水洗涤烧杯2~3次,并将洗涤液也全部转移到容量瓶中;
⑤继续向容量瓶中加蒸馏水,直至液面接近刻度线
⑥改用
⑦盖好容量瓶塞,反复颠倒,摇匀;
⑧将配好的稀硫酸倒入试剂瓶中,贴好标签。
(3)由于操作不当,会引起实验误差。下列情况对所配制的H2SO4溶液的物质的量浓度有何影响?(用“偏大”“偏小”或“无影响”填写)
①用量筒量取浓硫酸时仰视读数
②摇匀后,发现溶液的液面低于刻度线,又加水至刻度线
③溶解后的溶液未经冷却直接转移至容量瓶中
④容量瓶用蒸馏水洗涤后残留有少量的水
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.新冠病毒主要通过人际传播,所以每个人都有可能成为防疫的破防口。疫情的一次次反扑,也一次次告诉我们,这场“战争”仍未取得胜利。因此,大家日常生活中还是要戴好口罩做好防范,尽早接种疫苗。“84消毒液”是一种常见的消毒液,可用于灭活新冠病毒,某品牌的“84消毒液”的主要成分为NaClO,浓度为4.0 mol/L,密度为1.2 g/mL。请回答下列问题:
(1)该“84消毒液”的质量分数为___________ (保留3位有效数字)。
(2)某同学欲用NaClO固体配制240 mL0.8 mol/L “84消毒液”。
①需要称量NaClO的质量为___________ g.
②下列操作会导致所得溶液浓度偏高的是___________ 。
A.用长时间放置在空气中的NaClO固体配制
B.配制前,容量瓶中有少量蒸馏水
C.定容时俯视容量瓶刻度线
Ⅱ.近年来,雾霾天气频繁发生,降低氮氧化物的排放,至关重要。
(3)三元催化剂能同时实现汽车尾气中的 、
、 、
、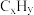 三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。
三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。

①X的化学式为___________ 。
②在图1的转化中,既有被氧化又有被还原的元素是___________ (填元素符号)。
(1)该“84消毒液”的质量分数为
(2)某同学欲用NaClO固体配制240 mL0.8 mol/L “84消毒液”。
①需要称量NaClO的质量为
②下列操作会导致所得溶液浓度偏高的是
A.用长时间放置在空气中的NaClO固体配制
B.配制前,容量瓶中有少量蒸馏水
C.定容时俯视容量瓶刻度线
Ⅱ.近年来,雾霾天气频繁发生,降低氮氧化物的排放,至关重要。
(3)三元催化剂能同时实现汽车尾气中的
 、
、 、
、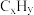 三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。
三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。
①X的化学式为
②在图1的转化中,既有被氧化又有被还原的元素是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】实验室需配制4.6 mol·L-1的H2SO4溶液0.5 L。
⑴ 需要浓度为18.4 mol·L-1的浓硫酸_______________ mL;
⑵ 需要用的玻璃仪器除玻璃棒、量筒外还有___________________________ ;
⑶ 配制过程中下列操作导致溶液浓度偏高的是____________________ 。
( A)移液时未充分洗涤烧杯和玻璃棒
( B)移液时未用玻璃棒引流而使少量液体外溢
( C)定容俯视刻度线
⑴ 需要浓度为18.4 mol·L-1的浓硫酸
⑵ 需要用的玻璃仪器除玻璃棒、量筒外还有
⑶ 配制过程中下列操作导致溶液浓度偏高的是
( A)移液时未充分洗涤烧杯和玻璃棒
( B)移液时未用玻璃棒引流而使少量液体外溢
( C)定容俯视刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室配制500mL0.1mol/LNa2CO3溶液,回答下列问题
(1)配制Na2CO3溶液时需用的主要仪器有托盘天平、滤纸、烧杯、药匙、___ 。
(2)容量瓶上标有刻度线、___ ,使用前要___ 。
(3)需用托盘天平称取Na2CO3____ g。
(4)若实验遇下列情况,溶液的浓度是偏高,偏低还是不变?
A.加水时超过刻度线___ ,
B.溶解后未冷却到室温就转入容量瓶___ ,
C.容量瓶内壁附有水珠而未干燥处理___ ,
D.定容时仰视___ ,
E.上下颠倒摇匀后液面低于刻线___ 。
(5)若实验室中要用浓度为16mol/L的浓硫酸配制480mL2.0mol/L的稀硫酸,则需要量取浓硫酸的体积为___ mL。
(1)配制Na2CO3溶液时需用的主要仪器有托盘天平、滤纸、烧杯、药匙、
(2)容量瓶上标有刻度线、
(3)需用托盘天平称取Na2CO3
(4)若实验遇下列情况,溶液的浓度是偏高,偏低还是不变?
A.加水时超过刻度线
B.溶解后未冷却到室温就转入容量瓶
C.容量瓶内壁附有水珠而未干燥处理
D.定容时仰视
E.上下颠倒摇匀后液面低于刻线
(5)若实验室中要用浓度为16mol/L的浓硫酸配制480mL2.0mol/L的稀硫酸,则需要量取浓硫酸的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】维生素C又名抗坏血酸,具有较强的还原性,分子式为C6H8O6,在医药和化学上有广泛应用。某研究性学习小组设计用2,6-二氯酚靛酚标准溶液测定油白菜样品中维生素C的含量。2,6-二氯酚靛酚钠盐(C12H6O2NCl2Na)呈蓝色,酸化后生成的氧化型2,6-二氯酚靛酚(C12H7O2NCl2)呈粉红色,被还原后变为无色的还原型2,6-二氯酚靛酚(C12H9O2NCl2)。
Ⅰ.配制2,6-二氯酚靛酚标准溶液
用2,6-二氯酚靛酚钠盐固体配制480mL0.010mol·L-12,6-二氯酚靛酚标准溶液的步骤如图所示:
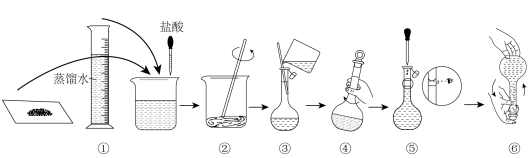
(1)在配制过程中必要的仪器有烧杯、玻璃棒、胶头滴管、电子天平和_______ ;检验操作④所用仪器是否漏水的操作是_______ 。
(2)经计算,需2,6-二氯酚靛酚钠盐固体的质量为_______ g。
(3)下列操作不会对所配标准溶液的浓度产生影响的是_______(填字母)。
Ⅱ.制备维生素C提取液
称取20g洗净的油白菜,向其中加入10mL酸化的蒸馏水(每10mL蒸馏水中加入10%盐酸1滴),用榨汁机榨成糊状,再用四层纱布过滤,反复抽提2~3次(纱布可用少量酸化的蒸馏水洗几次),合并滤液(滤液浑浊可离心分离),定容至50mL备用。
Ⅲ.测定维生素C的含量
取25.00mL维生素C提取液于锥形瓶中,加入5mL10%盐酸,再用0.010mol·L-1的2,6-二氯酚靛酚标准溶液滴定,反应原理可表示为:C6H8O6(抗坏血酸)+C12H7O2NCl2(氧化型2,6-二氯酚靛酚)→C6H6O6(脱氢抗坏血酸)+C12H9O2NCl2(还原型2,6-二氯酚靛酚)。滴定至终点时共消耗2,6-二氯酚靛酚标准溶液6.00mL。
(4)滴定时,根据_______ (填实验现象),即可确定滴定达到终点。
(5)该油白菜样品中维生素C的含量为_______ mg·100g-1。
Ⅰ.配制2,6-二氯酚靛酚标准溶液
用2,6-二氯酚靛酚钠盐固体配制480mL0.010mol·L-12,6-二氯酚靛酚标准溶液的步骤如图所示:

(1)在配制过程中必要的仪器有烧杯、玻璃棒、胶头滴管、电子天平和
(2)经计算,需2,6-二氯酚靛酚钠盐固体的质量为
(3)下列操作不会对所配标准溶液的浓度产生影响的是_______(填字母)。
| A.容量瓶用蒸馏水洗净,没有烘干 |
| B.操作③没有用蒸馏水洗涤烧杯2~3次,并转移洗涤液 |
| C.操作⑤仰视容量瓶的刻度线 |
| D.操作⑥后,发现液面略低于刻度线,再滴加蒸馏水定容并摇匀 |
Ⅱ.制备维生素C提取液
称取20g洗净的油白菜,向其中加入10mL酸化的蒸馏水(每10mL蒸馏水中加入10%盐酸1滴),用榨汁机榨成糊状,再用四层纱布过滤,反复抽提2~3次(纱布可用少量酸化的蒸馏水洗几次),合并滤液(滤液浑浊可离心分离),定容至50mL备用。
Ⅲ.测定维生素C的含量
取25.00mL维生素C提取液于锥形瓶中,加入5mL10%盐酸,再用0.010mol·L-1的2,6-二氯酚靛酚标准溶液滴定,反应原理可表示为:C6H8O6(抗坏血酸)+C12H7O2NCl2(氧化型2,6-二氯酚靛酚)→C6H6O6(脱氢抗坏血酸)+C12H9O2NCl2(还原型2,6-二氯酚靛酚)。滴定至终点时共消耗2,6-二氯酚靛酚标准溶液6.00mL。
(4)滴定时,根据
(5)该油白菜样品中维生素C的含量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】利用如图所示装置测定中和热的实验步骤如下:

①用量筒量取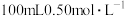 盐酸倒入小烧杯中,测出盐酸温度;
盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取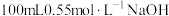 溶液,并用同一温度计测出其温度;
溶液,并用同一温度计测出其温度;
③将 和盐酸溶液一并倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。回答下列问题:
和盐酸溶液一并倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。回答下列问题:
(1)仪器a的名称是___________ 。烧杯间填满碎泡沫塑料的作用是___________ 。
(2)配制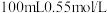 的氧氧化钠溶液,需要用到的仪器有托盘天平、烧杯、药匙、镊子、玻璃棒、量筒以及
的氧氧化钠溶液,需要用到的仪器有托盘天平、烧杯、药匙、镊子、玻璃棒、量筒以及___________ 。
(3)实验中改用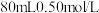 盐酸跟
盐酸跟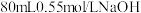 溶液进行反应,与上述实验相比,测得的中和热
溶液进行反应,与上述实验相比,测得的中和热___________ (填“相等”“不相等”)。用 溶液和硫酸代替上述试剂,所测中和热的数值
溶液和硫酸代替上述试剂,所测中和热的数值___________ 。(填“偏大”、“偏小”或“不变”)。
(4)倒入 和盐酸溶液的正确操作是___________(填字母)。
和盐酸溶液的正确操作是___________(填字母)。
(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和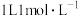 的稀盐酸恰好完全反应,其反应热分别为
的稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,其大小关系为
,其大小关系为___________ 。
(6)假设盐酸和氢氧化钠溶液的密度都是 ,又知中和反应后生成溶液的比热容
,又知中和反应后生成溶液的比热容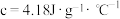 。为了计算中和热,某学生实验记录数据如下:
。为了计算中和热,某学生实验记录数据如下:
依据该学生的实验数据计算,该实验测得的中和热
___________ (结果保留一位小数)。

①用量筒量取
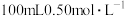 盐酸倒入小烧杯中,测出盐酸温度;
盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取
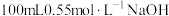 溶液,并用同一温度计测出其温度;
溶液,并用同一温度计测出其温度;③将
 和盐酸溶液一并倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。回答下列问题:
和盐酸溶液一并倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。回答下列问题:(1)仪器a的名称是
(2)配制
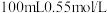 的氧氧化钠溶液,需要用到的仪器有托盘天平、烧杯、药匙、镊子、玻璃棒、量筒以及
的氧氧化钠溶液,需要用到的仪器有托盘天平、烧杯、药匙、镊子、玻璃棒、量筒以及(3)实验中改用
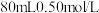 盐酸跟
盐酸跟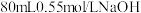 溶液进行反应,与上述实验相比,测得的中和热
溶液进行反应,与上述实验相比,测得的中和热 溶液和硫酸代替上述试剂,所测中和热的数值
溶液和硫酸代替上述试剂,所测中和热的数值(4)倒入
 和盐酸溶液的正确操作是___________(填字母)。
和盐酸溶液的正确操作是___________(填字母)。| A.沿玻璃棒缓僈倒入 | B.分三次倒入 |
| C.一次迅速倒入 | D.一边搅拌一边一次滴入 |
(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和
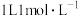 的稀盐酸恰好完全反应,其反应热分别为
的稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,其大小关系为
,其大小关系为(6)假设盐酸和氢氧化钠溶液的密度都是
 ,又知中和反应后生成溶液的比热容
,又知中和反应后生成溶液的比热容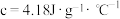 。为了计算中和热,某学生实验记录数据如下:
。为了计算中和热,某学生实验记录数据如下:| 实验序号 | 起始温度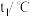 | 终止温度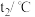 | |
| 盐酸 | 氢氧化钠溶液 | 混合溶液 | |
| 1 | 20.2 | 20.2 | 23.2 |
| 2 | 20.4 | 20.4 | 23.4 |
| 3 | 20.5 | 20.5 | 25.6 |

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验探究小组在实验中需要用到456mL1.00mol•L-1的HNO3溶液,但是在实验室中只发现一瓶8.00mol•L-1的HNO3溶液,该小组用8.00mol•L-1的HNO3溶液配制所需溶液。
(1)该实验中需要量取8.00mol•L-1的HNO3溶液__ mL。
(2)实验中所需的玻璃仪器包括玻璃棒、__ mL量筒、烧杯、__ 、胶头滴管等。
(3)下列实验操作中导致配制的溶液浓度偏高的是__ 。
A.取8.00mol•L-1的HNO3溶液溶液时仰视刻度线
B.量取用的量筒水洗后未进行任何操作
C.8.00mol•L-1的HNO3溶液从量筒转移至烧杯后用水洗涤量筒并全部转移至烧杯
D.定容时仰视刻度线
E.定容后,将容量瓶振荡摇匀后,发现液面低于刻度线,未进行任何操作
(1)该实验中需要量取8.00mol•L-1的HNO3溶液
(2)实验中所需的玻璃仪器包括玻璃棒、
(3)下列实验操作中导致配制的溶液浓度偏高的是
A.取8.00mol•L-1的HNO3溶液溶液时仰视刻度线
B.量取用的量筒水洗后未进行任何操作
C.8.00mol•L-1的HNO3溶液从量筒转移至烧杯后用水洗涤量筒并全部转移至烧杯
D.定容时仰视刻度线
E.定容后,将容量瓶振荡摇匀后,发现液面低于刻度线,未进行任何操作
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室需要0.3 mol/L NaOH溶液480 mL和1.0 mol/L硫酸溶液250 mL。根据这两种溶液的配制情况回答下列问题。
(1)如图所示的仪器中配制溶液肯定不需要的是________ (填序号),配制上述溶液还需用到的玻璃仪器是________ (填仪器名称)。

(2)下列操作中,容量瓶所不具备的功能有________ (填序号)。
A.配制一定体积准确浓度的标准溶液 B.贮存溶液 C.测量容量瓶规格以下的任意体积的液体 D.准确稀释某一浓度的溶液 E.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为________ g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度___ 0.3 mol/L(填“大于”“等于”或“小于”,下同)。
(4)根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为_______ mL(计算结果保留一位小数)。如果实验室有15 mL、20 mL、50 mL量筒,应选用________ mL的量筒最好。
(1)如图所示的仪器中配制溶液肯定不需要的是

(2)下列操作中,容量瓶所不具备的功能有
A.配制一定体积准确浓度的标准溶液 B.贮存溶液 C.测量容量瓶规格以下的任意体积的液体 D.准确稀释某一浓度的溶液 E.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为
(4)根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】实验室需要0.1 mol/L NaOH溶液450 mL,需要0.5 mol/L硫酸溶液500 mL.根据这两种溶液的配制情况回答下列问题:

(1)如图所示的仪器中配制溶液肯定不需要的是____ (填序号),配制上述溶液还需用到的玻璃仪器是____ (填仪器名称).
(2)根据计算用托盘天平称取NaOH的质量为____ g.
(3)根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为
___ mL(计算结果保留一位小数).如果实验室有15 mL、20 mL、50 mL量筒,应选用_____ mL的量筒最好.配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是___________ 。
(4)取用任意体积的所配0.5 mol/L硫酸溶液时,下列物理量中不随所取体积的多少而变化的是(填字母)_____
A.溶液中H2SO4的物质的量 B.溶液的浓度
C.溶液中SO42-的数目 D.溶液的密度
(5)将所配制的稀H2SO4进行测定,发现浓度大于0.5mol/L。请你分析下列哪些操作会引起所配浓度偏大(填写字母)_____________________________ 。
A.烧杯未进行洗涤
B.配制前,容量瓶中有少量蒸馏水
C.浓硫酸在烧杯中稀释后,未冷却就立即转移到容量瓶中,并进行定容;
D.往容量瓶转移时,有少量液体溅出
E.用量筒量取浓硫酸时,仰视量筒的刻度
F.在容量瓶中定容时俯视容量瓶刻度线
G.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线。

(1)如图所示的仪器中配制溶液肯定不需要的是
(2)根据计算用托盘天平称取NaOH的质量为
(3)根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为
(4)取用任意体积的所配0.5 mol/L硫酸溶液时,下列物理量中不随所取体积的多少而变化的是(填字母)
A.溶液中H2SO4的物质的量 B.溶液的浓度
C.溶液中SO42-的数目 D.溶液的密度
(5)将所配制的稀H2SO4进行测定,发现浓度大于0.5mol/L。请你分析下列哪些操作会引起所配浓度偏大(填写字母)
A.烧杯未进行洗涤
B.配制前,容量瓶中有少量蒸馏水
C.浓硫酸在烧杯中稀释后,未冷却就立即转移到容量瓶中,并进行定容;
D.往容量瓶转移时,有少量液体溅出
E.用量筒量取浓硫酸时,仰视量筒的刻度
F.在容量瓶中定容时俯视容量瓶刻度线
G.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线。
您最近一年使用:0次



