某学生做同主族元素性质递变规律的实验时,自己设计了一套实验方案,并记录了有关实验现象。请你帮助该学生整理并完成实验报告。
(1)实验目的:_______ 。
(2)实验用品:仪器:①_______ ;②_______ (请填写两种主要玻璃仪器)。
药品:氯水、溴水、溴化钠溶液、碘化钾溶液、四氯化碳。
(3)实验内容:
实验结论:_______ 。
(4)问题和讨论:
同一主族元素,自上而下,元素原子的电子层数增多,原子半径_______ ,原子核对最外层电子的吸引力逐渐_______ 。
(1)实验目的:
(2)实验用品:仪器:①
药品:氯水、溴水、溴化钠溶液、碘化钾溶液、四氯化碳。
(3)实验内容:
| 序号 | 实验方案 | 实验现象 |
| ① | 将少量氯水滴入盛有少量NaBr溶液的试管中,振荡; | 加入氯水后,溶液由无色变为橙色 |
| ② | 将少量溴水滴入盛有少量KI溶液的试管中,振荡; | 加入溴水后,溶液由无色变为褐色 |
(4)问题和讨论:
同一主族元素,自上而下,元素原子的电子层数增多,原子半径
2022高一·全国·专题练习 查看更多[1]
(已下线)2.3.1 卤素单质的性质-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)
更新时间:2022-10-17 14:36:05
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】根据短周期元素的信息回答问题。
(1)写出A、B的元素符号____________ 、_________ ,C、D的元素的名称__________ 、_____________ 。
(2)写出B、C单质在加热时反应的方程式____________________________________
(3)从原子结构角度分析A与B的______________ 相同,C与D的_______________ 相同。
| 元素信息 | |
| A | 第3周期第ⅥA族 |
| B | 族序数是周期数的3倍 |
| C | 原子序数是11 |
| D | D3+与Ne电子数相同 |
(1)写出A、B的元素符号
(2)写出B、C单质在加热时反应的方程式
(3)从原子结构角度分析A与B的
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】联合国大会将2019年定为“化学元素周期表国际年”,显示了元素周期表的重要性。表中列出了部分元素在周期表中的位置:

回答下列问题:
(1)元素a~k中非金属性最强的是____ (填元素符号),b与g的原子核电荷数相差____ (填数值)。
(2)e、f、j三种元素最高价氧化物对应的水化物的碱性由强到弱依次为____ (填化学式)。
(3)设计一个实验方案,比较h、k单质氧化性的强弱____ 。
(4)金属镓(Ga)常用作光学玻璃、真空管、半导体的原料。
①预测Ga的化学性质并填写表格:
以上预测都是依据____ 。
②氮化镓(CaN)材料的研究与应用是目前全球半导体研究的前沿和热点。工业上用含铁酸镓Ga2(Fe2O4)3矿渣经过硫酸浸出获得2种金属盐,进一步利用镓盐可制备具有优异光电性能的CaN。写出Ga2(Fe2O4)3用硫酸浸出时发生反应的离子方程式为____ 。

回答下列问题:
(1)元素a~k中非金属性最强的是
(2)e、f、j三种元素最高价氧化物对应的水化物的碱性由强到弱依次为
(3)设计一个实验方案,比较h、k单质氧化性的强弱
(4)金属镓(Ga)常用作光学玻璃、真空管、半导体的原料。
①预测Ga的化学性质并填写表格:
| 预测性质(所填物质类别不同) | 反应后可能的生成物(填化学式) |
| Ga能与 | |
| Ga能与 | Ga2(SO4)3、 |
| Ga能与NaOH溶液反应 |
②氮化镓(CaN)材料的研究与应用是目前全球半导体研究的前沿和热点。工业上用含铁酸镓Ga2(Fe2O4)3矿渣经过硫酸浸出获得2种金属盐,进一步利用镓盐可制备具有优异光电性能的CaN。写出Ga2(Fe2O4)3用硫酸浸出时发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】元素周期表在学习、研究和生产实践中有很重要的作用。下表显示了元素周期表中的短周期,①~⑤代表5种元素。
(1)②在元素周期表中的位置是___________ 。
(2)①分别与④、⑤形成的化合物中,稳定性强的是___________ (用化学式表示)。
(3)③和④分别形成的最高价氧化物对应的水化物可以发生反应,离子方程式是___________ 。
(4)用原子结构解释④和⑤非金属性强弱的原因:___________ 。
(5)元素硒(Se)的原子结构示意图为 。下列推断正确的是___________(填字母)。
。下列推断正确的是___________(填字母)。
| ① | ||||||||
| ② | ||||||||
| ③ | ④ | ⑤ | ||||||
(2)①分别与④、⑤形成的化合物中,稳定性强的是
(3)③和④分别形成的最高价氧化物对应的水化物可以发生反应,离子方程式是
(4)用原子结构解释④和⑤非金属性强弱的原因:
(5)元素硒(Se)的原子结构示意图为
 。下列推断正确的是___________(填字母)。
。下列推断正确的是___________(填字母)。| A.Se位于第4周期、与④同主族 | B.Se的最低负化合价为 |
C. 具有还原性 具有还原性 | D. 的酸性强于 的酸性强于 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】Ⅰ.某实验小组同学进行如下实验,以检验化学反应中的能量变化。请回答下列问题:

(1)实验中发现,反应后①中的温度升高;②中的温度降低。由此判断Ba(OH)2•8H2O与NH4Cl的反应是_______ (填“放热反应”或“吸热反应”),反应过程_______ 的能量变化可用图2表示(填“①”或“②”)。
(2)现有如下两个反应:A、NaOH+HCl=NaCl+H2O;B、2FeCl3+Cu=2FeCl2+CuCl2,以上两个反应能设计成原电池的是_______ ,负极材料为:_______ ,电解质溶液为:_______ ,负极的电极反应式为:_______ 。
Ⅱ.某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。利用如图装置可验证同主族元素非金属性的变化规律

(3)干燥管D的作用为_______ 。
(4)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液_______ (填现象)即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用NaOH溶液吸收尾气。
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中可加_______ 溶液,观察到C中溶液_______ (填现象),即可证明,反应的离子方程式为:_______ ,但有的同学认为该实验不严谨,应在两装置间添加装有_______ 溶液的洗气瓶,目的是_______ 。

(1)实验中发现,反应后①中的温度升高;②中的温度降低。由此判断Ba(OH)2•8H2O与NH4Cl的反应是
(2)现有如下两个反应:A、NaOH+HCl=NaCl+H2O;B、2FeCl3+Cu=2FeCl2+CuCl2,以上两个反应能设计成原电池的是
Ⅱ.某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。利用如图装置可验证同主族元素非金属性的变化规律

(3)干燥管D的作用为
(4)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中可加
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】某研究性学习小组设计了一组实验来探究元素周期律。
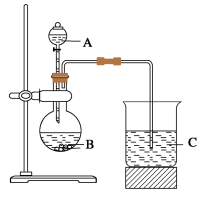
甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成S、C、Si三种元素的非金属性强弱比较的实验研究。
(1)图中仪器A的名称是____ 。
(2)甲同学实验步骤:连接仪器、______ 、加药品、滴入试剂。
(3)①图中仪器A中盛放试剂为硫酸,C中的盛放试剂为_______ 溶液。
②能说明碳元素的非金属性比硅元素强的实验现象是___

甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成S、C、Si三种元素的非金属性强弱比较的实验研究。
(1)图中仪器A的名称是
(2)甲同学实验步骤:连接仪器、
(3)①图中仪器A中盛放试剂为硫酸,C中的盛放试剂为
②能说明碳元素的非金属性比硅元素强的实验现象是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】Ⅰ.下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1) 装置C中①的名称是____________ ,冷却水的方向是____________ 。
(2) 从氯化钠溶液中得到氯化钠固体,选择装置______ (填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置________ ,检验自来水中Cl-是否除净的方法为:取少量锥形瓶中的水于洁净试管中,滴加_________ 溶液,不产生白色沉淀表明Cl-已除净。
Ⅱ.从某同学想通过实验探究硫和碳得电子能力的强弱,通过比较它们最高价氧化物对应水化物的酸性强弱来验证,设计了如图实验,请回答:

(1) 仪器a的名称是__________ ,应盛放下列药品中的__________ (填字母);
A.稀硫酸 B.亚硫酸 C.氢硫酸 D.盐酸
(2) 仪器b的名称是__________ ,应盛放下列药品中的__________ (填字母);
A.碳酸钙 B.硫酸钠 C.氯化钠 D.碳酸钠
(3) 仪器c中应盛放的药品是__________ ,如果看到的现象是__________ ,证明b中反应产生了__________ ,即可证明_______ 比_________ 酸性强,得电子能力________ 比________ 强。

(1) 装置C中①的名称是
(2) 从氯化钠溶液中得到氯化钠固体,选择装置
Ⅱ.从某同学想通过实验探究硫和碳得电子能力的强弱,通过比较它们最高价氧化物对应水化物的酸性强弱来验证,设计了如图实验,请回答:

(1) 仪器a的名称是
A.稀硫酸 B.亚硫酸 C.氢硫酸 D.盐酸
(2) 仪器b的名称是
A.碳酸钙 B.硫酸钠 C.氯化钠 D.碳酸钠
(3) 仪器c中应盛放的药品是
您最近一年使用:0次



