回答下列问题:
(1)①写出 Cl-的结构示意图_______ ;
②写出 NaHSO4 在水溶液中的电离方程式_______ 。
(2)写出电解饱和食盐水的离子方程式_______ ; 写出镁与 CO2 反应的化学方程式_______ 。
(3)已知阴离子 R2﹣的原子核内有 n 个中子,R 原子的质量数为 m,则 w 克 R2-所含有电子的物质的量是_______ 。
(1)①写出 Cl-的结构示意图
②写出 NaHSO4 在水溶液中的电离方程式
(2)写出电解饱和食盐水的离子方程式
(3)已知阴离子 R2﹣的原子核内有 n 个中子,R 原子的质量数为 m,则 w 克 R2-所含有电子的物质的量是
更新时间:2022/10/23 11:19:13
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分
(1)写出元素符号: B.________ C______ 、D________ 、E_______ ;
(2)D- 离子结构示意图___________ ,B+ 离子结构示意图______________ ,
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
1 | ||||||||
2 | D | |||||||
3 | B | C | E | |||||
4 | A |
(1)写出元素符号: B.
(2)D- 离子结构示意图
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】磷的单质及其化合物用途非常广泛。完成下列填空:
(1)画出磷的原子结构示意图________ 。
(2)磷酸钙真空制磷的反应为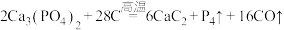 。该反应的氧化产物是
。该反应的氧化产物是________ (填化学式); 中的共价键的类型为
中的共价键的类型为________ 。
(3)次磷酸钠的结构为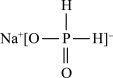 。
。
①次磷酸钠的化学式为________ ,磷的化合价为________ 。
②次磷酸钠为________ 盐(填“正”“酸式”)。
(1)画出磷的原子结构示意图
(2)磷酸钙真空制磷的反应为
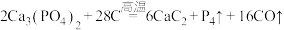 。该反应的氧化产物是
。该反应的氧化产物是 中的共价键的类型为
中的共价键的类型为(3)次磷酸钠的结构为
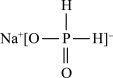 。
。①次磷酸钠的化学式为
②次磷酸钠为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求写出方程式。
其中1、2写离子方程式;3、4写水溶液中的电离方程式;5、6写一个对应的化学方程式
(1)碳酸钙和盐酸_______________________________
(2)氢氧化钡溶液和稀硫酸_______________________________
(3)NaHSO4_______________________________
(4)KClO3_______________________________
(5)H + + OH — = H2O_______________________________
(6)CO32 —+2H + =CO2↑+H2O_______________________________
其中1、2写离子方程式;3、4写水溶液中的电离方程式;5、6写一个对应的化学方程式
(1)碳酸钙和盐酸
(2)氢氧化钡溶液和稀硫酸
(3)NaHSO4
(4)KClO3
(5)H + + OH — = H2O
(6)CO32 —+2H + =CO2↑+H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】有以下10种物质,请回答下列问题:①干冰②KNO3③蔗糖④稀硫酸⑤NaHSO4溶液⑥碳酸氢钠⑦氢氧化钡溶液⑧冰醋酸(CH3COOH)⑨氯化氢⑩N2
(1)其中能导电的是___________ (填写编号,下同);属于电解质的是___________ ;属于非电解质的是___________ 。
(2)写出物质④在水中的电离方程式:___________ 。
(3)写出物质④和⑦反应的离子方程式:___________ 。
(4)写出物质⑤和⑥在水中发生反应的离子方程式:___________ 。
(1)其中能导电的是
(2)写出物质④在水中的电离方程式:
(3)写出物质④和⑦反应的离子方程式:
(4)写出物质⑤和⑥在水中发生反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】对物质进行分类,有利于更好的研究和认识物质。完成下列问题
(1)有下列物质:①H2O;②空气;③Mg;④CaO;⑤H2SO4;⑥Ca(OH)2;⑦碘酒;⑧NaHCO3,其中属于混合物的是___________ (填序号,下同);属于盐的是___________ 。
(2)以下为中学化学中常见的几种物质:①CO2;②熔融KCl;③NaHSO4固体;④铜;⑤稀硫酸;⑥澄清石灰水;⑦C2H5OH,其中属于电解质的有___________ (填序号,下同);属于非电解质的有___________ ;能导电的有___________ 。
(3)按要求写出相关方程式:
①Fe2(SO4)3的电离方程式:___________
②将NaHSO4与Ba(OH)2在溶液中按1:1的分子数之比混合发生反应,其离子方程式:___________
③过氧化钠与水反应的化学方程式:___________ 。
(1)有下列物质:①H2O;②空气;③Mg;④CaO;⑤H2SO4;⑥Ca(OH)2;⑦碘酒;⑧NaHCO3,其中属于混合物的是
(2)以下为中学化学中常见的几种物质:①CO2;②熔融KCl;③NaHSO4固体;④铜;⑤稀硫酸;⑥澄清石灰水;⑦C2H5OH,其中属于电解质的有
(3)按要求写出相关方程式:
①Fe2(SO4)3的电离方程式:
②将NaHSO4与Ba(OH)2在溶液中按1:1的分子数之比混合发生反应,其离子方程式:
③过氧化钠与水反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】工业上电解制碱的技术是用离子交换膜法,主要原料是饱和食盐水。下图为离子交换膜法电解原理示意图:
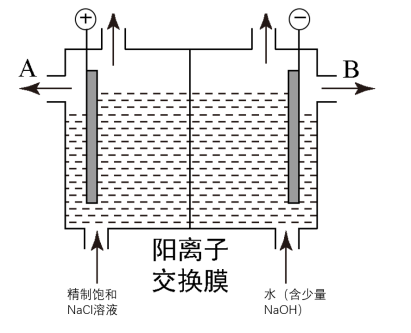
请回答下列问题:
(1)A极为电解槽的_______ 极(正、负、阴、阳),电极反应式为_______ 。
(2)电解槽中部的阳离子交换膜把电解槽隔成了阴极室和阳极室,它只允许_______ (填离子符号,下同)通过,而不允许_______ 和气体通过。
(3)电解法制碱的主要原料饱和食盐水是由粗盐制得,其中含有泥沙及 、
、 、
、 、
、 等杂质,因此必须精制。精制时所用试剂为①
等杂质,因此必须精制。精制时所用试剂为① ②
② ③
③ ④盐酸,这四种试剂的添加顺序为
④盐酸,这四种试剂的添加顺序为_______ (填序号)。
(4)若将标准状况下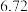 L阳极气体通入热的氢氧化钠溶液中,反应中只有一种元素的化合价发生改变,电子转移数是
L阳极气体通入热的氢氧化钠溶液中,反应中只有一种元素的化合价发生改变,电子转移数是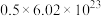 ,产物中得到了两种含氯化合物,写出该反应的离子方程式:
,产物中得到了两种含氯化合物,写出该反应的离子方程式:_______ 。

请回答下列问题:
(1)A极为电解槽的
(2)电解槽中部的阳离子交换膜把电解槽隔成了阴极室和阳极室,它只允许
(3)电解法制碱的主要原料饱和食盐水是由粗盐制得,其中含有泥沙及
 、
、 、
、 、
、 等杂质,因此必须精制。精制时所用试剂为①
等杂质,因此必须精制。精制时所用试剂为① ②
② ③
③ ④盐酸,这四种试剂的添加顺序为
④盐酸,这四种试剂的添加顺序为(4)若将标准状况下
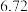 L阳极气体通入热的氢氧化钠溶液中,反应中只有一种元素的化合价发生改变,电子转移数是
L阳极气体通入热的氢氧化钠溶液中,反应中只有一种元素的化合价发生改变,电子转移数是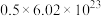 ,产物中得到了两种含氯化合物,写出该反应的离子方程式:
,产物中得到了两种含氯化合物,写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】工业上利用电解饱和食盐水可制得重要化工产品。
(1)反应化学方程式为:___ 。
(2)电解饱和食盐水时,___ 极区附近溶液pH变大。
(3)取阴极区溶液作系列实验,下列结论中错误的是___ 。(填字母)
A.滴加石蕊试剂,溶液呈红色
B.滴加氯化镁溶液,有白色沉淀产生
C.加入石灰石,有气泡产生
D.先加足量硝酸,再滴加硝酸银溶液,若产生沉淀说明溶液中含有氯离子
(4)电解饱和食盐水一段时间后,想要让溶液恢复电解前的状态,应往溶液中加入(或通入)一定量的___ (填字母)。
A.NaCl固体 B.NaCl溶液 C.HCl气体 D.盐酸
(1)反应化学方程式为:
(2)电解饱和食盐水时,
(3)取阴极区溶液作系列实验,下列结论中错误的是
A.滴加石蕊试剂,溶液呈红色
B.滴加氯化镁溶液,有白色沉淀产生
C.加入石灰石,有气泡产生
D.先加足量硝酸,再滴加硝酸银溶液,若产生沉淀说明溶液中含有氯离子
(4)电解饱和食盐水一段时间后,想要让溶液恢复电解前的状态,应往溶液中加入(或通入)一定量的
A.NaCl固体 B.NaCl溶液 C.HCl气体 D.盐酸
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氢氧化钠是白色固体,易潮解,具有强腐蚀性,所以又叫火碱、烧碱、苛性钠。是常用的碱性干燥剂,是重要的化工原料。
工业制法:氯碱工业2NaCl+2H2O Cl2↑+H2↑+2NaOH
Cl2↑+H2↑+2NaOH
苛化法:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
在实验室,钠、氧化钠(Na2O)、过氧化钠(Na2O2)分别与水反应都生成NaOH。回答下列问题:
(1)在“氯碱工业”反应中,反应前后氯元素的化合价变化是____ (填“升高”、“降低”、“不变”)。
(2)Ca(OH)2可拆写,苛化法的离子方程式为____ 。
(3)写出Na2O与水反应的化学方程式____ 。
(4)补项:过氧化钠与水反应为:2Na2O2+2H2O=4NaOH+____ ↑。
(5)NaOH固体不能干燥酸性气体。能用NaOH固体干燥的气体是____ (填序号)。
a.HCl b.H2 c.NH3(碱性气体) d.CO2
工业制法:氯碱工业2NaCl+2H2O
 Cl2↑+H2↑+2NaOH
Cl2↑+H2↑+2NaOH苛化法:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
在实验室,钠、氧化钠(Na2O)、过氧化钠(Na2O2)分别与水反应都生成NaOH。回答下列问题:
(1)在“氯碱工业”反应中,反应前后氯元素的化合价变化是
(2)Ca(OH)2可拆写,苛化法的离子方程式为
(3)写出Na2O与水反应的化学方程式
(4)补项:过氧化钠与水反应为:2Na2O2+2H2O=4NaOH+
(5)NaOH固体不能干燥酸性气体。能用NaOH固体干燥的气体是
a.HCl b.H2 c.NH3(碱性气体) d.CO2
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题
Ⅰ.图是部分元素原子或离子的结构示意图。请你仔细观察、分析,然后回答问题:
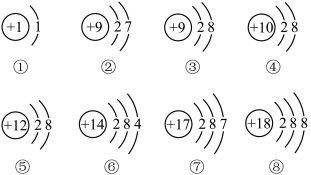
(1)用序号填空:上述粒子中,属于稀有气体元素的原子是_______ ;在化学反应中容易得到电子的是_______ ;属于阳离子的是_______ ;表示F-的是_______ ;属于同一种元素的是_______ ;属于非金属元素的是_______ ;电子层数相同,最外层电子数也相同的粒子有_______ 。
Ⅱ.某微粒的结构示意图可表示为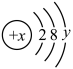 。
。
(2)当x=10+y时,该粒子为_______ (填“原子”“阳离子”或“阴离子”),当x<10+y时,该粒子为_______ 。
(3)当y=2时,x=_______ 。该元素能形成的离子符号为_______ 。
(4)若该结构示意图表示的粒子是R-,则x=_______ ,y=_______ 。
Ⅰ.图是部分元素原子或离子的结构示意图。请你仔细观察、分析,然后回答问题:

(1)用序号填空:上述粒子中,属于稀有气体元素的原子是
Ⅱ.某微粒的结构示意图可表示为
 。
。(2)当x=10+y时,该粒子为
(3)当y=2时,x=
(4)若该结构示意图表示的粒子是R-,则x=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求用合适的化学用语回答下列问题:
(1)写出含有8个质子、10个中子的原子化学符号___________ 。
(2)相同质量的D2O和H2O中质子数之比是___________ 。
(3)第ⅦA族上下相邻的两种元素X、Y(X在上),X元素所在周期含m,Y元素所在周期含n种元素,若X的原子序数为x,则Y的原子序数为___________ 。
(4)金属Li与氧气加热生成物质的化学式___________ 。
(5)向NaHSO4溶液中滴加Ba(OH)2溶液至溶液呈中性的离子方程式:___________ 。
(6)“洁厕灵”和“84消毒液”混合发生氯气中毒的离子方程式:___________ 。
(7)标况下,VL NH3溶于1L水中所形成的氨水的密度为dg/cm3,该溶液的物质的量浓度为___________ 。
(8)—种固体管道疏通剂的主要成分是NaOH和Al粉,试解释其疏通原理(用化学方程式回答):___________ 。
(1)写出含有8个质子、10个中子的原子化学符号
(2)相同质量的D2O和H2O中质子数之比是
(3)第ⅦA族上下相邻的两种元素X、Y(X在上),X元素所在周期含m,Y元素所在周期含n种元素,若X的原子序数为x,则Y的原子序数为
(4)金属Li与氧气加热生成物质的化学式
(5)向NaHSO4溶液中滴加Ba(OH)2溶液至溶液呈中性的离子方程式:
(6)“洁厕灵”和“84消毒液”混合发生氯气中毒的离子方程式:
(7)标况下,VL NH3溶于1L水中所形成的氨水的密度为dg/cm3,该溶液的物质的量浓度为
(8)—种固体管道疏通剂的主要成分是NaOH和Al粉,试解释其疏通原理(用化学方程式回答):
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】填写下列空白:
(1)写出表示含有8个质子、10个中子的原子的化学符号:_______ 。
(2)原子符号为 X的元素属于第
X的元素属于第_______ 周期_______ 族。
(3)周期表中位于第8纵列的铁元素属于第_______ 族。
(4)周期表中第三周期最活泼的金属元素是_______ 。
(5)已知某微粒的结构示意图为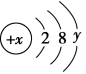 ,试回答下列问题:
,试回答下列问题:
①当x-y=10时,该微粒为_______ (填“原子”“阳离子”或“阴离子”)。
②当y=6时,元素最高价氧化物对应水化物的化学式为_______ 。
(1)写出表示含有8个质子、10个中子的原子的化学符号:
(2)原子符号为
 X的元素属于第
X的元素属于第(3)周期表中位于第8纵列的铁元素属于第
(4)周期表中第三周期最活泼的金属元素是
(5)已知某微粒的结构示意图为
 ,试回答下列问题:
,试回答下列问题:①当x-y=10时,该微粒为
②当y=6时,元素最高价氧化物对应水化物的化学式为
您最近一年使用:0次

 结构示意图:
结构示意图: );④熔融的
);④熔融的 ;⑤
;⑤ 固体;⑥液氨;⑦冰醋酸;⑧石墨。其中,属于电解质且能导电的是
固体;⑥液氨;⑦冰醋酸;⑧石墨。其中,属于电解质且能导电的是 的化学性质和卤素(
的化学性质和卤素( ,如
,如 )很相似,化学上称为拟卤素,试写出
)很相似,化学上称为拟卤素,试写出

