按要求用合适的化学用语回答下列问题:
(1)写出含有8个质子、10个中子的原子化学符号___________ 。
(2)相同质量的D2O和H2O中质子数之比是___________ 。
(3)第ⅦA族上下相邻的两种元素X、Y(X在上),X元素所在周期含m,Y元素所在周期含n种元素,若X的原子序数为x,则Y的原子序数为___________ 。
(4)金属Li与氧气加热生成物质的化学式___________ 。
(5)向NaHSO4溶液中滴加Ba(OH)2溶液至溶液呈中性的离子方程式:___________ 。
(6)“洁厕灵”和“84消毒液”混合发生氯气中毒的离子方程式:___________ 。
(7)标况下,VL NH3溶于1L水中所形成的氨水的密度为dg/cm3,该溶液的物质的量浓度为___________ 。
(8)—种固体管道疏通剂的主要成分是NaOH和Al粉,试解释其疏通原理(用化学方程式回答):___________ 。
(1)写出含有8个质子、10个中子的原子化学符号
(2)相同质量的D2O和H2O中质子数之比是
(3)第ⅦA族上下相邻的两种元素X、Y(X在上),X元素所在周期含m,Y元素所在周期含n种元素,若X的原子序数为x,则Y的原子序数为
(4)金属Li与氧气加热生成物质的化学式
(5)向NaHSO4溶液中滴加Ba(OH)2溶液至溶液呈中性的离子方程式:
(6)“洁厕灵”和“84消毒液”混合发生氯气中毒的离子方程式:
(7)标况下,VL NH3溶于1L水中所形成的氨水的密度为dg/cm3,该溶液的物质的量浓度为
(8)—种固体管道疏通剂的主要成分是NaOH和Al粉,试解释其疏通原理(用化学方程式回答):
20-21高一上·江苏南京·阶段练习 查看更多[2]
(已下线)专题八 原子结构与元素周期表(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)江苏省南京市金陵中学2020-2021学年高一上化学12月月考化学试题
更新时间:2021-12-10 11:10:10
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(1)实验室欲用NaOH固体配制1.0mol·L-1的NaOH溶液240mL:配制溶液时,一般可以分为以下几个步骤:①称量②计算③定容④溶解⑤转移⑥洗涤其正确的操作顺序为__ 。
(2)将40gNaOH配成2L溶液,其物质的量浓度为__ mol/L。
(3)FeCl3溶液中有少量的FeCl2杂质:除杂时发生的离子方程式__ 。
(4)钠投入水中发生反应的方程式___ 。如将2.3g钠投入水中,充分反应生成的NaOH的物质的量为___ mol,生成氢气的体积标准状况下为___ L,该反应的氧化剂是___ 。
(2)将40gNaOH配成2L溶液,其物质的量浓度为
(3)FeCl3溶液中有少量的FeCl2杂质:除杂时发生的离子方程式
(4)钠投入水中发生反应的方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】实验室要用CuSO4·5H2O晶体配制500 mL 0.1 mol·L-1 CuSO4溶液,回答下列问题:
(1)应该用托盘天平称取CuSO4·5H2O________ g。
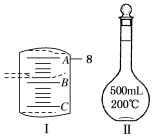
(2)如图Ⅰ表示10 mL量筒中液面的位置,A与B,B与C刻度间相差1 mL,如果刻度A为8,量筒中液体的体积是________ mL。
(3)若实验中如图Ⅱ所示的仪器有下列情况,对配制溶液的浓度有何影响?(填“偏高”“偏低”或“无影响”)
A.定容前容量瓶底部有水珠__________________________ ;
B.定容时加水超过刻度线____________________________ ;
C.最终定容时俯视观察液面__________________________ 。

(1)应该用托盘天平称取CuSO4·5H2O
(2)如图Ⅰ表示10 mL量筒中液面的位置,A与B,B与C刻度间相差1 mL,如果刻度A为8,量筒中液体的体积是
(3)若实验中如图Ⅱ所示的仪器有下列情况,对配制溶液的浓度有何影响?(填“偏高”“偏低”或“无影响”)
A.定容前容量瓶底部有水珠
B.定容时加水超过刻度线
C.最终定容时俯视观察液面
您最近一年使用:0次
【推荐1】Ⅰ.某些简单原子的原子结构可用如图形象地表示:
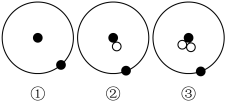
其中“●”表示质子或电子,“○”表示中子
(1)下列有关叙述正确的是_______ (填序号)。
(2)科学家已经发现一种新型氢分子,其化学式为H3,在相同条件下,等质量的H3和H2具有相同的_______ (填序号)。
Ⅱ.硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。请回答下列问题:
(3)Si元素位于元素周期表_______ ,在SiO2中,硅原子和氧原子以_______ (选填“极性共价键”、“非极性共价键”、“离子键”)连接形成立体网状结构,所以SiO2硬度大。
(4)国家速滑馆用到建筑黏合剂和防火剂硅酸钠,硅酸钠可由SiO2溶解在NaOH溶液中反应来制备,反应的离子方程式为_______ 。
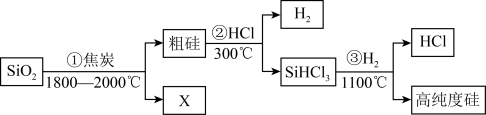
(5)由SiO2制备高纯度硅的工业流程如图所示,X为_______ ,可以循环使用的物质为_______ 和______ 。

其中“●”表示质子或电子,“○”表示中子
(1)下列有关叙述正确的是
| A.①②③是不同元素的原子 | B.①②③是三种化学性质不同的粒子 |
| C.①②③互为同位素 | D.①②③具有相同的质量数 |
| A.原子数 | B.分子数 | C.体积 | D.电子数 |
Ⅱ.硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。请回答下列问题:
(3)Si元素位于元素周期表
(4)国家速滑馆用到建筑黏合剂和防火剂硅酸钠,硅酸钠可由SiO2溶解在NaOH溶液中反应来制备,反应的离子方程式为
(5)由SiO2制备高纯度硅的工业流程如图所示,X为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列问题
(1)将Na2SO3溶液蒸干灼烧得到的物质是_______ (填化学式)。
(2)已知部分弱酸的电离常数如下表:(均为常温下的数据):
①同浓度的A-、B-、HC-、D-中结合H+的能力最强的是_______ 。
②pH相同的①NaA、②NaB、③NaD溶液,其物质的量浓度由大到小的顺序为_______ 。(填序号)
③25℃时,向NaD溶液中通入少量H2C,反应的离子方程式为_______ 。
④将浓度为0.02mol/L的HA与0.01mol/LNaOH溶液等体积混合,测得混合溶液中c(Na+)<c(A-),则c(H+)_______ c(OH-)(填“>”、“<”、“=”)
⑤下列反应不能发生的是:_______ (填编号)。
A.HA+NaB=HB+NaA B.HB+NaD=HD+NaB
C.H2C+NaB=HB+NaHC D.HD+A-=HA+D-
(1)将Na2SO3溶液蒸干灼烧得到的物质是
(2)已知部分弱酸的电离常数如下表:(均为常温下的数据):
| 酸 | 电离常数(Ka) |
| HA | 1.8×10-5 |
| HB | 3×10-8 |
| H2C | K1=4.4×10-7 K2=4.7×10-11 |
| HD | 6.2×10-10 |
②pH相同的①NaA、②NaB、③NaD溶液,其物质的量浓度由大到小的顺序为
③25℃时,向NaD溶液中通入少量H2C,反应的离子方程式为
④将浓度为0.02mol/L的HA与0.01mol/LNaOH溶液等体积混合,测得混合溶液中c(Na+)<c(A-),则c(H+)
⑤下列反应不能发生的是:
A.HA+NaB=HB+NaA B.HB+NaD=HD+NaB
C.H2C+NaB=HB+NaHC D.HD+A-=HA+D-
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】84消毒液、ClO2是常见的含氯消毒剂。
资料:84消毒液中含氟微粒主要有ClO-、Cl-、HClO;相同浓度时,HClO的氧化性强于ClO-;ORP是反映物质的氧化一还原性,ORP值越大,氧化性越强。通常情况下,应将84消毒液原液稀释后使用;一般不用于衣服等纺织品的洗涤消毒。
(1)制备ClO2的一种反应为:2NaClO3+2NaCl+2H2SO4=2ClO2↑+Cl2↑+2Na2SO4+2H2O,用单线桥法标出其电子转移的方向和数目_______ 。
(2)取含次氯酸钠0.2mol·L-1的消毒液1mL,加水稀释至200mL,则稀释后次氯酸钠的物质的量浓度为_______ mol·L-1。
(3)为研究84消毒液的性质与使用条件,进行下列实验:
【实验1】向两支试管中分别加入2mL84消毒液,在试管l中加入2mL水,试管2中加入2mL白醋,再分别放入相同的红色纸片。观察到试管2中纸片褪色更快。
①实验中在试管l中加入2mL水的目的是_______ 。
②试管2中纸片褪色更快的原因是_______ 。
③如果实验中加浓盐酸,会有黄绿色气体产生,反应的离子方程式是_______ 。
【实验2】测定84消毒液在不同温度时ORP随时间的变化情况,结果如图所示。
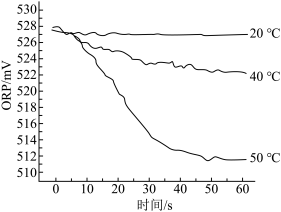
④实验表明,随温度升高,ORP值下降。50℃时ORP值下降较快的原因是_______ 。
资料:84消毒液中含氟微粒主要有ClO-、Cl-、HClO;相同浓度时,HClO的氧化性强于ClO-;ORP是反映物质的氧化一还原性,ORP值越大,氧化性越强。通常情况下,应将84消毒液原液稀释后使用;一般不用于衣服等纺织品的洗涤消毒。
(1)制备ClO2的一种反应为:2NaClO3+2NaCl+2H2SO4=2ClO2↑+Cl2↑+2Na2SO4+2H2O,用单线桥法标出其电子转移的方向和数目
(2)取含次氯酸钠0.2mol·L-1的消毒液1mL,加水稀释至200mL,则稀释后次氯酸钠的物质的量浓度为
(3)为研究84消毒液的性质与使用条件,进行下列实验:
【实验1】向两支试管中分别加入2mL84消毒液,在试管l中加入2mL水,试管2中加入2mL白醋,再分别放入相同的红色纸片。观察到试管2中纸片褪色更快。
①实验中在试管l中加入2mL水的目的是
②试管2中纸片褪色更快的原因是
③如果实验中加浓盐酸,会有黄绿色气体产生,反应的离子方程式是
【实验2】测定84消毒液在不同温度时ORP随时间的变化情况,结果如图所示。

④实验表明,随温度升高,ORP值下降。50℃时ORP值下降较快的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氯气及含氯化合物具有广泛的用途,完成下列填空。
(1)实验室制取氯气的传统方法是___________ (用离子方程式表示)。
(2)若用含有0.4 mol HCl的浓盐酸与足量的MnO2反应制取Cl2,制得的Cl2体积总是小于2.24 L (标准状况)的原因是___________ 。
(3)工业上用氯气与石灰乳反应制备漂白粉的化学方程式为___________ ;具有漂白功能的成分是___________ (用名称表示)。
(4)室温下,久置于空气中的漂白粉最可能含有的杂质为___________ (用化学式表示)。
(5)将Cl2溶于水得到___________ 色的氯水,其中含氯元素的微粒除ClO- 外,还有___________ 。
(6)某温度下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3 的混合溶液,经测定ClO-与ClO 的物质的量浓度之比为1 : 1,则在该反应中,被氧化的氯元素和被还原的氯元素的物质的量之比为
的物质的量浓度之比为1 : 1,则在该反应中,被氧化的氯元素和被还原的氯元素的物质的量之比为___________ 。
(1)实验室制取氯气的传统方法是
(2)若用含有0.4 mol HCl的浓盐酸与足量的MnO2反应制取Cl2,制得的Cl2体积总是小于2.24 L (标准状况)的原因是
(3)工业上用氯气与石灰乳反应制备漂白粉的化学方程式为
(4)室温下,久置于空气中的漂白粉最可能含有的杂质为
(5)将Cl2溶于水得到
(6)某温度下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3 的混合溶液,经测定ClO-与ClO
 的物质的量浓度之比为1 : 1,则在该反应中,被氧化的氯元素和被还原的氯元素的物质的量之比为
的物质的量浓度之比为1 : 1,则在该反应中,被氧化的氯元素和被还原的氯元素的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。氯及其化合物有重要用途,图为氯元素的“价类二维图”的部分信息。请回答下列问题:
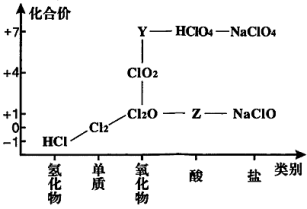
(1)根据图中信息写出Y、Z的化学式_______ 、_______ 。
(2)已知高氯酸(HClO4)是强酸,写出高氯酸与氢氧化钠反应的离子方程式_______ 。
(3)氯气既有氧化性又有还原性,结合图示说明理由_______ 
(4)实验室可用二氧化锰与浓盐酸在加热条件下制得氯气。写出该反应的化学方程式_______ ,该反应中盐酸表现_______ (填字母)。
A.酸性 B.氧化性 C.还原性
(5)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为NaClO+2HCl═NaCl+Cl2↑+H2O,下列有关该反应说法不正确 的是_______ 。
A.n(氧化剂)∶n(还原剂)=1∶1 B.n(氧化剂)∶n(还原剂)=1∶2
C.氧化性:NaClO>Cl2 D.Cl2既是氧化产物又是还原产物
(6)某游泳池常用来NaClO抑制藻类生长,工作人员一次错用H2O2消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了O2和NaCl,写出相应的化学方程式_______ 。

(1)根据图中信息写出Y、Z的化学式
(2)已知高氯酸(HClO4)是强酸,写出高氯酸与氢氧化钠反应的离子方程式
(3)氯气既有氧化性又有还原性,结合图示说明理由

(4)实验室可用二氧化锰与浓盐酸在加热条件下制得氯气。写出该反应的化学方程式
A.酸性 B.氧化性 C.还原性
(5)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为NaClO+2HCl═NaCl+Cl2↑+H2O,下列有关该反应说法
A.n(氧化剂)∶n(还原剂)=1∶1 B.n(氧化剂)∶n(还原剂)=1∶2
C.氧化性:NaClO>Cl2 D.Cl2既是氧化产物又是还原产物
(6)某游泳池常用来NaClO抑制藻类生长,工作人员一次错用H2O2消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了O2和NaCl,写出相应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)现有以下物质:①NaCl晶体 ②液态SO3 ③液态的醋酸 ④汞 ⑤BaSO4固体 ⑥蔗糖(C12H22O11) ⑦酒精(C2H5OH) ⑧熔化K2SO4 请回答下列问题(用序号):
①以上物质中属于电解质的是____________ ;
②以上物质中属于非电解质的是___________ ;
(2)碘元素的一种核素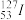 I可用于治疗肿瘤。该核素的质子数为
I可用于治疗肿瘤。该核素的质子数为_________ ,中子数为___________ ,质量数为______________ ,核外电子数为______________ 。
(3)在一定条件下,21.6gA单质与1.20molCl2完全反应,生成0.800molAClx,则X=____________ ,A的摩尔质量为_______________ 。
(4)有反应如下:Al2O3+N2+3C=2AlN+3CO
①标出该反应中电子转移的方向和数目______________ 。
②在该反应中,氧化剂是___________ ,还原剂是_________________ 。
①以上物质中属于电解质的是
②以上物质中属于非电解质的是
(2)碘元素的一种核素
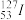 I可用于治疗肿瘤。该核素的质子数为
I可用于治疗肿瘤。该核素的质子数为(3)在一定条件下,21.6gA单质与1.20molCl2完全反应,生成0.800molAClx,则X=
(4)有反应如下:Al2O3+N2+3C=2AlN+3CO
①标出该反应中电子转移的方向和数目
②在该反应中,氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)下列7种化学符号: H、
H、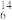 C、
C、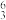 Li、
Li、 Mg、
Mg、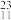 Na、
Na、 N、
N、 Li。其中表示核素的符号共
Li。其中表示核素的符号共_____ 种,互为同位素的是____ 和_____ ,中子数相等,但质子数不相等的核素是_____ 和_____ 。
(2)请选择下列物质中合适的物质直接填空:NaOH、氯化钡、氮气、CO2、H2O2、氯化铵。只含有离子键的有_____ (请用化学式填写,下同),既含有离子键又含有共价键的有_____ ,只含有极性键的有_____ ,含有非极性键的有_____ 。
(1)下列7种化学符号:
 H、
H、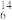 C、
C、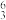 Li、
Li、 Mg、
Mg、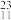 Na、
Na、 N、
N、 Li。其中表示核素的符号共
Li。其中表示核素的符号共(2)请选择下列物质中合适的物质直接填空:NaOH、氯化钡、氮气、CO2、H2O2、氯化铵。只含有离子键的有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求填空。
(1)33.3g某金属氯化物 中含有
中含有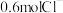 ,则M的相对原子质量为
,则M的相对原子质量为_______ 。
(2)标准状况下,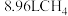 和
和 的混合气体,其质量为7.6g,则混合气体中
的混合气体,其质量为7.6g,则混合气体中 的体积为
的体积为_______ L, 的质量为
的质量为_______ g。
(3) 个
个 约含
约含_______ 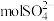 ,其质量为
,其质量为_______ g。
(4)中子数为18的硫原子,其微粒符号可表示为_______ 。
(5)质量数为37、中子数为20的原子,其结构示意图可表示为_______ 。
(6)已知Mm+的电子数为a,M的质量数为A,则 的M的中子数为
的M的中子数为_______ 。
(1)33.3g某金属氯化物
 中含有
中含有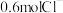 ,则M的相对原子质量为
,则M的相对原子质量为(2)标准状况下,
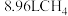 和
和 的混合气体,其质量为7.6g,则混合气体中
的混合气体,其质量为7.6g,则混合气体中 的体积为
的体积为 的质量为
的质量为(3)
 个
个 约含
约含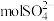 ,其质量为
,其质量为(4)中子数为18的硫原子,其微粒符号可表示为
(5)质量数为37、中子数为20的原子,其结构示意图可表示为
(6)已知Mm+的电子数为a,M的质量数为A,则
 的M的中子数为
的M的中子数为
您最近一年使用:0次

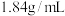 ,质量分数为98%,配制230mL1.0mol/L的稀硫酸需用量筒量取该浓硫酸
,质量分数为98%,配制230mL1.0mol/L的稀硫酸需用量筒量取该浓硫酸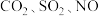 )可获得含
)可获得含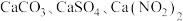 的副产品,工业流程如下:
的副产品,工业流程如下: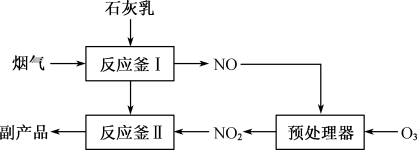
 转化为
转化为 反应的化学方程式:
反应的化学方程式:

