氯气及含氯化合物具有广泛的用途,完成下列填空。
(1)实验室制取氯气的传统方法是___________ (用离子方程式表示)。
(2)若用含有0.4 mol HCl的浓盐酸与足量的MnO2反应制取Cl2,制得的Cl2体积总是小于2.24 L (标准状况)的原因是___________ 。
(3)工业上用氯气与石灰乳反应制备漂白粉的化学方程式为___________ ;具有漂白功能的成分是___________ (用名称表示)。
(4)室温下,久置于空气中的漂白粉最可能含有的杂质为___________ (用化学式表示)。
(5)将Cl2溶于水得到___________ 色的氯水,其中含氯元素的微粒除ClO- 外,还有___________ 。
(6)某温度下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3 的混合溶液,经测定ClO-与ClO 的物质的量浓度之比为1 : 1,则在该反应中,被氧化的氯元素和被还原的氯元素的物质的量之比为
的物质的量浓度之比为1 : 1,则在该反应中,被氧化的氯元素和被还原的氯元素的物质的量之比为___________ 。
(1)实验室制取氯气的传统方法是
(2)若用含有0.4 mol HCl的浓盐酸与足量的MnO2反应制取Cl2,制得的Cl2体积总是小于2.24 L (标准状况)的原因是
(3)工业上用氯气与石灰乳反应制备漂白粉的化学方程式为
(4)室温下,久置于空气中的漂白粉最可能含有的杂质为
(5)将Cl2溶于水得到
(6)某温度下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3 的混合溶液,经测定ClO-与ClO
 的物质的量浓度之比为1 : 1,则在该反应中,被氧化的氯元素和被还原的氯元素的物质的量之比为
的物质的量浓度之比为1 : 1,则在该反应中,被氧化的氯元素和被还原的氯元素的物质的量之比为
更新时间:2021-12-29 13:27:44
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】根据所学的知识填空。
(1)已知铜在常温下能被稀HNO3溶解:3Cu + 8HNO3=3Cu(NO3)2 + 2NO↑+ 4H2O
①用双线桥法表示上述电子转移的方向和数目(在化学方程式上标出)______ 。
②请将上述反应改写成离子方程式:_________________________________________ ;
③19.2g铜与稀硝酸完全反应,生成的气体在标准状况下的体积为_________________ L;若4 mol HNO3参加反应,则该过程转移电子的数目为__________________________ 。
(2)标准状况下,44.8 L由O2和CO2组成的混合气体的质量为82g,则O2的质量为_________ g,该混合气体的平均摩尔质量为_______________________ 。
(3)3.4g NH3中所含氢原子数目与标准状况下__________ L CH4所含氢原子数相同。
(1)已知铜在常温下能被稀HNO3溶解:3Cu + 8HNO3=3Cu(NO3)2 + 2NO↑+ 4H2O
①用双线桥法表示上述电子转移的方向和数目(在化学方程式上标出)
②请将上述反应改写成离子方程式:
③19.2g铜与稀硝酸完全反应,生成的气体在标准状况下的体积为
(2)标准状况下,44.8 L由O2和CO2组成的混合气体的质量为82g,则O2的质量为
(3)3.4g NH3中所含氢原子数目与标准状况下
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氧化还原反应对我们的生产和生活同时具有正负两方面的影响,如果我们能够掌握化学变化的规律,就有可能做到趋利避害,使之更好地为社会发展服务。下面我们逐一分析:
(1)黑火药是我国古代的四大发明之一,黑火药着火时,发生如下氧化还原反应: 。在此反应中,还原剂为
。在此反应中,还原剂为_______ (填化学式),还原产物是_______ (填化学式),当该反应转移2.4mol电子时,产生气体的体积为_______ L(标况下)。
(2)湿法制备高铁酸钾( )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:_______ 。
(3)汽车剧烈碰撞时,安全气囊中发生反应: 。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为
。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为_______ 。
(4) 与一定浓度的
与一定浓度的 反应,生成
反应,生成 、
、 、
、 、NO和
、NO和 ,当
,当 和NO的个数之比为2∶1时,则表现酸性与表现氧化性的
和NO的个数之比为2∶1时,则表现酸性与表现氧化性的 的个数之比为
的个数之比为_______ 。
(1)黑火药是我国古代的四大发明之一,黑火药着火时,发生如下氧化还原反应:
 。在此反应中,还原剂为
。在此反应中,还原剂为(2)湿法制备高铁酸钾(
 )是在碱性环境中进行,反应体系中有六种反应微粒:
)是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:(3)汽车剧烈碰撞时,安全气囊中发生反应:
 。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为
。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为(4)
 与一定浓度的
与一定浓度的 反应,生成
反应,生成 、
、 、
、 、NO和
、NO和 ,当
,当 和NO的个数之比为2∶1时,则表现酸性与表现氧化性的
和NO的个数之比为2∶1时,则表现酸性与表现氧化性的 的个数之比为
的个数之比为
您最近一年使用:0次
【推荐3】高锰酸钾、高铬酸是一种典型的强氧化剂。完成下列填空:
(1)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2 已知该反应中H2O2只发生如下过程:H2O2→O2
①该反应中的还原剂是_____________ 。
②该反应中,发生还原反应的过程是____________ →__________ 。
③写出该反应的化学方程式_______________________ 。
(2)在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
①MnO4-+Cu2S+H+→Cu2++SO2↑+Mn2++H2O(未配平)
②MnO4-+CuS+H+→Cu2++SO2↑+Mn2++H2O(未配平)
下列关于反应①的说法中正确的是______________ (填字母序号)。
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8∶5
c.生成2.24 L(标况下)SO2,反应转移电子的物质的量是0.8 mol
d.还原性的强弱关系是:Mn2+>Cu2S
(3)在稀硫酸中, 和H2O2也能发生氧化还原反应。
和H2O2也能发生氧化还原反应。
已知:2KMnO4+7H2O2+3H2SO4===K2SO4+2MnSO4+6O2↑+10H2O,则被2 mol KMnO4氧化的H2O2是____________ mol。
(4)高锰酸钾溶液与硫化亚铁固体有如下反应:
10FeS+6KMnO4+24H2SO4===3K2SO4+6MnSO4+5Fe2(SO4)3+10S+24H2O
若上述反应前后固体的质量减少了2.8 g,则硫元素与KMnO4之间发生电子转移的数目为________ 。
(1)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2 已知该反应中H2O2只发生如下过程:H2O2→O2
①该反应中的还原剂是
②该反应中,发生还原反应的过程是
③写出该反应的化学方程式
(2)在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
①MnO4-+Cu2S+H+→Cu2++SO2↑+Mn2++H2O(未配平)
②MnO4-+CuS+H+→Cu2++SO2↑+Mn2++H2O(未配平)
下列关于反应①的说法中正确的是
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8∶5
c.生成2.24 L(标况下)SO2,反应转移电子的物质的量是0.8 mol
d.还原性的强弱关系是:Mn2+>Cu2S
(3)在稀硫酸中,
 和H2O2也能发生氧化还原反应。
和H2O2也能发生氧化还原反应。已知:2KMnO4+7H2O2+3H2SO4===K2SO4+2MnSO4+6O2↑+10H2O,则被2 mol KMnO4氧化的H2O2是
(4)高锰酸钾溶液与硫化亚铁固体有如下反应:
10FeS+6KMnO4+24H2SO4===3K2SO4+6MnSO4+5Fe2(SO4)3+10S+24H2O
若上述反应前后固体的质量减少了2.8 g,则硫元素与KMnO4之间发生电子转移的数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】I.洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
(1)用方程式表示工业上用石灰石、氯气为原料生产漂白粉的原理_______________________
(2)漂白粉可用于饮用水或环境消毒,它溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,写出相应的化学方程式__________________________________ 。
(3)浓盐酸和次氯酸钙能发生下列反应:Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O,该反应中转移的电子数为____________ 。
II.SO2被称为“空中死神”,其对环境的危害常表现为 酸雨。为了减少危害,人们进行了许多有益的探索和研究,并且在实际应用上取得了一定的成果。
(4)鉴别SO2和NH3的方法是_______________________ ,若观察到____________________ ,则证明气体是SO2,反之是NH3。
(5)近年来,有人提出了一种利用电解饱和氯化钠溶液(2NaCl+2H2O 2NaOH+Cl2↑+H2↑)循环治理含二氧化硫的废气并回收二氧化硫的方法。该方法的流程如下:
2NaOH+Cl2↑+H2↑)循环治理含二氧化硫的废气并回收二氧化硫的方法。该方法的流程如下:

①此种方法中,可以循环利用的物质是____________________________ 。
②写出反应I的离子方程式:____________________________ 。
(1)用方程式表示工业上用石灰石、氯气为原料生产漂白粉的原理
(2)漂白粉可用于饮用水或环境消毒,它溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,写出相应的化学方程式
(3)浓盐酸和次氯酸钙能发生下列反应:Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O,该反应中转移的电子数为
II.SO2被称为“空中死神”,其对环境的危害常表现为 酸雨。为了减少危害,人们进行了许多有益的探索和研究,并且在实际应用上取得了一定的成果。
(4)鉴别SO2和NH3的方法是
(5)近年来,有人提出了一种利用电解饱和氯化钠溶液(2NaCl+2H2O
 2NaOH+Cl2↑+H2↑)循环治理含二氧化硫的废气并回收二氧化硫的方法。该方法的流程如下:
2NaOH+Cl2↑+H2↑)循环治理含二氧化硫的废气并回收二氧化硫的方法。该方法的流程如下: 
①此种方法中,可以循环利用的物质是
②写出反应I的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】写出下列反应的方程式:
(1)氢氧化亚铁沉淀在空气中迅速变为灰绿色,最终变成红褐色对应的化学方程式___________ 。
(2)工业用氯化铁溶液腐蚀铜印刷电路板的离子方程式___________ 。
(3)漂白粉在空气中生效的化学方程式___________ 。
(4)请写出次氯酸光照分解的离子方程式___________ 。
(5) 中的少量
中的少量 ,可以利用加入酸性
,可以利用加入酸性 溶液进行检验,请写出离子方程式
溶液进行检验,请写出离子方程式______ 。
(1)氢氧化亚铁沉淀在空气中迅速变为灰绿色,最终变成红褐色对应的化学方程式
(2)工业用氯化铁溶液腐蚀铜印刷电路板的离子方程式
(3)漂白粉在空气中生效的化学方程式
(4)请写出次氯酸光照分解的离子方程式
(5)
 中的少量
中的少量 ,可以利用加入酸性
,可以利用加入酸性 溶液进行检验,请写出离子方程式
溶液进行检验,请写出离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】海洋是生命的摇篮,蕴藏着丰富的化学资源。回答下列问题:
(1)目前海水淡化的主要方法有_______ (填一种)。
(2)从氯碱工业的副产品中能够得到一种含氯消毒剂,有效成分为 ,该消毒剂起作用的原理是利用了
,该消毒剂起作用的原理是利用了 的
的_______ (填“强氧化性”或“强还原性”)。
(3)海水提镁工艺流程如图所示:
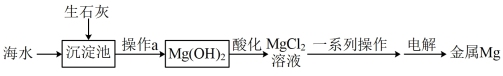
①操作a的名称为_______ 。
②用电解法制备金属镁,两位同学分别设计了下面的两种方法。
甲:电解氯化镁溶液。
乙:电解熔融的氯化镁。
其中_______ (填“甲”或“乙”)同学能够成功地制备金属镁,假设生产过程中镁元素没有损失,则制备120g镁所需生石灰的质量至少为_______ g。
(4)海水提溴工艺流程如图所示:

①海水中的Br-被Cl2氧化的离子方程式是_______ 。
②写出吸收塔中SO2将Br2转化为HBr的化学方程式:_______ 。
(1)目前海水淡化的主要方法有
(2)从氯碱工业的副产品中能够得到一种含氯消毒剂,有效成分为
 ,该消毒剂起作用的原理是利用了
,该消毒剂起作用的原理是利用了 的
的(3)海水提镁工艺流程如图所示:

①操作a的名称为
②用电解法制备金属镁,两位同学分别设计了下面的两种方法。
甲:电解氯化镁溶液。
乙:电解熔融的氯化镁。
其中
(4)海水提溴工艺流程如图所示:

①海水中的Br-被Cl2氧化的离子方程式是
②写出吸收塔中SO2将Br2转化为HBr的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。其中含氯消毒剂在生产生活中有着广泛的用途。
(1)①写出实验室中制取氯气的化学方程式_______ ;实验室用排_______ 的方法除去混在氯气的氯化氢杂质,用_______ 除去混在里面的水蒸气;
②写出次氯酸分解的化学反应方程式_______ ;新制氯水中含有的分子为_______ ;新制氯水含有多种离子,除OH-外,还有_______ ;
(2)常温下,氯气与烧碱溶液反应得“84”消毒液,NaClO 是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用。
①用离子方程式表示“84”消毒液的制备:_______ ;
②某温度下,将氯气通入NaOH溶液中,得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与ClO 的离子个数比为1∶3,请配平该反应的:
的离子个数比为1∶3,请配平该反应的:___ 。_______Cl2+ _______OH- = _______Cl-+1ClO-+3ClO +____H2O;
+____H2O;
(1)①写出实验室中制取氯气的化学方程式
②写出次氯酸分解的化学反应方程式
(2)常温下,氯气与烧碱溶液反应得“84”消毒液,NaClO 是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用。
①用离子方程式表示“84”消毒液的制备:
②某温度下,将氯气通入NaOH溶液中,得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与ClO
 的离子个数比为1∶3,请配平该反应的:
的离子个数比为1∶3,请配平该反应的: +____H2O;
+____H2O;
您最近一年使用:0次
【推荐2】(1)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为__________ ;漂白粉的有效成分是____________ (填化学式)。该反应中氧化剂与还原剂物质的量之比是_______ 。
(2)化学科学在药物的开发、合成和使用中起着至关重要的作用。如小苏打、氢氧化铝、三硅酸镁等可治疗胃酸过多,硫酸亚铁可补铁、防治贫血。试回答下列问题:
①写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:______________________ 。
②自选合适的氧化剂,将补铁剂中的Fe2+氧化成Fe3+,写出相关的离子反应方程式:_____________ 。检验Fe3+常用的试剂除碱外,还可以用_________ (填化学式),现象是_________________________ 。
(3)在反应2KMnO4 + 16HCl === 2KCl + 2MnCl2 + 5Cl2 + 8H2O中,氧化剂是________ ,氧化产物是_______ ,氧化产物与还原产物物质的量之比是__________ ,若有7.3g HCl被氧化,则转移的电子数为_________ mol。
(2)化学科学在药物的开发、合成和使用中起着至关重要的作用。如小苏打、氢氧化铝、三硅酸镁等可治疗胃酸过多,硫酸亚铁可补铁、防治贫血。试回答下列问题:
①写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:
②自选合适的氧化剂,将补铁剂中的Fe2+氧化成Fe3+,写出相关的离子反应方程式:
(3)在反应2KMnO4 + 16HCl === 2KCl + 2MnCl2 + 5Cl2 + 8H2O中,氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求写出如下化学反应方程式或离子反应方程式:
(1)碳酸氢钠俗名________________ ,能够用来治疗胃酸过多,写出相关反应的离子方程式:______________________ 。
(2)漂白粉或漂粉精的有效成分为__________________ ,制取漂白粉的化学方程式为:___________ ,为防止漂白粉变质,应注意___________ 保存。
(3)在反应 3BrF3+5H2O = HBrO3+Br2+9HF+O2 中,被氧化 元素是
元素是____________ ,当有5 mol水反应时,由H2O还原的BrF3为______________ mol。
(1)碳酸氢钠俗名
(2)漂白粉或漂粉精的有效成分为
(3)在反应 3BrF3+5H2O = HBrO3+Br2+9HF+O2 中,被氧化
 元素是
元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】填空。
(1)实验室制备Cl2的离子方程式___________ ,当加入一定量的浓盐酸与足量MnO2反应,实际生成的Cl2体积小于理论值的原因是___________ 。
(2)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型净水剂,可用FeCl3通过下述途径制取:FeCl3+NaOH+NaClO——Na2FeO4+NaCl+H2O
①氧化剂是___________
②每生成1molNa2FeO4整个反应转移电子为___________ mol。
③请用单线桥法表示电子转移情况____________ 。
(3)①0.4mol 中含有的电子数是
中含有的电子数是___________ ,3.9gNa2O2中阴阳离子总数为___________ 。
②原子数为3.01×1023个的氦气在标准状况下的体积为___________ L。
③某气体在标准状况下的密度为1.25g/L,则28g该气体为___________ mol。
(1)实验室制备Cl2的离子方程式
(2)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型净水剂,可用FeCl3通过下述途径制取:FeCl3+NaOH+NaClO——Na2FeO4+NaCl+H2O
①氧化剂是
②每生成1molNa2FeO4整个反应转移电子为
③请用单线桥法表示电子转移情况
(3)①0.4mol
 中含有的电子数是
中含有的电子数是②原子数为3.01×1023个的氦气在标准状况下的体积为
③某气体在标准状况下的密度为1.25g/L,则28g该气体为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】利用如图可从不同角度研究含氯物质的性质及其转化关系。回答下列问题:

(1)a物质的化学式为__ ,b属于__ (填“酸性”或“碱性”)氧化物。
(2)用ClO2消毒水时,ClO2还可将水中的Fe2+转化为Fe3+,Fe3+再水解生成Fe(OH)3胶体,说明ClO2具有__ 性,检验有胶体生成的简便方法是___ 。
(3)工业上可以用反应2NaClO3+H2SO4+SO2=2ClO2+2NaHSO4,制备ClO2,若生成1molClO2,则反应中转移电子的物质的量为__ 。
(4)实验室可用二氧化锰与浓盐酸在加热条件下制取氯气,写出该反应的化学方程式:__ 。
①浓盐酸在该反应中体现的性质有__ (填字母)。
A.还原性 B.氧化性 C.酸性
②若上述反应中产生0.2molCl2,需消耗MnO2的质量为__ g。

(1)a物质的化学式为
(2)用ClO2消毒水时,ClO2还可将水中的Fe2+转化为Fe3+,Fe3+再水解生成Fe(OH)3胶体,说明ClO2具有
(3)工业上可以用反应2NaClO3+H2SO4+SO2=2ClO2+2NaHSO4,制备ClO2,若生成1molClO2,则反应中转移电子的物质的量为
(4)实验室可用二氧化锰与浓盐酸在加热条件下制取氯气,写出该反应的化学方程式:
①浓盐酸在该反应中体现的性质有
A.还原性 B.氧化性 C.酸性
②若上述反应中产生0.2molCl2,需消耗MnO2的质量为
您最近一年使用:0次
【推荐3】I.完成下列氧化还原反应相关问题。
(1)误食NaNO2会使人体血红蛋白中的Fe2+转化为Fe3+而导致中毒,该过程中NaNO2表现出___________ (填“氧化性”或“还原性”)。
(2)已知NaNO2可以与NH4Cl反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目:___________ 。
Ⅱ.KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物ClO2。其反应的化学方程式为2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O
(3)该反应中的氧化产物为___________ (填化学式)。
(4)浓盐酸在该反应中显示出来的性质是___________ (填序号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(5)在碱性条件下加入NaClO3,可将NaCrO2转化为Na2CrO4,ClO 被还原为Cl−,其离子方程式为
被还原为Cl−,其离子方程式为___________ 。还原性:
___________ Cl−(填“>”“<”或“=”)。
(1)误食NaNO2会使人体血红蛋白中的Fe2+转化为Fe3+而导致中毒,该过程中NaNO2表现出
(2)已知NaNO2可以与NH4Cl反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目:
Ⅱ.KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物ClO2。其反应的化学方程式为2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O
(3)该反应中的氧化产物为
(4)浓盐酸在该反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(5)在碱性条件下加入NaClO3,可将NaCrO2转化为Na2CrO4,ClO
 被还原为Cl−,其离子方程式为
被还原为Cl−,其离子方程式为
您最近一年使用:0次



