采用“联合脱硫脱氮技术”处理烟气(含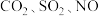 )可获得含
)可获得含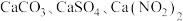 的副产品,工业流程如下:
的副产品,工业流程如下:
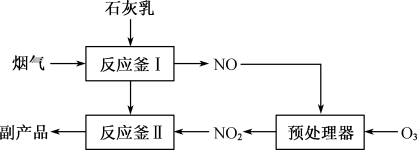
反应釜Ⅱ中 转化为
转化为 反应的化学方程式:
反应的化学方程式:_______ 。
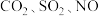 )可获得含
)可获得含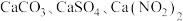 的副产品,工业流程如下:
的副产品,工业流程如下:
反应釜Ⅱ中
 转化为
转化为 反应的化学方程式:
反应的化学方程式:
2023高三·全国·专题练习 查看更多[2]
更新时间:2023-02-04 21:18:47
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】工业废水中的砷(As)(以+3和+5价的形式存在)会对环境造成严重污染。某化学兴趣小组分别以H3AsO3和H3AsO4以及Na3AsO3和Na3AsO4溶液模拟该类废水进行研究后,发现沉淀法和吸附法能使废水中的砷含量显著降低,达到排放标准。
(1)沉淀法:
①在H3AsO3水溶液中加入适量石灰乳,能够产生Ca3(AsO3)2沉淀。该反应的化学方程式为_______ 。
②在Na3AsO4溶液中加入磷酸铋(BiPO4),室温下达到平衡:BiPO4 (s)+ AsO (aq)
(aq)  BiAsO4 (s)+ PO
BiAsO4 (s)+ PO (aq),则溶液中c(AsO
(aq),则溶液中c(AsO )/c(PO
)/c(PO )=
)=_______ 。已知:Ksp(BiPO4)= a,Ksp(BiAsO4)=b
(2)氧化吸附法:
①已知AsO 比AsO
比AsO 的毒性更强,Bi5+具有强氧化性。写出碱性溶液中,Bi5+氧化AsO
的毒性更强,Bi5+具有强氧化性。写出碱性溶液中,Bi5+氧化AsO 得到BiAsO4沉淀的离子方程式
得到BiAsO4沉淀的离子方程式_______ 。
②Fe(OH)3胶体对五价砷有着良好的吸附性,溶液的pH对吸附剂表面所带电荷有影响。采用Bi5+和Fe2+联合处理含砷废水,在AsO 溶液中分别加入Bi5+和Fe2+,两种试剂先后顺序是
溶液中分别加入Bi5+和Fe2+,两种试剂先后顺序是_______ ,原因是_______ 。
③研究发现;pH越高,Fe(OH)3胶体对五价砷的吸附能力越弱,原因是_______ 。
(1)沉淀法:
①在H3AsO3水溶液中加入适量石灰乳,能够产生Ca3(AsO3)2沉淀。该反应的化学方程式为
②在Na3AsO4溶液中加入磷酸铋(BiPO4),室温下达到平衡:BiPO4 (s)+ AsO
 (aq)
(aq)  BiAsO4 (s)+ PO
BiAsO4 (s)+ PO (aq),则溶液中c(AsO
(aq),则溶液中c(AsO )/c(PO
)/c(PO )=
)=(2)氧化吸附法:
①已知AsO
 比AsO
比AsO 的毒性更强,Bi5+具有强氧化性。写出碱性溶液中,Bi5+氧化AsO
的毒性更强,Bi5+具有强氧化性。写出碱性溶液中,Bi5+氧化AsO 得到BiAsO4沉淀的离子方程式
得到BiAsO4沉淀的离子方程式②Fe(OH)3胶体对五价砷有着良好的吸附性,溶液的pH对吸附剂表面所带电荷有影响。采用Bi5+和Fe2+联合处理含砷废水,在AsO
 溶液中分别加入Bi5+和Fe2+,两种试剂先后顺序是
溶液中分别加入Bi5+和Fe2+,两种试剂先后顺序是③研究发现;pH越高,Fe(OH)3胶体对五价砷的吸附能力越弱,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下列三组物质中,均有一种物质的类别与其他三种不同。
①MgO、 、
、 、CuO②HCl、
、CuO②HCl、 、
、 、
、 ③NaOH、
③NaOH、 、KOH、
、KOH、
(1)三种物质依次是(填化学式):
A_______ ;B_______ ;C_______ 。
(2)写出物质C的水溶液与足量稀硫酸反应的离子方程式:_______ 。
(3)将少量 通入
通入 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为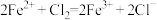 ,则
,则 、
、 、
、 三种离子的还原性由强到弱的顺序为
三种离子的还原性由强到弱的顺序为_______ 。
(4)①用双线桥法标出下列反应的电子转移情况:_______ 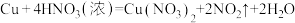 。
。
②该反应的还原剂是_______ ,还原产物是_______ 。
③该反应中氧化剂与氧化产物的质量之比是_______ 。
④当有63g 参加反应时,被氧化的物质其质量为
参加反应时,被氧化的物质其质量为_______ g。
①MgO、
 、
、 、CuO②HCl、
、CuO②HCl、 、
、 、
、 ③NaOH、
③NaOH、 、KOH、
、KOH、
(1)三种物质依次是(填化学式):
A
(2)写出物质C的水溶液与足量稀硫酸反应的离子方程式:
(3)将少量
 通入
通入 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为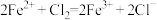 ,则
,则 、
、 、
、 三种离子的还原性由强到弱的顺序为
三种离子的还原性由强到弱的顺序为(4)①用双线桥法标出下列反应的电子转移情况:
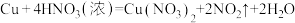 。
。②该反应的还原剂是
③该反应中氧化剂与氧化产物的质量之比是
④当有63g
 参加反应时,被氧化的物质其质量为
参加反应时,被氧化的物质其质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】共和国勋章获得者钟南山院士强调,要注意疫情防控常态化,坚持做好日常消毒工作。含氯消毒剂在卫生防疫方面起着重要的作用。常见的含氯消毒剂有漂白粉、84消毒液等。
(1)漂白粉和84消毒液具有杀菌消毒功能,主要是因为两者均含有_______ (填离子符号)。
(2)已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。回答下列问题:
该“84消毒液”的物质的量浓度约为_______  (计算结果保留两位有效数字)。
(计算结果保留两位有效数字)。
(3)“84消毒液”与“洁则灵”(主要成分为盐酸)一起使用反而会弄巧成拙,产生有毒的气体,造成中毒事件,写出反应的离子反应方程式_______
(4)实验室用 的浓盐酸配制
的浓盐酸配制 的盐酸240mL,应量取浓盐酸的体积为
的盐酸240mL,应量取浓盐酸的体积为_______ mL
(5)配制该盐酸溶液一般可分为以下几个步骤:①量取②计算③溶解(冷却)④摇匀⑤转移溶液(包括洗涤)⑥定容⑦注入试剂瓶贴标签。其正确的操作顺序是_______
(6)下列操作使配制的溶液的物质的量浓度偏高的是_______
①用量筒量取浓盐酸时,俯视刻度线
②用量筒量取浓盐酸后,用蒸馏水洗涤量筒后的溶液转入容量瓶中
③没有将洗涤烧杯和玻璃棒的溶液转入容量瓶中
④定容读数时,俯视容量瓶的刻度线
⑤未冷却就转移定容
(1)漂白粉和84消毒液具有杀菌消毒功能,主要是因为两者均含有
(2)已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。回答下列问题:
84消毒液 有效成分:NaClO 规格:1000mL 质量分数:25% 密度:1.19g/cm3 |
 (计算结果保留两位有效数字)。
(计算结果保留两位有效数字)。(3)“84消毒液”与“洁则灵”(主要成分为盐酸)一起使用反而会弄巧成拙,产生有毒的气体,造成中毒事件,写出反应的离子反应方程式
(4)实验室用
 的浓盐酸配制
的浓盐酸配制 的盐酸240mL,应量取浓盐酸的体积为
的盐酸240mL,应量取浓盐酸的体积为(5)配制该盐酸溶液一般可分为以下几个步骤:①量取②计算③溶解(冷却)④摇匀⑤转移溶液(包括洗涤)⑥定容⑦注入试剂瓶贴标签。其正确的操作顺序是
(6)下列操作使配制的溶液的物质的量浓度偏高的是
①用量筒量取浓盐酸时,俯视刻度线
②用量筒量取浓盐酸后,用蒸馏水洗涤量筒后的溶液转入容量瓶中
③没有将洗涤烧杯和玻璃棒的溶液转入容量瓶中
④定容读数时,俯视容量瓶的刻度线
⑤未冷却就转移定容
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室迅速制备少量氯气可利用如下反应:KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平),此反应常温下就可以迅速进行。结合信息,回答下列问题:
(1)上述反应中被还原的元素为__ (填元素符号),氧化产物是__ (填化学式);
(2)如果上述化学方程式中KMnO4和MnCl2的化学计量数都是2,则HCl的化学计量数是_ ;
(3)实验室通常利用MnO2与浓盐酸共热反应制得氯气,据此可知KMnO4、Cl2、MnO2三种物质的氧化性由弱到强的顺序为__ ;
(4)在酸性条件下, 也能与Fe2+反应生成Mn2+,该反应中Fe2+发生
也能与Fe2+反应生成Mn2+,该反应中Fe2+发生__ 反应。若Fe2+转化为Fe3+,则 和Fe2+的个数之比为
和Fe2+的个数之比为___ 。
(1)上述反应中被还原的元素为
(2)如果上述化学方程式中KMnO4和MnCl2的化学计量数都是2,则HCl的化学计量数是
(3)实验室通常利用MnO2与浓盐酸共热反应制得氯气,据此可知KMnO4、Cl2、MnO2三种物质的氧化性由弱到强的顺序为
(4)在酸性条件下,
 也能与Fe2+反应生成Mn2+,该反应中Fe2+发生
也能与Fe2+反应生成Mn2+,该反应中Fe2+发生 和Fe2+的个数之比为
和Fe2+的个数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】硫及其化合物在工业上有着广泛的应用。完成下列填空:
(1)写出工业上以硫磺为原料生产硫酸的第一步反应方程式______
(2)工业上用过硫酸钾(K2S2O8)测定钢铁中的锰含量,主要反应如下:____ Mn2++____ S2O82﹣+____ H2O→____ MnO4﹣+____ SO42﹣+______ H+。配平该反应方程式,氧化产物是______
(3)用电解硫酸氢钾的方法制取过硫酸钾:HSO4﹣在______ (填:“阳极”或“阴极”)反应生成S2O82﹣,另一极生成氢气,生成0.1mol的S2O82﹣同时可收集到______ g氢气
(4)已知硫酸的第二级电离并不完全:HSO4﹣ H++SO42﹣(Ki=1.2×10﹣2);在0.1mol/L的硫酸氢钾溶液中大约有30%的HSO4﹣电离,则该溶液中离子浓度由大到小排列第2位的离子是
H++SO42﹣(Ki=1.2×10﹣2);在0.1mol/L的硫酸氢钾溶液中大约有30%的HSO4﹣电离,则该溶液中离子浓度由大到小排列第2位的离子是____ ,第4位的离子是____ 。往该溶液中加入硫酸氢钾固体并保持温度不变,则溶液中
____ (填:“增大”、“减小”或“不变”)
(5)已知:HSO3﹣⇌H++SO32﹣K=1.02×10﹣7,NH4++H2O⇌NH3•H2O+H+ K=5.65×10﹣10。往亚硫酸氢铵中加入一定量的氢氧化钡溶液,可能发生的反应离子方程式是____ (选填编号)
a.HSO3﹣+Ba2++OH﹣=BaSO3↓+H2O
b.NH4++2HSO3﹣+2Ba2++3OH﹣=2BaSO3↓+2H2O+NH3•H2O
c.NH4++HSO3﹣+Ba2++2OH﹣=BaSO3↓+H2O+NH3•H2O
d.2NH4++4HSO3﹣+3Ba2++6OH﹣=3BaSO3↓+4H2O+2NH3•H2O+SO32﹣
(1)写出工业上以硫磺为原料生产硫酸的第一步反应方程式
(2)工业上用过硫酸钾(K2S2O8)测定钢铁中的锰含量,主要反应如下:
(3)用电解硫酸氢钾的方法制取过硫酸钾:HSO4﹣在
(4)已知硫酸的第二级电离并不完全:HSO4﹣
 H++SO42﹣(Ki=1.2×10﹣2);在0.1mol/L的硫酸氢钾溶液中大约有30%的HSO4﹣电离,则该溶液中离子浓度由大到小排列第2位的离子是
H++SO42﹣(Ki=1.2×10﹣2);在0.1mol/L的硫酸氢钾溶液中大约有30%的HSO4﹣电离,则该溶液中离子浓度由大到小排列第2位的离子是
(5)已知:HSO3﹣⇌H++SO32﹣K=1.02×10﹣7,NH4++H2O⇌NH3•H2O+H+ K=5.65×10﹣10。往亚硫酸氢铵中加入一定量的氢氧化钡溶液,可能发生的反应离子方程式是
a.HSO3﹣+Ba2++OH﹣=BaSO3↓+H2O
b.NH4++2HSO3﹣+2Ba2++3OH﹣=2BaSO3↓+2H2O+NH3•H2O
c.NH4++HSO3﹣+Ba2++2OH﹣=BaSO3↓+H2O+NH3•H2O
d.2NH4++4HSO3﹣+3Ba2++6OH﹣=3BaSO3↓+4H2O+2NH3•H2O+SO32﹣
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氧化还原反应、离子反应在生产生活中应用广泛。
(1) 和
和 都是大气污染物。利用氨水可以将
都是大气污染物。利用氨水可以将 和
和 吸收,原理如下图所示:
吸收,原理如下图所示:
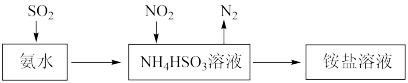
 被吸收的离子方程式是
被吸收的离子方程式是_____ 。
(2)用高能电子束激活烟气(主要成分是 等),会产生
等),会产生 等强氧化性微粒。烟气经下列过程可获得化肥。该化肥中含有的离子是
等强氧化性微粒。烟气经下列过程可获得化肥。该化肥中含有的离子是 、
、_____ (填离子符号)。

(3)SCR(选择性催化还原)工作原理

①尿素 水溶液热解为
水溶液热解为 和
和 ,该反应化学方程式
,该反应化学方程式_____
②反应器中 还原
还原 的化学方程式是
的化学方程式是_____
(4)NSR( 储存还原)的工作原理如下图所示,柴油发动机工作时在稀燃(
储存还原)的工作原理如下图所示,柴油发动机工作时在稀燃( 充足、柴油较少)和富燃(
充足、柴油较少)和富燃( 不足、柴油较多)条件下交替进行,通过
不足、柴油较多)条件下交替进行,通过 和
和 的相互转化实现
的相互转化实现 的储存和还原。
的储存和还原。
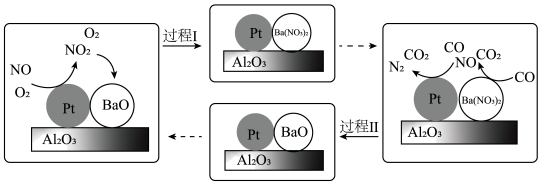
① 吸收
吸收 的反应中氧化剂与还原剂的粒子个数之比是
的反应中氧化剂与还原剂的粒子个数之比是_____ 。
②富燃条件下 表面反应的化学方程式是
表面反应的化学方程式是_____ 。
③若柴油中硫含量较高,在稀燃过程中, 吸收氮氧化物的能力下降至很低水平,结合化学方程式解释原因
吸收氮氧化物的能力下降至很低水平,结合化学方程式解释原因_____ 。
④研究 对
对 吸收氮氧化物的影响,一定温度下,测得气体中
吸收氮氧化物的影响,一定温度下,测得气体中 的体积分数与氮氧化物吸收率的关系如图所示。下列相关分析中正确的是
的体积分数与氮氧化物吸收率的关系如图所示。下列相关分析中正确的是_____ 。
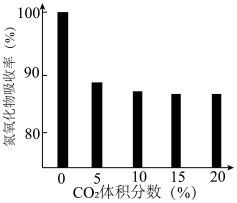
A.一定范围内,氮氧化物吸收率随 体积分数的增大而下降,原因可能是
体积分数的增大而下降,原因可能是 与
与 反应生成
反应生成 ,覆盖在
,覆盖在 表面
表面
B.当 体积分数达到
体积分数达到 时,氮氧化物吸收率依然
时,氮氧化物吸收率依然 体积分数
体积分数 较高,其原因可能是
较高,其原因可能是 在一定程度上也能吸收
在一定程度上也能吸收
C.以上分析均不对
(1)
 和
和 都是大气污染物。利用氨水可以将
都是大气污染物。利用氨水可以将 和
和 吸收,原理如下图所示:
吸收,原理如下图所示: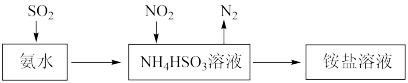
 被吸收的离子方程式是
被吸收的离子方程式是(2)用高能电子束激活烟气(主要成分是
 等),会产生
等),会产生 等强氧化性微粒。烟气经下列过程可获得化肥。该化肥中含有的离子是
等强氧化性微粒。烟气经下列过程可获得化肥。该化肥中含有的离子是 、
、
(3)SCR(选择性催化还原)工作原理

①尿素
 水溶液热解为
水溶液热解为 和
和 ,该反应化学方程式
,该反应化学方程式②反应器中
 还原
还原 的化学方程式是
的化学方程式是(4)NSR(
 储存还原)的工作原理如下图所示,柴油发动机工作时在稀燃(
储存还原)的工作原理如下图所示,柴油发动机工作时在稀燃( 充足、柴油较少)和富燃(
充足、柴油较少)和富燃( 不足、柴油较多)条件下交替进行,通过
不足、柴油较多)条件下交替进行,通过 和
和 的相互转化实现
的相互转化实现 的储存和还原。
的储存和还原。
①
 吸收
吸收 的反应中氧化剂与还原剂的粒子个数之比是
的反应中氧化剂与还原剂的粒子个数之比是②富燃条件下
 表面反应的化学方程式是
表面反应的化学方程式是③若柴油中硫含量较高,在稀燃过程中,
 吸收氮氧化物的能力下降至很低水平,结合化学方程式解释原因
吸收氮氧化物的能力下降至很低水平,结合化学方程式解释原因④研究
 对
对 吸收氮氧化物的影响,一定温度下,测得气体中
吸收氮氧化物的影响,一定温度下,测得气体中 的体积分数与氮氧化物吸收率的关系如图所示。下列相关分析中正确的是
的体积分数与氮氧化物吸收率的关系如图所示。下列相关分析中正确的是
A.一定范围内,氮氧化物吸收率随
 体积分数的增大而下降,原因可能是
体积分数的增大而下降,原因可能是 与
与 反应生成
反应生成 ,覆盖在
,覆盖在 表面
表面B.当
 体积分数达到
体积分数达到 时,氮氧化物吸收率依然
时,氮氧化物吸收率依然 体积分数
体积分数 较高,其原因可能是
较高,其原因可能是 在一定程度上也能吸收
在一定程度上也能吸收
C.以上分析均不对
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使红色湿润石蕊试纸变蓝的气体,它们之间能发生如下反应:
①A+H2O―→B+C ②C + F―→D
③D+NaOH F+E+H2O
F+E+H2O
(1)写出它们的化学式:
C________ ,D________ ,F________ 。
(2)写出各步反应的离子方程式:
①_______________________________________________________________ ;
②_______________________________________________________________ 。
(3)工业生产C的过程中有如下一步反应,即F经催化氧化生成B和H2O。写出该步反应的化学方程式:____________________________________________________________ 。
①A+H2O―→B+C ②C + F―→D
③D+NaOH
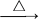 F+E+H2O
F+E+H2O(1)写出它们的化学式:
C
(2)写出各步反应的离子方程式:
①
②
(3)工业生产C的过程中有如下一步反应,即F经催化氧化生成B和H2O。写出该步反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】合成氨是人类科学技术发展史上的一项重大突破,解决了地球上因粮食不足导致的饥饿和死亡问题,这也充分说明了含氮化合物对人类生存的巨大意义。回答下列问题
(1)工业上用氢气和氮气直接合成氨,写出反应的化学方程式_______________ 。氨气极易溶于水,水溶液显 _____ 性,能使酚酞溶液变____ 色,使湿润的红色石蕊试纸变_____ 色。
(2)氮的氧化物有多种,一氧化氮和二氧化氮都是大气污染物。氨气在催化剂作用下可被氧化生成一氧化氮,一氧化氮气体与空气变___ 色,原因是__________ (用化学方程式表示);二氧化氮易溶于水并与水反应,此反应的氧化剂是_______ ,还原剂是______ ,氧化剂和还原剂的质量之比为______
(1)工业上用氢气和氮气直接合成氨,写出反应的化学方程式
(2)氮的氧化物有多种,一氧化氮和二氧化氮都是大气污染物。氨气在催化剂作用下可被氧化生成一氧化氮,一氧化氮气体与空气变
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】“价一类”二维图是元素化合物知识结构化的良好工具,如图是氮元素的“价一类”二维图。回答下列问题:

(1) 的电子式为
的电子式为_______ 。
(2)若物质 为
为 ,其气态呈
,其气态呈_______ 色,不能用排水法收集B气体的原因是_______ 。
(3) 是重要的化工原料,可以合成
是重要的化工原料,可以合成 ,写出工业上以
,写出工业上以 为原料制取
为原料制取 的第一步反应的化学方程式:
的第一步反应的化学方程式:_______ 。
(4)实验室中,检验 溶液中含有
溶液中含有 的实验操作和现象是
的实验操作和现象是_______ 。
(5)铜和足量的 的稀溶液反应,当生成
的稀溶液反应,当生成 (标准状况)
(标准状况) 时,转移的电子数目约为
时,转移的电子数目约为_______ ;反应中 表现的性质为
表现的性质为_______ (填字母)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(6)把盛有 由
由 和
和 组成的混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为
组成的混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为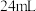 ,则原混合气中
,则原混合气中 的体积是
的体积是_______  。
。

(1)
 的电子式为
的电子式为(2)若物质
 为
为 ,其气态呈
,其气态呈(3)
 是重要的化工原料,可以合成
是重要的化工原料,可以合成 ,写出工业上以
,写出工业上以 为原料制取
为原料制取 的第一步反应的化学方程式:
的第一步反应的化学方程式:(4)实验室中,检验
 溶液中含有
溶液中含有 的实验操作和现象是
的实验操作和现象是(5)铜和足量的
 的稀溶液反应,当生成
的稀溶液反应,当生成 (标准状况)
(标准状况) 时,转移的电子数目约为
时,转移的电子数目约为 表现的性质为
表现的性质为A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(6)把盛有
 由
由 和
和 组成的混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为
组成的混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为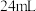 ,则原混合气中
,则原混合气中 的体积是
的体积是 。
。
您最近一年使用:0次



