84消毒液、ClO2是常见的含氯消毒剂。
资料:84消毒液中含氟微粒主要有ClO-、Cl-、HClO;相同浓度时,HClO的氧化性强于ClO-;ORP是反映物质的氧化一还原性,ORP值越大,氧化性越强。通常情况下,应将84消毒液原液稀释后使用;一般不用于衣服等纺织品的洗涤消毒。
(1)制备ClO2的一种反应为:2NaClO3+2NaCl+2H2SO4=2ClO2↑+Cl2↑+2Na2SO4+2H2O,用单线桥法标出其电子转移的方向和数目_______ 。
(2)取含次氯酸钠0.2mol·L-1的消毒液1mL,加水稀释至200mL,则稀释后次氯酸钠的物质的量浓度为_______ mol·L-1。
(3)为研究84消毒液的性质与使用条件,进行下列实验:
【实验1】向两支试管中分别加入2mL84消毒液,在试管l中加入2mL水,试管2中加入2mL白醋,再分别放入相同的红色纸片。观察到试管2中纸片褪色更快。
①实验中在试管l中加入2mL水的目的是_______ 。
②试管2中纸片褪色更快的原因是_______ 。
③如果实验中加浓盐酸,会有黄绿色气体产生,反应的离子方程式是_______ 。
【实验2】测定84消毒液在不同温度时ORP随时间的变化情况,结果如图所示。
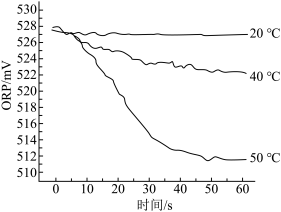
④实验表明,随温度升高,ORP值下降。50℃时ORP值下降较快的原因是_______ 。
资料:84消毒液中含氟微粒主要有ClO-、Cl-、HClO;相同浓度时,HClO的氧化性强于ClO-;ORP是反映物质的氧化一还原性,ORP值越大,氧化性越强。通常情况下,应将84消毒液原液稀释后使用;一般不用于衣服等纺织品的洗涤消毒。
(1)制备ClO2的一种反应为:2NaClO3+2NaCl+2H2SO4=2ClO2↑+Cl2↑+2Na2SO4+2H2O,用单线桥法标出其电子转移的方向和数目
(2)取含次氯酸钠0.2mol·L-1的消毒液1mL,加水稀释至200mL,则稀释后次氯酸钠的物质的量浓度为
(3)为研究84消毒液的性质与使用条件,进行下列实验:
【实验1】向两支试管中分别加入2mL84消毒液,在试管l中加入2mL水,试管2中加入2mL白醋,再分别放入相同的红色纸片。观察到试管2中纸片褪色更快。
①实验中在试管l中加入2mL水的目的是
②试管2中纸片褪色更快的原因是
③如果实验中加浓盐酸,会有黄绿色气体产生,反应的离子方程式是
【实验2】测定84消毒液在不同温度时ORP随时间的变化情况,结果如图所示。

④实验表明,随温度升高,ORP值下降。50℃时ORP值下降较快的原因是
更新时间:2023-06-13 14:32:05
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】根据所学知识,回答下列问题:
(1)分类在化学学习中起着非常重要的作用,下列分类标准合理的是___ (填标号)。
(2)现有以下六种物质:①NaCl溶液,②Cl2,③HClO,④蔗糖,⑤NaOH固体,⑥稀硫酸。其中属于电解质的是___ (填序号)。
(3)化学计量是化学定量研究的基础。
①3.01×1023个CH4分子的物质的量为___ mol,质量为___ g。
②将30mL0.5mol•L-1NaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为___ mol•L-1。
③等质量的H2S和NH3,其分子个数比N(H2S):N(NH3)=___ ,标准状况下气体的体积比V(H2S):V(NH3)= ___ 。
(4)食品干燥剂的作用是降低食品包装袋中的温度,防止食品变质腐败。CaO、CaCl2均可用作食品干燥剂。
①CaO吸水能力强的原理为____ (填化学方程式),CaO的保存方法为___ 。
②检验CaCl2溶液中Cl-存在的具体操作及现象为___ 。
(1)分类在化学学习中起着非常重要的作用,下列分类标准合理的是
| A.根据物质溶于水后形成的溶液呈碱性,可将此类物质归类为碱 |
| B.根据物质能否导电,将物质分为电解质和非电解质 |
| C.根据反应中是否有电子的转移,将化学反应分为氧化还原反应和非氧化还原反应 |
| D.根据分散系中分散质粒子的直径大小,将分散系分为溶液,胶体和浊液 |
(3)化学计量是化学定量研究的基础。
①3.01×1023个CH4分子的物质的量为
②将30mL0.5mol•L-1NaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为
③等质量的H2S和NH3,其分子个数比N(H2S):N(NH3)=
(4)食品干燥剂的作用是降低食品包装袋中的温度,防止食品变质腐败。CaO、CaCl2均可用作食品干燥剂。
①CaO吸水能力强的原理为
②检验CaCl2溶液中Cl-存在的具体操作及现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】将24.4 g NaOH固体溶于水配成100 mL溶液,其密度为1.219 g·mL-1。
(1)该溶液中NaOH的物质的量浓度为________ 。
(2)该溶液中NaOH的质量分数为________ 。
(3)从该溶液中取出10 mL,含NaOH的质量为________ ,含NaOH的物质的量为________ 。
(4)将取出的10 mL溶液加水稀释到100 mL,稀释后溶液中NaOH的物质的量浓度为________ 。
(1)该溶液中NaOH的物质的量浓度为
(2)该溶液中NaOH的质量分数为
(3)从该溶液中取出10 mL,含NaOH的质量为
(4)将取出的10 mL溶液加水稀释到100 mL,稀释后溶液中NaOH的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】实验室需要使用1.0mol/LNaOH溶液80mL。
(1)配制该NaOH溶液所需容量瓶的规格是_______ 。
(2)用托盘天平称取NaOH固体_______ g。
(3)称量完成后,进行如下操作:
A.将称好的NaOH固体放在烧杯中,用适量蒸馏水溶解。
B.待固体全部溶解后,将溶液立即转移到容量瓶。
C.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液也都用玻璃棒引流注入容量瓶,轻轻摇动容量瓶,使溶液混合均匀。
D.继续向容量瓶加蒸馏水至液面离容量瓶颈刻度线下_______ cm时,改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线相切。
E.盖好瓶塞,反复上下颠倒,摇匀。
上述操作不正确的是_______ (填序号)。
(4)若未进行上述操作C,则所得溶液浓度_______ (填“偏高”“偏低”或“无影响”,下同)。若定容时如下图操作,则所得溶液浓度_______ 。

(5)取上述溶液10mL稀释至50mL,所得NaOH溶液的物质的量浓度为_______ 。
(1)配制该NaOH溶液所需容量瓶的规格是
(2)用托盘天平称取NaOH固体
(3)称量完成后,进行如下操作:
A.将称好的NaOH固体放在烧杯中,用适量蒸馏水溶解。
B.待固体全部溶解后,将溶液立即转移到容量瓶。
C.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液也都用玻璃棒引流注入容量瓶,轻轻摇动容量瓶,使溶液混合均匀。
D.继续向容量瓶加蒸馏水至液面离容量瓶颈刻度线下
E.盖好瓶塞,反复上下颠倒,摇匀。
上述操作不正确的是
(4)若未进行上述操作C,则所得溶液浓度

(5)取上述溶液10mL稀释至50mL,所得NaOH溶液的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.分类方法应用比较广泛,属于同一类的物质具有相似性,在生活和学习中使用分类的方法处理问题,可以做到举一反三,还可以做到由此及彼。如:
(1)CO2、SiO2、SO2、SO3都属于酸性氧化物,由CO2+Ca(OH)2=CaCO3↓+H2O,可完成SO3与NaOH反应的方程式为:___ 。
(2)NaHCO3、NaHSO3、NaHS都属于弱酸形成的酸式盐,NaHCO3+HCl=NaCl+H2O+CO2↑及NaHCO3+NaOH=Na2CO3+H2O,可完成NaHS分别与HCl、NaOH反应的方程式为:___ 、___ 。
Ⅱ.氧化还原反应在人类的生产、生活中有着重要的应用。
(3)按如图所示操作,充分反应后:
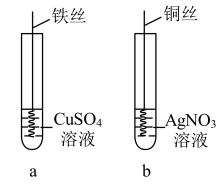
①a中发生反应的离子方程式为___ 。
②b中铜丝上观察到的现象是___ 。
③结合a、b实验现象可知:Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为__ 。
(4)氮氧化物是造成酸雨的成分之一,治理汽车尾气的一种方法是在汽车的排气管上装一个催化转换装置,使NO和CO反应,生成两种空气中的无毒气体。写出该反应的化学方程式,并用双线桥标出电子转移情况:___ 。
(5)高铁酸钠(Na2FeO4)是一种新型的净水剂,可以通过下述反应制取(未配平):Fe(OH)3+NaClO→Na2FeO4+NaCl+H2O。
①该反应中氧化剂是___ (填化学式),___ 元素被氧化(填元素符号)。
②将下面方程式配平、补充完整:__ 。
 Fe(OH)3+
Fe(OH)3+ +
+ NaClO→
NaClO→ Na2FeO4+
Na2FeO4+ NaCl+
NaCl+ H2O
H2O
(1)CO2、SiO2、SO2、SO3都属于酸性氧化物,由CO2+Ca(OH)2=CaCO3↓+H2O,可完成SO3与NaOH反应的方程式为:
(2)NaHCO3、NaHSO3、NaHS都属于弱酸形成的酸式盐,NaHCO3+HCl=NaCl+H2O+CO2↑及NaHCO3+NaOH=Na2CO3+H2O,可完成NaHS分别与HCl、NaOH反应的方程式为:
Ⅱ.氧化还原反应在人类的生产、生活中有着重要的应用。
(3)按如图所示操作,充分反应后:

①a中发生反应的离子方程式为
②b中铜丝上观察到的现象是
③结合a、b实验现象可知:Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为
(4)氮氧化物是造成酸雨的成分之一,治理汽车尾气的一种方法是在汽车的排气管上装一个催化转换装置,使NO和CO反应,生成两种空气中的无毒气体。写出该反应的化学方程式,并用双线桥标出电子转移情况:
(5)高铁酸钠(Na2FeO4)是一种新型的净水剂,可以通过下述反应制取(未配平):Fe(OH)3+NaClO→Na2FeO4+NaCl+H2O。
①该反应中氧化剂是
②将下面方程式配平、补充完整:
 Fe(OH)3+
Fe(OH)3+ +
+ NaClO→
NaClO→ Na2FeO4+
Na2FeO4+ NaCl+
NaCl+ H2O
H2O
您最近一年使用:0次
【推荐2】已知反应:①SO2+H2O=H2SO3;②2SO2+O2=2SO3;③SO2+2H2S=3S↓+2H2O。
(1)上述反应中SO2做还原剂的是_____ ,SO2做氧化剂的是______ 。
(2)用“单线桥”标出反应②中电子转移的方向和数目________ 。
(3)反应③中氧化产物与还原产物的质量比为________ 。
(4)反应③中0.5molSO2参加反应,转移电子数约为________ 。
(5)SO2可以使酸性KMnO4溶液紫色褪去,生成无色的Mn2+,此反应中________ 失去电子,________ 被还原。
(1)上述反应中SO2做还原剂的是
(2)用“单线桥”标出反应②中电子转移的方向和数目
(3)反应③中氧化产物与还原产物的质量比为
(4)反应③中0.5molSO2参加反应,转移电子数约为
(5)SO2可以使酸性KMnO4溶液紫色褪去,生成无色的Mn2+,此反应中
您最近一年使用:0次
【推荐3】根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题。
(1)氧化剂___________ ,还原剂___________ ;
(2)氧化产物___________ ,还原产物___________ ;
(3)用单线桥的方法表示该反应的电子转移情况___________ 。
(4)用双线桥的方法表示该反应的电子转移情况。___________ 。
(5)当有8个NH3分子参加反时,转移的电子个数为___________ 。
(1)氧化剂
(2)氧化产物
(3)用单线桥的方法表示该反应的电子转移情况
(4)用双线桥的方法表示该反应的电子转移情况。
(5)当有8个NH3分子参加反时,转移的电子个数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】正确写出下列化学用语。
(1)写出下列物质的化学式。
①潮湿氯水真正起漂白作用的成分:_______ ;
②磁铁矿的主要成分:_______ 。
(2)碳酸氢铵的电离方程式:_______ 。
(3)铝与 溶液反应的离子方程式:
溶液反应的离子方程式:_______ 。
(1)写出下列物质的化学式。
①潮湿氯水真正起漂白作用的成分:
②磁铁矿的主要成分:
(2)碳酸氢铵的电离方程式:
(3)铝与
 溶液反应的离子方程式:
溶液反应的离子方程式:
您最近一年使用:0次
【推荐2】从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。氯及其化合物有重要用途,以下是氯元素的“价类二维图”的部分信息。请回答下列问题:
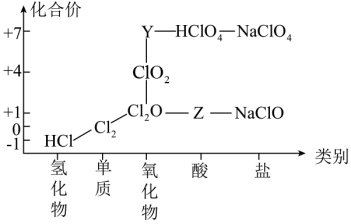
(1)根据图中信息写出Y、Z的化学式___________ 、___________ 。
(2)已知高氯酸( )是强酸,写出高氯酸与铁反应的离子方程式
)是强酸,写出高氯酸与铁反应的离子方程式___________ 。
(3)氯气既有氧化性又有还原性,结合上图说明理由___________
(4)实验室可用二氧化锰与浓盐酸在加热条件下制得氯气。该反应中盐酸表现___________(填字母)。
(5)已知高锰酸钾与浓盐酸混合也能产生氯气。化学反应方程式为: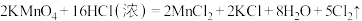 ,若生成标准状况下22.4L
,若生成标准状况下22.4L 则转移电子的物质的量是
则转移电子的物质的量是___________ 。
(6)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为 ,下列说法
,下列说法不正确 的是___________。
(7)某游泳池常用 来抑制藻类生长,工作人员一次错用
来抑制藻类生长,工作人员一次错用 消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了
消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了 和
和 ,写出相应的化学方程式
,写出相应的化学方程式___________ 。

(1)根据图中信息写出Y、Z的化学式
(2)已知高氯酸(
 )是强酸,写出高氯酸与铁反应的离子方程式
)是强酸,写出高氯酸与铁反应的离子方程式(3)氯气既有氧化性又有还原性,结合上图说明理由
(4)实验室可用二氧化锰与浓盐酸在加热条件下制得氯气。该反应中盐酸表现___________(填字母)。
| A.酸性 | B.氧化性 | C.还原性 | D.挥发性 |
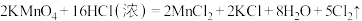 ,若生成标准状况下22.4L
,若生成标准状况下22.4L 则转移电子的物质的量是
则转移电子的物质的量是(6)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为
 ,下列说法
,下列说法| A.84消毒液的主要成分是NaClO | B.n(氧化剂):n(还原剂)=1:2 |
C.氧化性: | D. 既是氧化产物又是还原产物 既是氧化产物又是还原产物 |
 来抑制藻类生长,工作人员一次错用
来抑制藻类生长,工作人员一次错用 消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了
消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了 和
和 ,写出相应的化学方程式
,写出相应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氯及其化合物在生活中应用广泛。如图是一些含氯产品
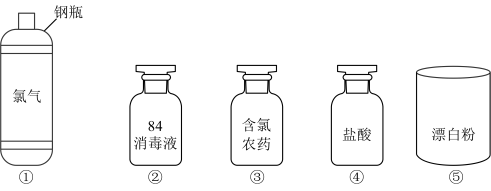
请回答下列问题:
(1)84消毒液的有效成分是次氯酸钠,从物质的分类上看,次氯酸钠属于___________ (填序号)
A.酸 B.碱 C.盐 D.非电解质 E.电解质 F.弱电解质
(2)如果发生了氯气泄漏,以下自救方法得当的是___________(填序号)。
(3)使用84消毒液漂白衣物时,在空气中放置一段时间,漂白效果更好,原因是________ ;
(4)将氯气通入冷的石灰乳中可制备漂白粉,用化学方程式表示制备原理___________ 。

请回答下列问题:
(1)84消毒液的有效成分是次氯酸钠,从物质的分类上看,次氯酸钠属于
A.酸 B.碱 C.盐 D.非电解质 E.电解质 F.弱电解质
(2)如果发生了氯气泄漏,以下自救方法得当的是___________(填序号)。
| A.向地势低的地方撤离 |
| B.观察风向,顺风撤离 |
| C.用蘸有肥皂水的毛巾捂住口鼻撤离 |
| D.用洁净抹布浸透氢氧化钠溶液捂住嘴和鼻 |
(3)使用84消毒液漂白衣物时,在空气中放置一段时间,漂白效果更好,原因是
(4)将氯气通入冷的石灰乳中可制备漂白粉,用化学方程式表示制备原理
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅
②粗硅与干燥HCl气体反应制得SiHCl3:Si+3HCl SiHCl3+H2
SiHCl3+H2
③SiHCl3与过量H2在1000℃~1100℃反应制得纯硅
已知SiHCl3能与H2O强烈反应,在空气中易自燃。请回答下列问题:
(1)第①步制备粗硅的化学反应方程式为__________________ 。
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl3(沸点33.0℃)中含有少量SiCl4
(沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHCl3采用的方法为_______________ 。
(3)用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去):
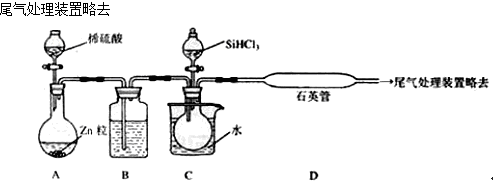
①装置B中的试剂是______ 。装置C中的烧瓶需要水浴加热,其目的是_________ 。
②反应一段时间后,装置D中观察到的现象是____________ ,装置D不能采用普通玻璃管的原因是____________ ,装置D中发生反应的化学方程式为______________ 。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及________ 。
④为鉴定产品硅中是否含微量铁单质,将试样用稀盐酸溶解,取上层清液后需再加入的试剂(填写字母代号)是___________ 。
a.碘水 b.氯水 c.Mg(OH)2 固体 d.KSCN溶液 e.Na2SO3溶液
①高温下用碳还原二氧化硅制得粗硅
②粗硅与干燥HCl气体反应制得SiHCl3:Si+3HCl
 SiHCl3+H2
SiHCl3+H2③SiHCl3与过量H2在1000℃~1100℃反应制得纯硅
已知SiHCl3能与H2O强烈反应,在空气中易自燃。请回答下列问题:
(1)第①步制备粗硅的化学反应方程式为
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl3(沸点33.0℃)中含有少量SiCl4
(沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHCl3采用的方法为
(3)用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去):

①装置B中的试剂是
②反应一段时间后,装置D中观察到的现象是
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及
④为鉴定产品硅中是否含微量铁单质,将试样用稀盐酸溶解,取上层清液后需再加入的试剂(填写字母代号)是
a.碘水 b.氯水 c.Mg(OH)2 固体 d.KSCN溶液 e.Na2SO3溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】2015年9月20日是第27个“全国爱牙日”。为了防止龋齿,正确的刷牙方式和选用适宜的牙膏很重要。对牙膏中的物质的探究要用到许多化学知识。
下表列出了三种牙膏中的摩擦剂:
(1)三种牙膏的摩擦剂中,氢氧化铝是氢氧化物,碳酸钙和二氧化硅分别是________ 、________ (填物质类别)。
(2)根据你的推测,牙膏摩擦剂的溶解性________ (填“易溶”和“难溶”)。
(3)牙膏中的摩擦剂碳酸钙可以用石灰石来制备。某同学设计了一种实验室制备碳酸钙的实验方案,其流程图为:

请写出上述方案中反应③的化学方程式:_________________________________________________ 。
(4)请你仍用石灰石作为原料(其他试剂自选),设计实验室制备碳酸钙的另一种实验方案,依照(3)所示,将你的实验方案用流程图表示出来:
 →
→_______________
你设计的方案的优点为___________________________________ 。
下表列出了三种牙膏中的摩擦剂:
| 牙膏 | ×××牙膏 | ×××牙膏 | ××牙膏 |
| 摩擦剂 | 氢氧化铝 | 碳酸钙 | 二氧化硅 |
(1)三种牙膏的摩擦剂中,氢氧化铝是氢氧化物,碳酸钙和二氧化硅分别是
(2)根据你的推测,牙膏摩擦剂的溶解性
(3)牙膏中的摩擦剂碳酸钙可以用石灰石来制备。某同学设计了一种实验室制备碳酸钙的实验方案,其流程图为:

请写出上述方案中反应③的化学方程式:
(4)请你仍用石灰石作为原料(其他试剂自选),设计实验室制备碳酸钙的另一种实验方案,依照(3)所示,将你的实验方案用流程图表示出来:
 →
→你设计的方案的优点为
您最近一年使用:0次



