从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。氯及其化合物有重要用途,图为氯元素的“价类二维图”的部分信息。请回答下列问题:
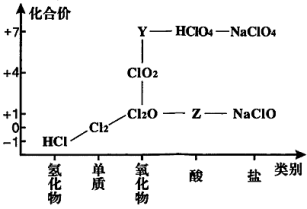
(1)根据图中信息写出Y、Z的化学式_______ 、_______ 。
(2)已知高氯酸(HClO4)是强酸,写出高氯酸与氢氧化钠反应的离子方程式_______ 。
(3)氯气既有氧化性又有还原性,结合图示说明理由_______ 
(4)实验室可用二氧化锰与浓盐酸在加热条件下制得氯气。写出该反应的化学方程式_______ ,该反应中盐酸表现_______ (填字母)。
A.酸性 B.氧化性 C.还原性
(5)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为NaClO+2HCl═NaCl+Cl2↑+H2O,下列有关该反应说法不正确 的是_______ 。
A.n(氧化剂)∶n(还原剂)=1∶1 B.n(氧化剂)∶n(还原剂)=1∶2
C.氧化性:NaClO>Cl2 D.Cl2既是氧化产物又是还原产物
(6)某游泳池常用来NaClO抑制藻类生长,工作人员一次错用H2O2消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了O2和NaCl,写出相应的化学方程式_______ 。

(1)根据图中信息写出Y、Z的化学式
(2)已知高氯酸(HClO4)是强酸,写出高氯酸与氢氧化钠反应的离子方程式
(3)氯气既有氧化性又有还原性,结合图示说明理由

(4)实验室可用二氧化锰与浓盐酸在加热条件下制得氯气。写出该反应的化学方程式
A.酸性 B.氧化性 C.还原性
(5)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为NaClO+2HCl═NaCl+Cl2↑+H2O,下列有关该反应说法
A.n(氧化剂)∶n(还原剂)=1∶1 B.n(氧化剂)∶n(还原剂)=1∶2
C.氧化性:NaClO>Cl2 D.Cl2既是氧化产物又是还原产物
(6)某游泳池常用来NaClO抑制藻类生长,工作人员一次错用H2O2消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了O2和NaCl,写出相应的化学方程式
更新时间:2021-03-11 17:55:55
|
相似题推荐
【推荐1】砷与氮为同主族元素,砷及其化合物可应用宁农药、除草剂、杀虫剂等。完成下列填空:
(1)法庭医学常用马氏试砷法来证明是否砒霜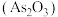 中毒:把试样与锌和盐酸混合,若试样中含有砒霜,则会反应生成砷化氢、氯化锌与水,写出该反应的化学方程式
中毒:把试样与锌和盐酸混合,若试样中含有砒霜,则会反应生成砷化氢、氯化锌与水,写出该反应的化学方程式_____ 。
(2) 和
和 在盐酸中反应转化为
在盐酸中反应转化为 (其中
(其中 为+2价)和
为+2价)和 并放出
并放出 气体,该反应中氧化产物与还原产物的物质的量之比为转移
气体,该反应中氧化产物与还原产物的物质的量之比为转移 电子。写出物质
电子。写出物质 的化学式
的化学式_____ 。
(3)已知 。为验证该反应具有可逆性,将等物质的量浓度的碘水与
。为验证该反应具有可逆性,将等物质的量浓度的碘水与 溶液按体积比为
溶液按体积比为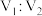 的比例混合(另加入适量的碱)。当
的比例混合(另加入适量的碱)。当
_____  (填“>”或“<”)时,只需加入
(填“>”或“<”)时,只需加入_____ (填试剂名称)就可以确定该反应具有可逆性。上述反应显示: 能在碱性溶液中被
能在碱性溶液中被 氧化成
氧化成 ,而
,而 又能在酸性溶液中被I-还原成
又能在酸性溶液中被I-还原成 ,这表明
,这表明_____ 。
(1)法庭医学常用马氏试砷法来证明是否砒霜
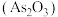 中毒:把试样与锌和盐酸混合,若试样中含有砒霜,则会反应生成砷化氢、氯化锌与水,写出该反应的化学方程式
中毒:把试样与锌和盐酸混合,若试样中含有砒霜,则会反应生成砷化氢、氯化锌与水,写出该反应的化学方程式(2)
 和
和 在盐酸中反应转化为
在盐酸中反应转化为 (其中
(其中 为+2价)和
为+2价)和 并放出
并放出 气体,该反应中氧化产物与还原产物的物质的量之比为转移
气体,该反应中氧化产物与还原产物的物质的量之比为转移 电子。写出物质
电子。写出物质 的化学式
的化学式(3)已知
 。为验证该反应具有可逆性,将等物质的量浓度的碘水与
。为验证该反应具有可逆性,将等物质的量浓度的碘水与 溶液按体积比为
溶液按体积比为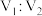 的比例混合(另加入适量的碱)。当
的比例混合(另加入适量的碱)。当
 (填“>”或“<”)时,只需加入
(填“>”或“<”)时,只需加入 能在碱性溶液中被
能在碱性溶液中被 氧化成
氧化成 ,而
,而 又能在酸性溶液中被I-还原成
又能在酸性溶液中被I-还原成 ,这表明
,这表明
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下列物质:①Na2CO3•10H2O②熔融KCl③KClO3晶体④SO2⑤液氯⑥NaHSO4溶液⑦Cu片⑧氢氧化铁胶体
(1)在所处状态下能导电的是______ (填序号,下同);属于电解质的是______ ;属于非电解质的是______ ;Na2CO3的电离方程式为_______ 。
(2)向⑧中逐滴加入⑥,看到的现象是______ 。
(3)加热24.5gKClO3晶体使其充分分解,反应过程中转移的电子数为____ NA。
(4)配平:_____________
______KMnO4+______HCl(浓)=_______KCl+_______Cl2↑+_______MnCl2+________H2O
(1)在所处状态下能导电的是
(2)向⑧中逐滴加入⑥,看到的现象是
(3)加热24.5gKClO3晶体使其充分分解,反应过程中转移的电子数为
(4)配平:
______KMnO4+______HCl(浓)=_______KCl+_______Cl2↑+_______MnCl2+________H2O
您最近一年使用:0次
【推荐3】某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是____ 。
(2)已知2molKBrO3在反应中得到10mol电子生成X,则X的化学式为____ 。
(3)根据上述反应可推知____ 。
a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>X d.还原性:X>AsH3
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并用单线桥法标出电子转移的方向和数目: ,
,______ 。
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是
(2)已知2molKBrO3在反应中得到10mol电子生成X,则X的化学式为
(3)根据上述反应可推知
a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>X d.还原性:X>AsH3
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并用单线桥法标出电子转移的方向和数目:
 ,
,
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氢化钠 (NaH)可在野外用作生氢剂,其化学反应原理为: 。请回答:
。请回答:
(1)NaH属于___________ 化合物(填“共价”或“离子”),NaOH中的化学键有___________ (填写类型)。
(2)用单线桥表示该反应的电子转移情况___________ 。
(3)下列反应与上述反应在氧化还原原理上最相似的是___________。
 。请回答:
。请回答:(1)NaH属于
(2)用单线桥表示该反应的电子转移情况
(3)下列反应与上述反应在氧化还原原理上最相似的是___________。
A. | B.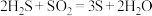 |
C. | D. |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】碱金属元素的氢化物(通式为MH)均为白色晶体,其中H-有很强的还原性,工业上常用作还原剂。
(1)写出NaH在高温下与TiCl4反应生成Ti的化学方程式:___________ 。
(2)已知MH能与水剧烈反应:MH+H2O=MOH+H2↑,在此反应中,H2O是___________ 剂,H2为___________ 产物(填“氧化”、“还原”或“氧化还原”)。
(3)MH和液氨之间也有类似MH和H2O之间的反应,写出MH和液氨反应的化学方程式:___________ 。
(1)写出NaH在高温下与TiCl4反应生成Ti的化学方程式:
(2)已知MH能与水剧烈反应:MH+H2O=MOH+H2↑,在此反应中,H2O是
(3)MH和液氨之间也有类似MH和H2O之间的反应,写出MH和液氨反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】碘及其化合物用途非常广泛。回答下列问题:
(1)2018年CHEMICAL PHYSICS LETTERS报道了Guy Schmitz等学者的研究: 和
和 在96%的浓硫酸中会反应生成一系列化合物(如图)。
在96%的浓硫酸中会反应生成一系列化合物(如图)。
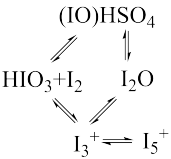
① 中碘的化合价为
中碘的化合价为___________ 价。
②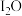 的电子式可表示为
的电子式可表示为___________ 。
③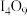 是一种盐,阳离子呈
是一种盐,阳离子呈 价,该盐的化学式为
价,该盐的化学式为___________ 。
(2)实验室用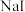 和浓酸反应制取少量
和浓酸反应制取少量 气体,可选用的适宜的酸是___________(填标号)。
气体,可选用的适宜的酸是___________(填标号)。
(3)已知下列反应: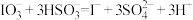

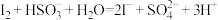
①该条件下,微粒 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为___________ 。
②我国加碘食盐一般加入的是碘酸钾( ),检验食盐中是否加碘,可用醋酸溶液和一种试纸,该试纸是
),检验食盐中是否加碘,可用醋酸溶液和一种试纸,该试纸是___________ 。
(4) 和
和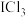 均可用于测定油脂的碘值。
均可用于测定油脂的碘值。
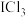 可由
可由 、
、 及稍过量浓盐酸在低于
及稍过量浓盐酸在低于 下制得,该反应的化学方程式为
下制得,该反应的化学方程式为___________ 。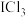 易水解生成
易水解生成 及另两种产物,则另两种产物分别是
及另两种产物,则另两种产物分别是___________ 和___________ 。(填化学式)
(5)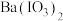 是一种分析试剂,隔绝空气在温度高于
是一种分析试剂,隔绝空气在温度高于 时发生分解,生成
时发生分解,生成 、
、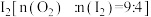 和一种含碘化合物(相对分子质量为1131,且
和一种含碘化合物(相对分子质量为1131,且 和
和 的物质的量之比为5:2),该化合物的化学式为
的物质的量之比为5:2),该化合物的化学式为___________ 。
(1)2018年CHEMICAL PHYSICS LETTERS报道了Guy Schmitz等学者的研究:
 和
和 在96%的浓硫酸中会反应生成一系列化合物(如图)。
在96%的浓硫酸中会反应生成一系列化合物(如图)。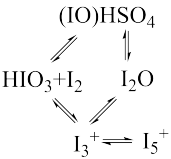
①
 中碘的化合价为
中碘的化合价为②
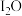 的电子式可表示为
的电子式可表示为③
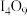 是一种盐,阳离子呈
是一种盐,阳离子呈 价,该盐的化学式为
价,该盐的化学式为(2)实验室用
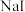 和浓酸反应制取少量
和浓酸反应制取少量 气体,可选用的适宜的酸是___________(填标号)。
气体,可选用的适宜的酸是___________(填标号)。| A.浓盐酸 | B.浓硫酸 | C.浓硝酸 | D.浓磷酸 |
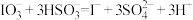

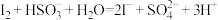
①该条件下,微粒
 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为②我国加碘食盐一般加入的是碘酸钾(
 ),检验食盐中是否加碘,可用醋酸溶液和一种试纸,该试纸是
),检验食盐中是否加碘,可用醋酸溶液和一种试纸,该试纸是(4)
 和
和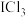 均可用于测定油脂的碘值。
均可用于测定油脂的碘值。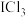 可由
可由 、
、 及稍过量浓盐酸在低于
及稍过量浓盐酸在低于 下制得,该反应的化学方程式为
下制得,该反应的化学方程式为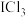 易水解生成
易水解生成 及另两种产物,则另两种产物分别是
及另两种产物,则另两种产物分别是(5)
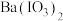 是一种分析试剂,隔绝空气在温度高于
是一种分析试剂,隔绝空气在温度高于 时发生分解,生成
时发生分解,生成 、
、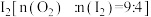 和一种含碘化合物(相对分子质量为1131,且
和一种含碘化合物(相对分子质量为1131,且 和
和 的物质的量之比为5:2),该化合物的化学式为
的物质的量之比为5:2),该化合物的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】2013年H7N9禽流感肆虐期间为了保证卫生环境,常使用漂白液和漂白粉对环境和饮用水进行杀菌、消毒,以抑制大规模传染病爆发。钠、镁及其化合物在工业中具有广泛的应用。回答下列问题:
(1)写出钠与水反应的化学方程式____________________
(2)写出镁与二氧化碳反应的化学方程式___________________
(3)漂白粉溶于水后,与空气中CO2发生反应,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为__________________
(4)某研究性学习小组对漂白液进行了如下实验探究:取漂白液少量,滴入3~5滴紫色石蕊试液,发现溶液先变蓝色后褪色,可以证明漂白液具有的性质_________ (填序号)。
(1)写出钠与水反应的化学方程式
(2)写出镁与二氧化碳反应的化学方程式
(3)漂白粉溶于水后,与空气中CO2发生反应,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为
(4)某研究性学习小组对漂白液进行了如下实验探究:取漂白液少量,滴入3~5滴紫色石蕊试液,发现溶液先变蓝色后褪色,可以证明漂白液具有的性质
| A.酸性 | B.碱性 | C.漂白性 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】洪灾过后,饮用水的消毒、杀菌成为抑制大规模传染性疾病暴发的有效方法之一。漂白粉是常用的消毒剂。
(1)工业上将氯气通入石灰乳制取漂白粉,化学方程式为_________ 。
(2)制取的漂白粉主要成分是_________ (填化学式)。
(3)在使用漂白粉时,加入适量稀盐酸,可增强消毒、杀菌作用,发生化学反应的化学方程式为_________ 。
(4)瓶装漂白粉久置于空气中呈稀粥状而失效。试用化学方程式表示漂白粉在空气中易失效的原因(用化学方程式表示):_________ 。
(1)工业上将氯气通入石灰乳制取漂白粉,化学方程式为
(2)制取的漂白粉主要成分是
(3)在使用漂白粉时,加入适量稀盐酸,可增强消毒、杀菌作用,发生化学反应的化学方程式为
(4)瓶装漂白粉久置于空气中呈稀粥状而失效。试用化学方程式表示漂白粉在空气中易失效的原因(用化学方程式表示):
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】突如其来的新冠肺炎使人们认识到日常杀菌消毒的重要性。氯气、“84”消毒液、漂白粉都是生活中常用的含氯消毒剂,回答下列问题:
(1)工业生产漂白粉的化学方程式为___________ 。
(2)取一滴“84”消毒液滴在pH试纸上,可观察到先变蓝后褪色的现象,证明“84”消毒液具有___________ 性和___________ 性。
(3)日常生活中“84”消毒液若与洁厕灵(含盐酸)混用,发生反应:NaClO+2HCl=NaCl+Cl2↑+H2O,该反应的氧化剂为_________ ,若反应中转移1.5mol电子,则生成的氯气在标准状况下体积为_________ L。
(4)“84”消毒液需要避光密封保存,否则容易变质而失效,用化学方程式解释其原因:①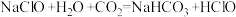 ;②
;②___________ 。
(1)工业生产漂白粉的化学方程式为
(2)取一滴“84”消毒液滴在pH试纸上,可观察到先变蓝后褪色的现象,证明“84”消毒液具有
(3)日常生活中“84”消毒液若与洁厕灵(含盐酸)混用,发生反应:NaClO+2HCl=NaCl+Cl2↑+H2O,该反应的氧化剂为
(4)“84”消毒液需要避光密封保存,否则容易变质而失效,用化学方程式解释其原因:①
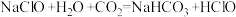 ;②
;②
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氯气是一种重要的化工原料.
(1)氯气是一种黄绿色气体,化学性质上和氧气有许多相似之处,比如:氯气也能支持燃烧,写出铁丝在氯气中燃烧的方程式:______ ;氢气在氯气的燃烧观察的现象为: ______
(2)氯气和石灰乳反应可以制得漂白粉,漂白粉暴露在空气中因吸收了空气中的 和
和 而失效,漂白粉失效过程的化学反应方程式为:
而失效,漂白粉失效过程的化学反应方程式为: ______
(3)氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空 、b、c、d中重合部分代表物质间反应,且氯水足量
、b、c、d中重合部分代表物质间反应,且氯水足量 .
.

 过程的反应方程式
过程的反应方程式 ______ , e过程中的化学方程式为 ______ .
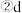 过程所观察到的现象为:
过程所观察到的现象为: ______
b过程证明了氯水的存在______ 微粒

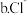
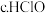
 .
.
(1)氯气是一种黄绿色气体,化学性质上和氧气有许多相似之处,比如:氯气也能支持燃烧,写出铁丝在氯气中燃烧的方程式:
(2)氯气和石灰乳反应可以制得漂白粉,漂白粉暴露在空气中因吸收了空气中的
 和
和 而失效,漂白粉失效过程的化学反应方程式为:
而失效,漂白粉失效过程的化学反应方程式为: (3)氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空
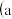 、b、c、d中重合部分代表物质间反应,且氯水足量
、b、c、d中重合部分代表物质间反应,且氯水足量 .
.
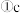 过程的反应方程式
过程的反应方程式 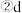 过程所观察到的现象为:
过程所观察到的现象为: b过程证明了氯水的存在

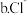
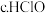
 .
.
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知 Ca(OH)2 与 Cl2 反应的氧化产物与温度有关,在一定量的石灰乳中通入足量的氯气,二者恰好完全反应。生成 Cl-、ClO-、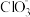 三种含氯元素的离子,其中 ClO- 、
三种含氯元素的离子,其中 ClO- 、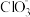 两种离子的物质的量(n)与反应时间
两种离子的物质的量(n)与反应时间
(t)的曲线如图所示。
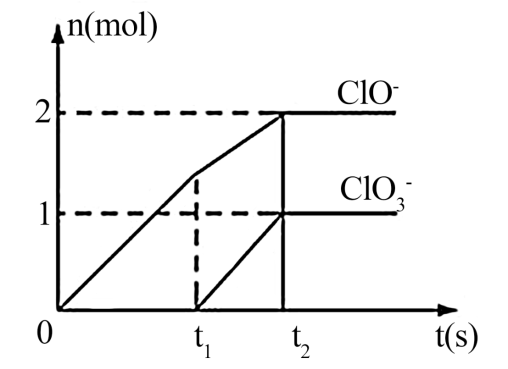
(1)t1 时,开始有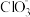 生成的原因是
生成的原因是_____ 。
(2)t2 时,Ca(OH)2 与 Cl2 发生反应的总的化学方程式为___________ 。
(3)该石灰乳中含有 Ca(OH)2 的物质的量是________ mol。
(4)若反应物的量不变,在某温度下恰好完全反应时,氧化产物比值为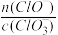 a ,则 n(Cl-)=
a ,则 n(Cl-)=_____ mol
(用含 a 的代数式来表示)。
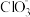 三种含氯元素的离子,其中 ClO- 、
三种含氯元素的离子,其中 ClO- 、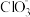 两种离子的物质的量(n)与反应时间
两种离子的物质的量(n)与反应时间(t)的曲线如图所示。

(1)t1 时,开始有
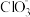 生成的原因是
生成的原因是(2)t2 时,Ca(OH)2 与 Cl2 发生反应的总的化学方程式为
(3)该石灰乳中含有 Ca(OH)2 的物质的量是
(4)若反应物的量不变,在某温度下恰好完全反应时,氧化产物比值为
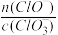 a ,则 n(Cl-)=
a ,则 n(Cl-)=(用含 a 的代数式来表示)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】在学习元素周期表后,某化学兴趣小组在老师的指导下,设计实验以探究元素性质的递变规律。为了验证卤族部分元素性质递变规律,设计如图所示装置(夹持装置已略去)进行实验。( 易溶于
易溶于 ,液体呈紫红色)。
,液体呈紫红色)。
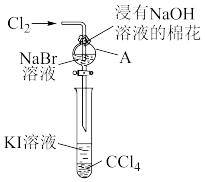
(1)指出溴元素在周期表中的位置:_______ 。
(2)A中发生反应的离子方程式是_______ 。
(3)向A中通入 充分反应后,将A中液体滴入试管内,取下试管,充分振荡,静置,可观察到的现象是
充分反应后,将A中液体滴入试管内,取下试管,充分振荡,静置,可观察到的现象是_______ 。
(4)根据上述实验操作步骤,为确保“非金属性:氯元素>溴元素>碘元素”的实验结论可靠,你认为做好本实验最关键因素是_______ 。
(5)下列性质的递变规律正确,且能作为卤族元素非金属性递变规律判断依据的是_______ (填序号)。
a. 的熔点逐渐升高 b.HCl、HBr、HI的稳定性逐渐减弱
的熔点逐渐升高 b.HCl、HBr、HI的稳定性逐渐减弱
c.HCl、HBr、HI的酸性逐渐减弱 d.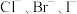 的还原性逐渐增强
的还原性逐渐增强
 易溶于
易溶于 ,液体呈紫红色)。
,液体呈紫红色)。
(1)指出溴元素在周期表中的位置:
(2)A中发生反应的离子方程式是
(3)向A中通入
 充分反应后,将A中液体滴入试管内,取下试管,充分振荡,静置,可观察到的现象是
充分反应后,将A中液体滴入试管内,取下试管,充分振荡,静置,可观察到的现象是(4)根据上述实验操作步骤,为确保“非金属性:氯元素>溴元素>碘元素”的实验结论可靠,你认为做好本实验最关键因素是
(5)下列性质的递变规律正确,且能作为卤族元素非金属性递变规律判断依据的是
a.
 的熔点逐渐升高 b.HCl、HBr、HI的稳定性逐渐减弱
的熔点逐渐升高 b.HCl、HBr、HI的稳定性逐渐减弱c.HCl、HBr、HI的酸性逐渐减弱 d.
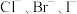 的还原性逐渐增强
的还原性逐渐增强
您最近一年使用:0次



