一定条件下,在一氧化碳变换反应CO+H2O CO2+H2中,有关反应条件改变使反应速率增大的原因分析错误的是
CO2+H2中,有关反应条件改变使反应速率增大的原因分析错误的是
 CO2+H2中,有关反应条件改变使反应速率增大的原因分析错误的是
CO2+H2中,有关反应条件改变使反应速率增大的原因分析错误的是| A.使用催化剂,活化分子百分数增大,单位时间内有效碰撞的次数增加 |
| B.升高温度,活化分子百分数增大,单位时间内有效碰撞的次数增加 |
| C.增大CO的浓度,单位体积内活化分子数增多,单位时间内有效碰撞的次数增加 |
| D.压缩容器,活化分子百分数增大,单位时间内有效碰撞的次数增加 |
更新时间:2022-11-04 19:10:29
|
【知识点】 活化能及其对反应速率的影响解读
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列关于化学反应速率的说法正确的是
①恒温时,增大压强,化学反应速率一定加快
②其他条件不变,温度越高,化学反应速率越快
③使用催化剂可改变反应速率,从而改变该反应过程中吸收或放出的热量
④3 mol•L﹣1•s﹣1的反应速率一定比1 mol•L﹣1•s﹣1的反应速率大
⑤升高温度能使化学反应速率增大,主要原因是增大了反应物分子中活化分子的百分数
⑥有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
⑦增大反应物浓度,可增大活化分子的百分数,从而使单位时间有效碰撞次数增多
⑧催化剂不参与反应,但能降低活化能增大活化分子的百分数,从而增大反应速率
①恒温时,增大压强,化学反应速率一定加快
②其他条件不变,温度越高,化学反应速率越快
③使用催化剂可改变反应速率,从而改变该反应过程中吸收或放出的热量
④3 mol•L﹣1•s﹣1的反应速率一定比1 mol•L﹣1•s﹣1的反应速率大
⑤升高温度能使化学反应速率增大,主要原因是增大了反应物分子中活化分子的百分数
⑥有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
⑦增大反应物浓度,可增大活化分子的百分数,从而使单位时间有效碰撞次数增多
⑧催化剂不参与反应,但能降低活化能增大活化分子的百分数,从而增大反应速率
| A.②⑤ | B.②⑥⑧ | C.②③⑤⑦⑧ | D.①②④⑤⑧ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在固体M的催化下,A转化为D和E分两步进行:① ;②
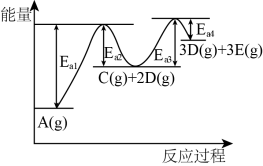
;②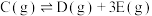 ,其反应过程能量变化如图所示,下列说法错误的是
,其反应过程能量变化如图所示,下列说法错误的是
 ;②
;②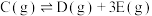 ,其反应过程能量变化如图所示,下列说法错误的是
,其反应过程能量变化如图所示,下列说法错误的是
| A.该反应的速率是由步骤I决定的 |
B.总反应的焓变 |
| C.反应过程中,C物质很难大量积累 |
| D.催化剂的作用是降低反应的活化能,但活化分子百分数不变 |
您最近一年使用:0次

 。
。 加氢制
加氢制 的一种催化机理如图,下列说法正确的是
的一种催化机理如图,下列说法正确的是
 是中间产物
是中间产物 可以释放出带负电荷的
可以释放出带负电荷的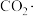
 经过Ni活性中心裂解产生活化态H·的过程中
经过Ni活性中心裂解产生活化态H·的过程中
 作催化剂可以降低反应的焓变,从而提高化学反应速率
作催化剂可以降低反应的焓变,从而提高化学反应速率

