在炽热条件下,将石蜡油分解产生的乙烯通入下列各试管里,装置如图所示。

根据上述装置,回答下列问题:
(1)预测:A装置中的现象是_______ ,B装置中的现象是 _______ 。
(2)D装置中溶液由紫色变无色,D装置中发生反应的类型为_______ 。
(3)写出A装置中发生反应的化学方程式_______ ,反应类型为 _______ 。E装置的作用是 _______ 。
(4)丙烯( )与乙烯具有相似的化学性质(写结构简式)。
)与乙烯具有相似的化学性质(写结构简式)。
①丙烯与溴的加成反应产物为_______ 。
②在一定条件下丙烯与 的加成产物可能为
的加成产物可能为_______ 。

根据上述装置,回答下列问题:
(1)预测:A装置中的现象是
(2)D装置中溶液由紫色变无色,D装置中发生反应的类型为
(3)写出A装置中发生反应的化学方程式
(4)丙烯(
 )与乙烯具有相似的化学性质(写结构简式)。
)与乙烯具有相似的化学性质(写结构简式)。①丙烯与溴的加成反应产物为
②在一定条件下丙烯与
 的加成产物可能为
的加成产物可能为
更新时间:2022-10-08 17:58:12
|
相似题推荐
解答题-有机推断题
|
较易
(0.85)
解题方法
【推荐1】某烷烃的相对分子质量为30,请回答以下问题:
(1)该烷烃的结构简式为_________________ ;
(2)该烷烃与氯气在光照条件下生成一氯代物,请写出该反应的化学方程式___________________ ,该反应的反应类型为_______________ ;
(3)该烷烃可以由含有相同碳原子数的烯烃与氢气反应得到,请写出该反应的化学反应方程式
______________________ ,该反应的反应类型为_______________ 。
(1)该烷烃的结构简式为
(2)该烷烃与氯气在光照条件下生成一氯代物,请写出该反应的化学方程式
(3)该烷烃可以由含有相同碳原子数的烯烃与氢气反应得到,请写出该反应的化学反应方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
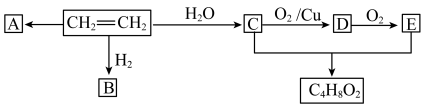
【推荐2】已知A是一种常见的有机化学原料,能用作植物的生长调节剂,也是衡量一个国家石油化水平的标志。有关A的一些转化关系如图,试回答相关问题。
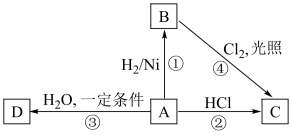
(1)由A制备C时,可以是A-C,也可以是A-B-C,其中_______ 的途径更好,理由是_______ 。
(2)图中反应③的化学方程式为_______ D中官能团的名称为_______ ;图中所示的四个反应中属于加成反应的有_______ (填标号)。
(3)工业上,可通过方法_______ (填标号)获得A。
a.石油的分馏 b.石油的裂解

(1)由A制备C时,可以是A-C,也可以是A-B-C,其中
(2)图中反应③的化学方程式为
(3)工业上,可通过方法
a.石油的分馏 b.石油的裂解
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】Ⅰ.如图是实验室制乙烯的发生装置和乙烯性质实验装置,反应原理为
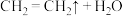 ,回答下列问题:
,回答下列问题:
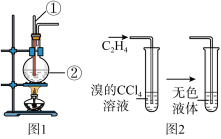
(1)图1中仪器①、②的名称分别为___________ 、___________ 。
(2)收集乙烯气体最好的方法是___________ 。
(3)向溴的四氯化碳溶液中通入乙烯(如图2),溶液的颜色很快褪去,该反应的化学方程式为___________ 。
Ⅱ.实验室制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫。有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。试回答下列问题:
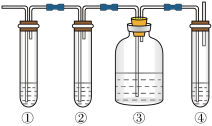
(4)图中①、②、③、④装置盛放的试剂是下列中的___________(将正确选项填入空格内):
①:A;②___________ ;③___________ ;④:D。
A.品红溶液 B.氢氧化钠溶液 C.浓硫酸 D.酸性高锰酸钾溶液
(5)能说明二氧化硫气体存在的现象是___________ 。
(6)使用装置③的目的是___________ 。
(7)确认含有乙烯的现象是___________ 。

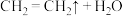 ,回答下列问题:
,回答下列问题:
(1)图1中仪器①、②的名称分别为
(2)收集乙烯气体最好的方法是
(3)向溴的四氯化碳溶液中通入乙烯(如图2),溶液的颜色很快褪去,该反应的化学方程式为
Ⅱ.实验室制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫。有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。试回答下列问题:

(4)图中①、②、③、④装置盛放的试剂是下列中的___________(将正确选项填入空格内):
①:A;②
A.品红溶液 B.氢氧化钠溶液 C.浓硫酸 D.酸性高锰酸钾溶液
(5)能说明二氧化硫气体存在的现象是
(6)使用装置③的目的是
(7)确认含有乙烯的现象是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】实验室可以用乙醇和浓硫酸在170℃时制乙烯,化学反应原理为CH3CH2OH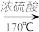 CH2=CH2↑+H2O。由于浓硫酸具有强氧化性,故该反应的副产物有二氧化硫和二氧化碳等。某同学根据上述信息和相应的实验目的选择下列实验装置设计。实验(每种装置都有若干个):
CH2=CH2↑+H2O。由于浓硫酸具有强氧化性,故该反应的副产物有二氧化硫和二氧化碳等。某同学根据上述信息和相应的实验目的选择下列实验装置设计。实验(每种装置都有若干个):
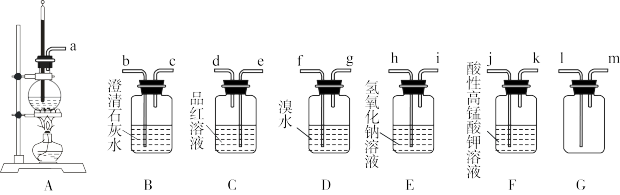
请回答下列问题:
(1)验证乙醇与浓硫酸混合反应产生了二氧化硫和二氧化碳。
①选择必要装置并进行连接:a→_____ (填接口序号)。
②确定混合气体中有二氧化碳存在的实验依据是______ 。
(2)选择装置制备1,2—二溴乙烷。
①该同学设计的方案中装置连接顺序为A→E→D。此方案是否合理?_____ (填“合理”或“不合理”);若不合理,请提出改进方案或方法_____ 。
②分离出1,2—二溴乙烷的操作中使用的玻璃仪器为_____ 。
③有同学建议在A、E之间增加G装置,其作用是____ ,a与G装置接口___ (填“1”或“m”)连接。
(3)阅读资料知“酸性高锰酸钾溶液能氧化乙烯生成二氧化碳”。
请设计实验方案验证资料的真实性。
①装置连接顺序为A→_____ 。
②能证明上述资料真实的实验现象是_____ 。
(4)为了探究乙烯与溴水的反应是取代反应还是加成反应,该同学进行如下实验:①测定D装置中溴水的pH;②将纯净的乙烯通入D装置至溶液褪色;③____ 。
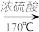 CH2=CH2↑+H2O。由于浓硫酸具有强氧化性,故该反应的副产物有二氧化硫和二氧化碳等。某同学根据上述信息和相应的实验目的选择下列实验装置设计。实验(每种装置都有若干个):
CH2=CH2↑+H2O。由于浓硫酸具有强氧化性,故该反应的副产物有二氧化硫和二氧化碳等。某同学根据上述信息和相应的实验目的选择下列实验装置设计。实验(每种装置都有若干个):
请回答下列问题:
(1)验证乙醇与浓硫酸混合反应产生了二氧化硫和二氧化碳。
①选择必要装置并进行连接:a→
②确定混合气体中有二氧化碳存在的实验依据是
(2)选择装置制备1,2—二溴乙烷。
①该同学设计的方案中装置连接顺序为A→E→D。此方案是否合理?
②分离出1,2—二溴乙烷的操作中使用的玻璃仪器为
③有同学建议在A、E之间增加G装置,其作用是
(3)阅读资料知“酸性高锰酸钾溶液能氧化乙烯生成二氧化碳”。
请设计实验方案验证资料的真实性。
①装置连接顺序为A→
②能证明上述资料真实的实验现象是
(4)为了探究乙烯与溴水的反应是取代反应还是加成反应,该同学进行如下实验:①测定D装置中溴水的pH;②将纯净的乙烯通入D装置至溶液褪色;③
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】为证明乙烯能被酸性 溶液氧化,某小组按下图装置制备乙烯并检验其化学性质。
溶液氧化,某小组按下图装置制备乙烯并检验其化学性质。

完成下列填空:
(1)加热圆底烧瓶,使温度迅速上升到_______ ℃,观察到烧瓶中的无色液体逐渐变黑。该黑色的物质是_______ 。
(2)酸性 溶液很快褪色,但不能说明乙烯具有还原性。理由是
溶液很快褪色,但不能说明乙烯具有还原性。理由是_______ 。
(3)选用下列装置(可重复使用也可不用)来证明乙烯具有还原性,请将装置按编号依次排列,并在装置序号对应位置的下一行写出装置内所放的药品。

装置:a→_______ →b。
药品:(a药品略)_______ (b酸性 溶液)。
溶液)。
(4)若将b中酸性 溶液换成溴水,溴水也能褪色且可观察到b底部有少量无色油状液体生成,可证明该无色油状液体中含有溴元素的试剂是
溶液换成溴水,溴水也能褪色且可观察到b底部有少量无色油状液体生成,可证明该无色油状液体中含有溴元素的试剂是_______ 。
 溶液氧化,某小组按下图装置制备乙烯并检验其化学性质。
溶液氧化,某小组按下图装置制备乙烯并检验其化学性质。
完成下列填空:
(1)加热圆底烧瓶,使温度迅速上升到
(2)酸性
 溶液很快褪色,但不能说明乙烯具有还原性。理由是
溶液很快褪色,但不能说明乙烯具有还原性。理由是(3)选用下列装置(可重复使用也可不用)来证明乙烯具有还原性,请将装置按编号依次排列,并在装置序号对应位置的下一行写出装置内所放的药品。

装置:a→
药品:(a药品略)
 溶液)。
溶液)。(4)若将b中酸性
 溶液换成溴水,溴水也能褪色且可观察到b底部有少量无色油状液体生成,可证明该无色油状液体中含有溴元素的试剂是
溶液换成溴水,溴水也能褪色且可观察到b底部有少量无色油状液体生成,可证明该无色油状液体中含有溴元素的试剂是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】某同学为了检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物,选用了如图所示实验装置。

(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式___________ 。
(2)②中酸性KMnO4溶液的作用是___________ 。
(3)②中两次用到品红溶液,它们的作用分别是A___________ ,B___________ 。
(4)证明SO2的漂白性是可逆性的操作及现象为___________ 。
(5)③中出现的现象是___________ ,发生反应的离子方程式是___________ 。

(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式
(2)②中酸性KMnO4溶液的作用是
(3)②中两次用到品红溶液,它们的作用分别是A
(4)证明SO2的漂白性是可逆性的操作及现象为
(5)③中出现的现象是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】如图是某同学设计的放热反应的观察装置,其实验操作是:①按图所示将实验装置连接好;②在U形管内加入少量红墨水,打开T形管螺旋夹,使U形管内两边的液面处于同一水平面,再夹紧螺旋夹;③在中间的试管里盛1g氧化钙,当滴入2mL左右的蒸馏水后,即可观察。试回答:

(1)实验中观察到的现象是_______ 。
(2)该实验之前必须进行的一步操作是________ 。
(3)实验中发生反应的化学方程式为_________ 。
(4)说明CaO、H2O的能量与Ca(OH)2的能量之间的关系:________ 。

(1)实验中观察到的现象是
(2)该实验之前必须进行的一步操作是
(3)实验中发生反应的化学方程式为
(4)说明CaO、H2O的能量与Ca(OH)2的能量之间的关系:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】某学习小组探究实验室制备氯气的反应,分析物质氧化性和还原性的变化规律。回答下列问题:
(1)写出实验室制备氯气的离子反应方程式,并用双线桥表示电子转移的方向和数目:___________ 。
(2)反应进行一段时间后,不再产生氯气,此时观察到烧瓶中有固体剩余,甲同学认为反应不再产生氯气是因为溶液中不存在Cl-。
①检验溶液中是否存在Cl-的操作是___________ 。
②乙同学认为这个观点不正确,理由是___________ 。
(3)经检验,反应停止后溶液中仍然存在较多H+和Cl-,丙同学就反应停止的原因提出两种猜想,并用反应后的固液混合物进行实验验证。
猜想1:c(H+)降低,使MnO2氧化性减弱
猜想2:c(Cl-)降低,使盐酸还原性减弱
表格中试剂a为___________ (填化学式);现象b为___________ 。
(4)由(3)中实验可知:c(H+)越大,MnO2氧化性越强。据此探究卤素离子的还原性强弱。相同浓度的KCl、KBr和KI溶液分别与MnO2反应,所需的c(H+)最低的是___________ 溶液(填“KCl”或“KBr”或“KI”),从原子结构角度说明理由___________ 。
(1)写出实验室制备氯气的离子反应方程式,并用双线桥表示电子转移的方向和数目:
(2)反应进行一段时间后,不再产生氯气,此时观察到烧瓶中有固体剩余,甲同学认为反应不再产生氯气是因为溶液中不存在Cl-。
①检验溶液中是否存在Cl-的操作是
②乙同学认为这个观点不正确,理由是
(3)经检验,反应停止后溶液中仍然存在较多H+和Cl-,丙同学就反应停止的原因提出两种猜想,并用反应后的固液混合物进行实验验证。
猜想1:c(H+)降低,使MnO2氧化性减弱
猜想2:c(Cl-)降低,使盐酸还原性减弱
| 序号 | 实验操作(加热装置省略) | 试剂 | 现象 | 结论 |
| Ⅰ |  | 较浓的H2SO4 | b | 猜想1正确 |
| Ⅱ | a | b | 猜想2正确 |
(4)由(3)中实验可知:c(H+)越大,MnO2氧化性越强。据此探究卤素离子的还原性强弱。相同浓度的KCl、KBr和KI溶液分别与MnO2反应,所需的c(H+)最低的是
您最近一年使用:0次

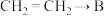 的反应类型是
的反应类型是 的化学方程式是
的化学方程式是 在一定条件下发生聚合反应生成A,化学方程式是
在一定条件下发生聚合反应生成A,化学方程式是

