已知:298K时,相关物质的相对能量如下表所示:
下列说法不正确的是
| 物质 |  |  |  |  |  |  |  |
| 相对能量/(kJ/mol) | 0 | 0 | 0 | -110 | -393 | -242 | -286 |
A.1  完全燃烧生成 完全燃烧生成 放出的热量为286 放出的热量为286 |
B. 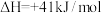 |
C.已知  , ,  ,则 ,则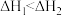 |
| D.将碳先与水蒸气作用转化成水煤气再燃烧,与直接燃烧等质量的碳,反应后都恢复至室温,两个过程的热效应是一样的 |
更新时间:2022-10-26 17:59:02
|
相似题推荐
单选题
|
容易
(0.94)
名校
【推荐1】半导体工业用石英砂做原料通过三个重要反应生产单质硅:
①SiO2(s)(石英砂)+2C(s)=Si(s)(粗硅)+2CO(g) ΔH=+625.63 kJ·mol-1
②Si(s) (粗硅)+2Cl2(g)=SiCl4(g) ΔH=-657.01 kJ·mol-1
③SiCl4(g)+2Mg(s)=2MgCl2(s)+Si(s)(纯硅) ΔH=-625.63 kJ·mol-1
生产1.00 kg纯硅的总反应热为
①SiO2(s)(石英砂)+2C(s)=Si(s)(粗硅)+2CO(g) ΔH=+625.63 kJ·mol-1
②Si(s) (粗硅)+2Cl2(g)=SiCl4(g) ΔH=-657.01 kJ·mol-1
③SiCl4(g)+2Mg(s)=2MgCl2(s)+Si(s)(纯硅) ΔH=-625.63 kJ·mol-1
生产1.00 kg纯硅的总反应热为
| A.2.43×104 kJ | B.-2.35×104 kJ |
| C.-2.23×104 kJ | D.-2.14×104 kJ |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】在298K、101kPa时,已知:



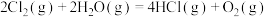

则 与
与 和
和 间的关系正确的是
间的关系正确的是




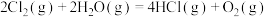

则
 与
与 和
和 间的关系正确的是
间的关系正确的是A.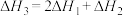 | B. |
C.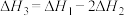 | D.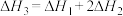 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】图像法是研究化学反应的一种常用方法。已知化学反应A2(g)+B2(g)=2AB(g)的能量变化曲线如图所示,则下列叙述中正确的是


| A.A2(g)+B2(g)=2AB(g)是一个放热反应 |
| B.A2(g)与B2(g)每生成2molAB(g)时吸收bkJ能量 |
| C.该反应中反应物的总能量低于生成物的总能量 |
| D.断裂1molA-A键和1molB-B键时放出akJ能量 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐2】2022年北京冬奥会秉承“绿色办奥”的理念,首次使用氢能作为火炬燃料。下列说法正确的是
| A.火炬使用氢能燃料,碳排放量为零,符合“碳中和”理念 |
| B.火炬燃料的燃烧包含热能转化为化学能的过程 |
| C.需要加热才能发生的反应就一定是吸热反应 |
| D.燃烧属于放热反应,反应物的总能量低于生成物的总能量 |
您最近一年使用:0次

 H2(g)+
H2(g)+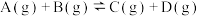 过程中的能量变化如图所示:下列说法正确的是
过程中的能量变化如图所示:下列说法正确的是
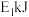
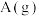 的能量一定大于
的能量一定大于 


