乙醇俗称酒精,分子式为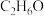 ,常温常压下是一种无色易挥发的液体,能与水以任意比例互溶。乙醇完全燃烧时发生反应:
,常温常压下是一种无色易挥发的液体,能与水以任意比例互溶。乙醇完全燃烧时发生反应: ;不完全燃烧时会有CO生成。请回答下列问题:
;不完全燃烧时会有CO生成。请回答下列问题:
(1)0.5mol 与
与_______ g  含有的氧原子数相同。
含有的氧原子数相同。
(2)同温同压下,同体积的 和CO的物质的量之比为
和CO的物质的量之比为_______ ,质量之比为_______
(3)乙醇完全燃烧时,每消耗9.6g ,生成
,生成 的体积为
的体积为_______ L(标准状况下)。
(4)将23g乙醇溶于一定量的水中配制成500mL乙醇溶液(密度为 ),则该溶液的物质的量浓度为
),则该溶液的物质的量浓度为_______ 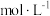 ,质量分数为
,质量分数为_______ %。
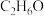 ,常温常压下是一种无色易挥发的液体,能与水以任意比例互溶。乙醇完全燃烧时发生反应:
,常温常压下是一种无色易挥发的液体,能与水以任意比例互溶。乙醇完全燃烧时发生反应: ;不完全燃烧时会有CO生成。请回答下列问题:
;不完全燃烧时会有CO生成。请回答下列问题:(1)0.5mol
 与
与 含有的氧原子数相同。
含有的氧原子数相同。(2)同温同压下,同体积的
 和CO的物质的量之比为
和CO的物质的量之比为(3)乙醇完全燃烧时,每消耗9.6g
 ,生成
,生成 的体积为
的体积为(4)将23g乙醇溶于一定量的水中配制成500mL乙醇溶液(密度为
 ),则该溶液的物质的量浓度为
),则该溶液的物质的量浓度为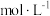 ,质量分数为
,质量分数为
更新时间:2022-11-17 10:01:02
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】①同温同压下,同体积的氨气和硫化氢气体(H2S)的质量比为_________ ;
②同质量的氨气和硫化氢气体的体积比为_______________ ,其中含有的氢的原子个数比为___________ ;
③若二者氢原子数相等,它们的体积比为_____________ ;
④在相同条件下,在5.6g氮气中应添加___________ g氨气所组成的混合气体与16g氧气所占的体积相等。
②同质量的氨气和硫化氢气体的体积比为
③若二者氢原子数相等,它们的体积比为
④在相同条件下,在5.6g氮气中应添加
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)0.5 mol H2O的质量为_______________ ,其中含有_______________ 个水分子,共有_______________ 个原子。
(2)质量都是50g的HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是_______________ ;在相同温度和相同压强条件下,体积最大的是_______________ ,体积最小的是_______________ 。
(2)质量都是50g的HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)1.8g水与____ mol硫酸所含的分子数相等,它们所含氧原子数之比是____ 。
(2)相等物质的量的CO和CO2相比较,则:
①它们所含的氧原子数目之比为__________
②它们所含的电子数目之比为____________
(3)现有mg某气体,它由三原子分子构成,它的摩尔质量为Mg·mol-1。若阿伏加 德罗常数用NA表示,则:
①该气体所含原子总数为____________ 个;
②构成该气体原子的相对原子质量为________ ;
③3.2g某气体中含有的分子数约为3.01×1022,此气体的摩尔质量为_____ 。
(2)相等物质的量的CO和CO2相比较,则:
①它们所含的氧原子数目之比为
②它们所含的电子数目之比为
(3)现有mg某气体,它由三原子分子构成,它的摩尔质量为Mg·mol-1。若阿伏加 德罗常数用NA表示,则:
①该气体所含原子总数为
②构成该气体原子的相对原子质量为
③3.2g某气体中含有的分子数约为3.01×1022,此气体的摩尔质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)已知在标况下的四种物质 ①4.48L CH4 ②3.01×1023个HCl分子 ③10.2g H2S ④0.2mol C2H5OH,物质的量最大的是________ ;质量最小的是________ ;含氢原子数最多的是_________ 。
(2)能用于区别MgCl2溶液与Al(OH)3胶体的物理方法是________________________________
(3)标准状况下,15gCO和CO2混合气体的体积为11.2L,则CO和CO2 的体积比为________________________
(2)能用于区别MgCl2溶液与Al(OH)3胶体的物理方法是
(3)标准状况下,15gCO和CO2混合气体的体积为11.2L,则CO和CO2 的体积比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】①6gH2分子、②2molNH3分子、③4℃时9mLH2O分子(1g/mL)、④1.505×1023个H2SO4分子、⑤标准状况下33.6LO2分子。
(1)其中分子数量最多的是___ ,分子数由少到多的顺序是___ 。
(2)质量由小到大的顺序是___ 。
(1)其中分子数量最多的是
(2)质量由小到大的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1) 9.03×1024个H2O分子的物质的量为__________ ,在标准状况4.48 L SO2的质量为___________ 。
(2) 0.3mol NH3分子中所含氢原子数与________ 个水分子中所含氢原子数相等。
(3) 已知16 g A和20 g B恰好完全反应生成0.04 mol C和31.76 g D,则C的摩尔质量为__ 。
(4) 在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)分别用p(Ne)、p(H2)、p(O2)表示,由大到小的顺序是__ 。
(5) 在质量分数为28%的KOH溶液中,OH- 与H2O的个数之比为________ 。
(2) 0.3mol NH3分子中所含氢原子数与
(3) 已知16 g A和20 g B恰好完全反应生成0.04 mol C和31.76 g D,则C的摩尔质量为
(4) 在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)分别用p(Ne)、p(H2)、p(O2)表示,由大到小的顺序是
(5) 在质量分数为28%的KOH溶液中,OH- 与H2O的个数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】碘是生命体中的必需元素,碘及其化合物在生活中有重要的用途。
(1)KIO3可作为食盐中的补碘剂,KIO3中碘的化合价是__ 。
(2)实验室中制取少量碘可采用如下方法:KI+CuSO4→A(白色)↓+K2SO4+I2。16.0gCuSO4与过量KI反应后可得19.1g的A,则A的化学式为__ 。
(3)单质碘与氟气反应可制得IF5,实验表明液态IF5具有一定的导电性,研究人员发现产生这一现象的可能原因在于IF5的自偶电离(如:2H2O H3O++OH-),生成的阳离子为IF
H3O++OH-),生成的阳离子为IF ,则阴离子为
,则阴离子为__ 。
(4)碘的纯度分析:精确量取0.1150g精制后的碘置于碘量瓶中,加入KI和水振荡至完全溶解(KI仅用于溶解)。以0.0500mol•L-1的Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液17.00mL。则该碘的质量分数为多少___ ?(已知:2S2O +I2=2I-+S4O
+I2=2I-+S4O )
)
(1)KIO3可作为食盐中的补碘剂,KIO3中碘的化合价是
(2)实验室中制取少量碘可采用如下方法:KI+CuSO4→A(白色)↓+K2SO4+I2。16.0gCuSO4与过量KI反应后可得19.1g的A,则A的化学式为
(3)单质碘与氟气反应可制得IF5,实验表明液态IF5具有一定的导电性,研究人员发现产生这一现象的可能原因在于IF5的自偶电离(如:2H2O
 H3O++OH-),生成的阳离子为IF
H3O++OH-),生成的阳离子为IF ,则阴离子为
,则阴离子为(4)碘的纯度分析:精确量取0.1150g精制后的碘置于碘量瓶中,加入KI和水振荡至完全溶解(KI仅用于溶解)。以0.0500mol•L-1的Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液17.00mL。则该碘的质量分数为多少
 +I2=2I-+S4O
+I2=2I-+S4O )
)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】物质的量是高中化学常用的物理量,请完成以下有关计算。
(1)含0.4 mol Al3+的Al2(SO4)3中所含的SO42-的物质的量是___________ 。
(2)___________ molH2O2所含原子数与0.2molH3PO4所含原子数相等。
(3)某硫酸钠溶液中含有3.01×1022个Na+,则溶液中SO42-的物质的量是___________ 。
(4)0.7 mol H2O的质量为___________ 。
(5)483gNa2SO4·10H2O中所含的Na+的物质的量是___ mol,所含H2O分子的数目是___ 个。
(6)质量相同的H2、NH3、SO2、O3四种气体中,含有分子数目最少的是____________ 。
(7)a个X原子的总质量为bg,则X的相对原子质量可以表示为___________
(8)现有mg某气体,它是三原子分子,其摩尔质量为Mg·mol-1。若阿伏伽德罗常数用NA表示,请用以上符号及相应数字填写下列空格。
(1)含0.4 mol Al3+的Al2(SO4)3中所含的SO42-的物质的量是
(2)
(3)某硫酸钠溶液中含有3.01×1022个Na+,则溶液中SO42-的物质的量是
(4)0.7 mol H2O的质量为
(5)483gNa2SO4·10H2O中所含的Na+的物质的量是
(6)质量相同的H2、NH3、SO2、O3四种气体中,含有分子数目最少的是
(7)a个X原子的总质量为bg,则X的相对原子质量可以表示为
(8)现有mg某气体,它是三原子分子,其摩尔质量为Mg·mol-1。若阿伏伽德罗常数用NA表示,请用以上符号及相应数字填写下列空格。
①该气体的物质的量为
②该气体所含原子总数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(混合物平均摩尔质量通常可表示为: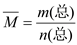 ,利用此概念可以讨论许多化学问题:
,利用此概念可以讨论许多化学问题:
(1)相同条件下,潮湿空气的密度___________ (选填“>”、“<”或“=”)干燥空气的密度,理由是___________ ___________________________________________________________________;
(2)在一定条件下的密闭容器中,以碳和水蒸气为反应物,发生反应:
C(s)+H2O(g) CO(g)+H2(g);达到平衡后保持温度不变并加压,则
CO(g)+H2(g);达到平衡后保持温度不变并加压,则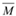 (混合气)将
(混合气)将___________ (填写“变大”、“变小”或“不变”);
(3)以物质的量之比为1:2相混合的Na2SO3和K2SO3的混合物共a g,与足量盐酸反应生成的SO2物质的量n(SO2)=___________ mol(用含a的代数式表示)。
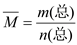 ,利用此概念可以讨论许多化学问题:
,利用此概念可以讨论许多化学问题:(1)相同条件下,潮湿空气的密度
(2)在一定条件下的密闭容器中,以碳和水蒸气为反应物,发生反应:
C(s)+H2O(g)
 CO(g)+H2(g);达到平衡后保持温度不变并加压,则
CO(g)+H2(g);达到平衡后保持温度不变并加压,则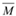 (混合气)将
(混合气)将(3)以物质的量之比为1:2相混合的Na2SO3和K2SO3的混合物共a g,与足量盐酸反应生成的SO2物质的量n(SO2)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】通过计算,回答下列问题:
(1)标况下 分子中所含原子数与
分子中所含原子数与______ 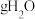 分子中所含原子数相等。
分子中所含原子数相等。
(2)一定条件下, 和
和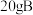 恰好完全反应生成
恰好完全反应生成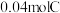 和
和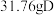 ,则C的摩尔质量为
,则C的摩尔质量为______ 。
(3)等质量的 和
和 中所含有的电子数之比为
中所含有的电子数之比为______ 。
(4)标准状况下, 与足量
与足量 反应转移的电子数为
反应转移的电子数为______ 。
(1)标况下
 分子中所含原子数与
分子中所含原子数与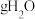 分子中所含原子数相等。
分子中所含原子数相等。(2)一定条件下,
 和
和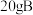 恰好完全反应生成
恰好完全反应生成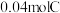 和
和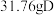 ,则C的摩尔质量为
,则C的摩尔质量为(3)等质量的
 和
和 中所含有的电子数之比为
中所含有的电子数之比为(4)标准状况下,
 与足量
与足量 反应转移的电子数为
反应转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】研究含硼化合物具有重要意义。
(1) 易溶于热水、在冷水中溶解度较小,可通过如下过程制得:称取10 g钠硼解石[主要成分
易溶于热水、在冷水中溶解度较小,可通过如下过程制得:称取10 g钠硼解石[主要成分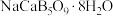 ,含少量
,含少量 、NaCl和难溶于酸的物质],除去氯化钠后,在60℃下用浓硝酸溶解,趁热过滤,将滤渣用热水洗净后,合并滤液和洗涤液,降温结晶,过滤得
、NaCl和难溶于酸的物质],除去氯化钠后,在60℃下用浓硝酸溶解,趁热过滤,将滤渣用热水洗净后,合并滤液和洗涤液,降温结晶,过滤得 。
。
①写出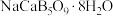 与硝酸反应生成
与硝酸反应生成 的化学方程式:
的化学方程式:______ 。
②60℃时,控制钠硼解石量一定,硝酸溶解时B的浸出率随液固质量比 的变化如图所示。硝酸溶解时控制液固质量比为5∶1,而不采用更大液固质量比的原因是
的变化如图所示。硝酸溶解时控制液固质量比为5∶1,而不采用更大液固质量比的原因是______ 。

③钠硼解石中的B可看成以 形式存在。液固质量比为测定钠硼解石中
形式存在。液固质量比为测定钠硼解石中 的质量分数,实验方案如下:将所得
的质量分数,实验方案如下:将所得 用热水完全溶解后,加水定容至500 mL。取25.00 mL溶液,加入适量甘露醇(甘露醇与
用热水完全溶解后,加水定容至500 mL。取25.00 mL溶液,加入适量甘露醇(甘露醇与 结合后,每分子
结合后,每分子 可电离出1个
可电离出1个 ),滴入2~3滴酚酞作指示剂,用0.2500 mol·L
),滴入2~3滴酚酞作指示剂,用0.2500 mol·L NaOH标准溶液进行滴定,终点时消耗NaOH标准溶液20.00 mL。根据实验数据计算钠硼解石中
NaOH标准溶液进行滴定,终点时消耗NaOH标准溶液20.00 mL。根据实验数据计算钠硼解石中 的质量分数,写出计算过程
的质量分数,写出计算过程______ 。
(2)一种镍磷化合物催化氨硼烷水解制氢的可能机理如图所示。

①“中间体I”中B、N上所连H分别吸附在Ni和P上的原因是______ 。
②“中间体III”可以进一步水解,则氨硼烷水解最终所得含硼化合物的化学式为____________ 。
(3)一种 是核工业屏蔽中子的新型材料。其晶胞中Ca处于晶胞的体心位置,占据晶胞8个顶点的是由B原子构成的正八面体。晶胞和正八面体结构如图所示。
是核工业屏蔽中子的新型材料。其晶胞中Ca处于晶胞的体心位置,占据晶胞8个顶点的是由B原子构成的正八面体。晶胞和正八面体结构如图所示。 中
中
______ 。

(1)
 易溶于热水、在冷水中溶解度较小,可通过如下过程制得:称取10 g钠硼解石[主要成分
易溶于热水、在冷水中溶解度较小,可通过如下过程制得:称取10 g钠硼解石[主要成分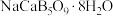 ,含少量
,含少量 、NaCl和难溶于酸的物质],除去氯化钠后,在60℃下用浓硝酸溶解,趁热过滤,将滤渣用热水洗净后,合并滤液和洗涤液,降温结晶,过滤得
、NaCl和难溶于酸的物质],除去氯化钠后,在60℃下用浓硝酸溶解,趁热过滤,将滤渣用热水洗净后,合并滤液和洗涤液,降温结晶,过滤得 。
。①写出
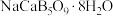 与硝酸反应生成
与硝酸反应生成 的化学方程式:
的化学方程式:②60℃时,控制钠硼解石量一定,硝酸溶解时B的浸出率随液固质量比
 的变化如图所示。硝酸溶解时控制液固质量比为5∶1,而不采用更大液固质量比的原因是
的变化如图所示。硝酸溶解时控制液固质量比为5∶1,而不采用更大液固质量比的原因是
③钠硼解石中的B可看成以
 形式存在。液固质量比为测定钠硼解石中
形式存在。液固质量比为测定钠硼解石中 的质量分数,实验方案如下:将所得
的质量分数,实验方案如下:将所得 用热水完全溶解后,加水定容至500 mL。取25.00 mL溶液,加入适量甘露醇(甘露醇与
用热水完全溶解后,加水定容至500 mL。取25.00 mL溶液,加入适量甘露醇(甘露醇与 结合后,每分子
结合后,每分子 可电离出1个
可电离出1个 ),滴入2~3滴酚酞作指示剂,用0.2500 mol·L
),滴入2~3滴酚酞作指示剂,用0.2500 mol·L NaOH标准溶液进行滴定,终点时消耗NaOH标准溶液20.00 mL。根据实验数据计算钠硼解石中
NaOH标准溶液进行滴定,终点时消耗NaOH标准溶液20.00 mL。根据实验数据计算钠硼解石中 的质量分数,写出计算过程
的质量分数,写出计算过程(2)一种镍磷化合物催化氨硼烷水解制氢的可能机理如图所示。

①“中间体I”中B、N上所连H分别吸附在Ni和P上的原因是
②“中间体III”可以进一步水解,则氨硼烷水解最终所得含硼化合物的化学式为
(3)一种
 是核工业屏蔽中子的新型材料。其晶胞中Ca处于晶胞的体心位置,占据晶胞8个顶点的是由B原子构成的正八面体。晶胞和正八面体结构如图所示。
是核工业屏蔽中子的新型材料。其晶胞中Ca处于晶胞的体心位置,占据晶胞8个顶点的是由B原子构成的正八面体。晶胞和正八面体结构如图所示。 中
中

您最近一年使用:0次

 溶液的体积
溶液的体积

