某小组设计如下实验研究实验室中的甲酸。已知:25℃时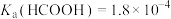
(1)配制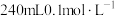 的HCOOH溶液,需
的HCOOH溶液,需 的HCOOH溶液的体积为
的HCOOH溶液的体积为_______ mL。
(2)为确定甲酸溶液的准确浓度,取20mL甲酸溶液于锥形瓶中,加入2滴_______ 溶液,用 的NaOH溶液滴定至终点,消耗NaOH溶液的体积为22.04mL,滴定实验中所使用的锥形瓶的容积最恰当的是
的NaOH溶液滴定至终点,消耗NaOH溶液的体积为22.04mL,滴定实验中所使用的锥形瓶的容积最恰当的是_______ (填字母)。
A.50mL B.100mL C.200mL D.250mL
(3)下列关于滴定操作的说法正确的_______
(4)小组同学用_______ 测出25℃时该甲酸溶液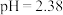 ,则水电离产生的
,则水电离产生的 数量级为
数量级为_______ 。
(5)25℃时甲酸与醋酸钠溶液反应: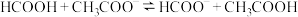 ,该反应的平衡常数为10,则该温度下醋酸的电离常数
,该反应的平衡常数为10,则该温度下醋酸的电离常数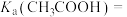
_______ 。
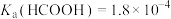
(1)配制
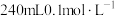 的HCOOH溶液,需
的HCOOH溶液,需 的HCOOH溶液的体积为
的HCOOH溶液的体积为(2)为确定甲酸溶液的准确浓度,取20mL甲酸溶液于锥形瓶中,加入2滴
 的NaOH溶液滴定至终点,消耗NaOH溶液的体积为22.04mL,滴定实验中所使用的锥形瓶的容积最恰当的是
的NaOH溶液滴定至终点,消耗NaOH溶液的体积为22.04mL,滴定实验中所使用的锥形瓶的容积最恰当的是A.50mL B.100mL C.200mL D.250mL
(3)下列关于滴定操作的说法正确的_______
| A.滴定前应检查滴定管是否漏水,进行洗涤、润洗 |
| B.将标准溶液装入滴定管时,应借助玻璃棒或漏斗等玻璃仪器转移 |
| C.进行滴定操作时,眼睛要始终注视着滴定管内液面的变化 |
| D.滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁 |
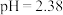 ,则水电离产生的
,则水电离产生的 数量级为
数量级为(5)25℃时甲酸与醋酸钠溶液反应:
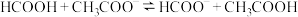 ,该反应的平衡常数为10,则该温度下醋酸的电离常数
,该反应的平衡常数为10,则该温度下醋酸的电离常数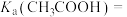
更新时间:2022-11-12 09:23:53
|
相似题推荐
计算题
|
较易
(0.85)
解题方法
【推荐1】配制500 mL 1 mol·L-1 H2SO4溶液,需要16 mol·L-1 H2SO4 溶液的体积为____________ 。
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐2】按要求完成下列空白:
(1) 已知3.01×1023个氖原子的质量为w g,则氖气的摩尔质量是_________ 。
(2) 在同温、同压下,实验测得CO、N2和O2三种气体的混合气体的密度是H2的14.5倍,其中O2的质量分数为_________ 。若其中CO和N2的物质的量之比为1: 1,则混合气体中氧元素的质量分数为_____ 。(保留3位有效数字)
(3) 将25℃ 101KPa条件下49 L的NH3气体(注:该条件下气体摩尔体积为24.5 L/mol)溶于166ml(ρ=1g/cm3)的水中,所得氨水的密度为0.8 g/cm3,该氨水的物质的量浓度为___________ ,取出 30.0 mL该溶液,配成4.0 mol/L的稀溶液,则稀释后溶液的体积为____________ mL。
(1) 已知3.01×1023个氖原子的质量为w g,则氖气的摩尔质量是
(2) 在同温、同压下,实验测得CO、N2和O2三种气体的混合气体的密度是H2的14.5倍,其中O2的质量分数为
(3) 将25℃ 101KPa条件下49 L的NH3气体(注:该条件下气体摩尔体积为24.5 L/mol)溶于166ml(ρ=1g/cm3)的水中,所得氨水的密度为0.8 g/cm3,该氨水的物质的量浓度为
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐1】完成下列小题
(1)25℃时,在2.0×10-3mol·L-1的氢氟酸水溶液中,调节溶液pH(忽略调节时体积变化),测得平衡体系中c(F-)、c(HF)与溶液pH的关系如图。
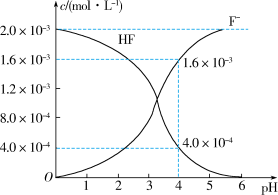
则25℃时,Ka(HF)=_____ (列式求值)。
(2)联氨(N2H4)为二元弱碱,在水中的电离方程式与氨相似。联氨第一步电离的平衡常数为_____ (已知:N2H4+H+ N2H
N2H 的K=8.7×107;Kw=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为
的K=8.7×107;Kw=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为_____ 。
(1)25℃时,在2.0×10-3mol·L-1的氢氟酸水溶液中,调节溶液pH(忽略调节时体积变化),测得平衡体系中c(F-)、c(HF)与溶液pH的关系如图。

则25℃时,Ka(HF)=
(2)联氨(N2H4)为二元弱碱,在水中的电离方程式与氨相似。联氨第一步电离的平衡常数为
 N2H
N2H 的K=8.7×107;Kw=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为
的K=8.7×107;Kw=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐2】在室温下,下列五种溶液:
①
 溶液②
溶液② 硫酸③
硫酸③
 ④0.1mo/LNaOH溶液⑤
④0.1mo/LNaOH溶液⑤
 溶液
溶液
(1)加水稀释100倍后,①中的pH___________ 5(填“>”、“<”或“=”)。
(2)若溶液③达到平衡时已电离的 为
为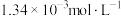 ,电离常数的值为
,电离常数的值为_____ 。
(3)溶液③中,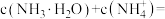
___________  。
。
(4)若取④0.1mol/LNaOH溶液10mL与⑤
 溶液15mL混合,假设混合后溶液体积为25mL,测混合后溶液的
溶液15mL混合,假设混合后溶液体积为25mL,测混合后溶液的 ___________(填序号)。(已知
___________(填序号)。(已知 )
)
①

 溶液②
溶液② 硫酸③
硫酸③
 ④0.1mo/LNaOH溶液⑤
④0.1mo/LNaOH溶液⑤
 溶液
溶液(1)加水稀释100倍后,①中的pH
(2)若溶液③达到平衡时已电离的
 为
为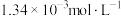 ,电离常数的值为
,电离常数的值为(3)溶液③中,
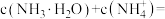
 。
。(4)若取④0.1mol/LNaOH溶液10mL与⑤

 溶液15mL混合,假设混合后溶液体积为25mL,测混合后溶液的
溶液15mL混合,假设混合后溶液体积为25mL,测混合后溶液的 ___________(填序号)。(已知
___________(填序号)。(已知 )
)| A.12 | B.11.7 | C.2 | D.1.7 |
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐3】国家标准规定酿造食醋总酸含量不得低于3.5g/100mL,为测定某品牌市售醋酸的浓度,用移液管移取25mL,定容至250mL。取25.00mL溶液,用0.2000 mol∙L−1 NaOH标准溶液滴定至终点。重复实验,数据如下:
已知:常温下,Ka(CH3COOH)=1.8×10−5, =2.236
=2.236
(1)该市售醋酸的含量为______ g/100mL
(2)该市售醋酸c(H+)约等于______ (保留小数点后一位)
| 序号 | 滴定前读数/mL | 滴定终点读数/mL |
| 1 | 0.00 | 19.98 |
| 2 | 2.40 | 22.40 |
| 3 | 1.54 | 21.56 |
已知:常温下,Ka(CH3COOH)=1.8×10−5,
 =2.236
=2.236(1)该市售醋酸的含量为
(2)该市售醋酸c(H+)约等于
您最近一年使用:0次




