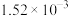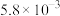下列是中学常见的物质:
①铜 ②亚硫酸 ③稀盐酸 ④氯化银 ⑤NH4HSO4 ⑥乙醇 ⑦冰醋酸 ⑧氨水 ⑨氢氧化钡溶液
回答下列问题:
(1)上述物质中能导电的是_______ (填写序号,下同),属于强电解质的是_______ ,属于弱电解质的是_______ 。
(2)分别写出②、⑤在水溶液中的电离方程式:_______ ,_______ 。
(3)写出⑦与⑧在水溶液中混合时的离子反应方程式:_______ 。
(4)向10ml 0.1mol/L醋酸溶液中加入蒸馏水,将其稀释到1L后,下列说法中不正确的是_______。
①铜 ②亚硫酸 ③稀盐酸 ④氯化银 ⑤NH4HSO4 ⑥乙醇 ⑦冰醋酸 ⑧氨水 ⑨氢氧化钡溶液
回答下列问题:
(1)上述物质中能导电的是
(2)分别写出②、⑤在水溶液中的电离方程式:
(3)写出⑦与⑧在水溶液中混合时的离子反应方程式:
(4)向10ml 0.1mol/L醋酸溶液中加入蒸馏水,将其稀释到1L后,下列说法中不正确的是_______。
| A.CH3COOH的电离程度增大 | B.c(CH3COO-)增大 |
| C.H+数目增多 | D. 减小 减小 |
更新时间:2022-11-04 17:42:34
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】按要求填空。
Ⅰ.现有以下物质:① 晶体 ②液态
晶体 ②液态 ③
③ 固体 ④熔融
固体 ④熔融 ⑤蔗糖 ⑥铜 ⑦
⑤蔗糖 ⑥铜 ⑦ ⑧
⑧ 溶液 ⑨淀粉溶液
溶液 ⑨淀粉溶液
(1)以上物质中能导电的是___________ ;
(2)属于电解质的是___________ ,属于非电解质的是___________ ;
(3)既不是电解质又不是非电解质的___________
Ⅱ.写出 的电离方程式:
的电离方程式:
(4) 在水溶液中电离:
在水溶液中电离:___________ ;
(5) 熔融状态下电离:
熔融状态下电离:___________ 。
Ⅲ.
(6) 的水溶液和淀粉溶液共同具备的性质是
的水溶液和淀粉溶液共同具备的性质是___________ (填序号)。
a.都不稳定,密封放置沉淀
b.都能产生丁达尔效应
c.分散质粒子可通过滤纸
(7) 的水溶液和淀粉溶液本质区别
的水溶液和淀粉溶液本质区别___________
Ⅰ.现有以下物质:①
 晶体 ②液态
晶体 ②液态 ③
③ 固体 ④熔融
固体 ④熔融 ⑤蔗糖 ⑥铜 ⑦
⑤蔗糖 ⑥铜 ⑦ ⑧
⑧ 溶液 ⑨淀粉溶液
溶液 ⑨淀粉溶液(1)以上物质中能导电的是
(2)属于电解质的是
(3)既不是电解质又不是非电解质的
Ⅱ.写出
 的电离方程式:
的电离方程式:(4)
 在水溶液中电离:
在水溶液中电离:(5)
 熔融状态下电离:
熔融状态下电离:Ⅲ.
(6)
 的水溶液和淀粉溶液共同具备的性质是
的水溶液和淀粉溶液共同具备的性质是a.都不稳定,密封放置沉淀
b.都能产生丁达尔效应
c.分散质粒子可通过滤纸
(7)
 的水溶液和淀粉溶液本质区别
的水溶液和淀粉溶液本质区别
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有下列几种物质:蔗糖、氯化钡固体、干冰、硫酸钡、纯碱、铁、盐酸、硝酸银溶液,按要求回答问题:
(1)难溶于水的电解质的是_______ 。
(2)写出纯碱在水中的电离方程式________________________ 。
(3)将足量的干冰升华后所得的气体通入烧碱溶液中,发生反应的离子方程式为____________ 。
(4)a、b、c、d是Na2CO3、BaCl2、盐酸、AgNO3四种溶液中的一种,现将它们两两混合,现象如下表所示:
①b是________ (用化学式填写),
②写出 a+c 反应的离子方程式________________________ 。
(1)难溶于水的电解质的是
(2)写出纯碱在水中的电离方程式
(3)将足量的干冰升华后所得的气体通入烧碱溶液中,发生反应的离子方程式为
(4)a、b、c、d是Na2CO3、BaCl2、盐酸、AgNO3四种溶液中的一种,现将它们两两混合,现象如下表所示:
| 反应物 | a+b | c+d | a+d | a+c | b+d |
| 现象 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 无色气体 |
①b是
②写出 a+c 反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】填空
(1)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为: 。该反应的还原剂是
。该反应的还原剂是________ ,氧化剂是________ 。
(2)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如:能帮助人体将食物中不易吸收的 转变为易吸收
转变为易吸收 ,这说明维生素C具有
,这说明维生素C具有________ (填“氧化性”或“还原性”)
(3)现有以下物质:①NaCl晶体;②干冰;③液态的醋酸;④铜;⑤ 固体;⑥蔗糖;⑦酒精;⑧熔融的
固体;⑥蔗糖;⑦酒精;⑧熔融的 ;⑨HCl。请回答下列问题(填序号)
;⑨HCl。请回答下列问题(填序号)
以上物质属于电解质的是________ ;以上物质属于非电解质的是________ 。
(4)用双线桥法标明电子转移的方向和数目:_____

(1)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:
 。该反应的还原剂是
。该反应的还原剂是(2)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如:能帮助人体将食物中不易吸收的
 转变为易吸收
转变为易吸收 ,这说明维生素C具有
,这说明维生素C具有(3)现有以下物质:①NaCl晶体;②干冰;③液态的醋酸;④铜;⑤
 固体;⑥蔗糖;⑦酒精;⑧熔融的
固体;⑥蔗糖;⑦酒精;⑧熔融的 ;⑨HCl。请回答下列问题(填序号)
;⑨HCl。请回答下列问题(填序号)以上物质属于电解质的是
(4)用双线桥法标明电子转移的方向和数目:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】科学研究中观察到的宏观现象能反映微观本质。例如,我们可以通过测定溶液导电能力来探查溶液中自由移动的离子浓度。某小组向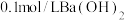 溶液中匀速滴加0.1mol/L稀硫酸,测得溶液导电能力的变化如图所示,回答下列问题:
溶液中匀速滴加0.1mol/L稀硫酸,测得溶液导电能力的变化如图所示,回答下列问题:

资料1:20℃时 溶解度为
溶解度为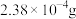 。
。
资料2:下表为20℃蒸馏水和饱和 溶液的电导率。
溶液的电导率。
注:电导率越大,溶液导电能力越强。
(1)硫酸的电离方程式是________ 。
(2)A~B段发生反应的化学方程式是________ 。
(3)关于图中的说法正确的是________(填字母)。
(4) 在水中的存在形式,同学们提出了不同的观点:
在水中的存在形式,同学们提出了不同的观点:
A只以 固体形式存在
固体形式存在
B.只以自由移动的 和
和 形式存在
形式存在
C.主要以 固体形式存在,同时存在极少量自由移动的
固体形式存在,同时存在极少量自由移动的 和
和
你支持观点________ (填字母)证据是________ (用文字和数据说明);由此可知,物质在水中的存在形式决定了其在离子方程式中能否写为离子形式。
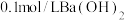 溶液中匀速滴加0.1mol/L稀硫酸,测得溶液导电能力的变化如图所示,回答下列问题:
溶液中匀速滴加0.1mol/L稀硫酸,测得溶液导电能力的变化如图所示,回答下列问题:
资料1:20℃时
 溶解度为
溶解度为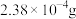 。
。资料2:下表为20℃蒸馏水和饱和
 溶液的电导率。
溶液的电导率。蒸馏水 | 饱和 | |
电导率(S/m) |
|
|
(1)硫酸的电离方程式是
(2)A~B段发生反应的化学方程式是
(3)关于图中的说法正确的是________(填字母)。
A.AB段溶液的导电能力不断减弱,说明生成的 不是电解质 不是电解质 |
| B.B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子 |
C.BC段溶液的导电能力不断增大,主要是由于过量的 电离出的离子导电 电离出的离子导电 |
D.a时刻 溶液与稀硫酸恰好完全中和 溶液与稀硫酸恰好完全中和 |
 在水中的存在形式,同学们提出了不同的观点:
在水中的存在形式,同学们提出了不同的观点:A只以
 固体形式存在
固体形式存在B.只以自由移动的
 和
和 形式存在
形式存在C.主要以
 固体形式存在,同时存在极少量自由移动的
固体形式存在,同时存在极少量自由移动的 和
和
你支持观点
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有下列物质①NaOH溶液;②铜丝;③液态HCl;④盐酸;⑤稀硫酸;⑥液氨;⑦酒精;⑧SO2;⑨BaSO4晶体;⑩熔融NaCl。
(1)上述状态下可导电的是__________ ;(填写数字序号,下同)
(2)属于非电解质的是________________ ;
(3)上述状态下属于强电解质不能导电的是__________ 。
(1)上述状态下可导电的是
(2)属于非电解质的是
(3)上述状态下属于强电解质不能导电的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)现在有下列10种物质:①H2O;②空气;③Mg;④CaO;⑤H2SO4;⑥Ca(OH)2;⑦CuSO4·5H2O;⑧碘酒;⑨无水乙醇;⑩NaHCO3。其中
属于混合物的是_______ (填序号,下同);
属于氧化物的是_______ ;属于碱的是_______ ;
属于酸的是_______ ;属于盐的是_______ 。
(2)以下几种物质:①干燥的食盐晶体;②液态氯化氢;③水银;④蔗糖;⑤KNO3溶液;⑥CO2;⑦熔融的KCl;⑧盐酸;⑨H2SO4。
以上物质中,能导电的是_______ (填序号,下同);属于电解质的是_______ ,属于非电解质的是_______ 。
(3)碳酸氢钠在水溶液中的电离方程式:_______ 。
属于混合物的是
属于氧化物的是
属于酸的是
(2)以下几种物质:①干燥的食盐晶体;②液态氯化氢;③水银;④蔗糖;⑤KNO3溶液;⑥CO2;⑦熔融的KCl;⑧盐酸;⑨H2SO4。
以上物质中,能导电的是
(3)碳酸氢钠在水溶液中的电离方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(Ⅰ)近年来我国对碳纳米管的研究也有了较大突破,即用电弧合成法来制碳纳米管,但往往有大量的碳纳米颗粒,需用氧化法来提纯这些颗粒,化学方程式为:
 (稀)
(稀) 
试回答下列问题:
(1)完成并配平上述反应的化学方程式_______ 。 (稀)
(稀)
(2)此反应的氧化剂是_______ ,被氧化的元素是_______ 。
(Ⅱ)把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl +N2
(3)发生化学反应的Cl2与NH3的分子数之比为:_______ ,反应中发生电子转移的Cl2与NH3的分子数之比为: _______ 。
(4)写出NH4Cl在溶液中的电离方程式_______ ,在其溶液中分散质粒子的直径范围为_______ 。
(5)若反应中有6.8克氨发生氧化反应,则反应中有生成氮气的质量为_______ 。
 (稀)
(稀) 
试回答下列问题:
(1)完成并配平上述反应的化学方程式
 (稀)
(稀)
(2)此反应的氧化剂是
(Ⅱ)把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl +N2
(3)发生化学反应的Cl2与NH3的分子数之比为:
(4)写出NH4Cl在溶液中的电离方程式
(5)若反应中有6.8克氨发生氧化反应,则反应中有生成氮气的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.下列三组物质中,均有一种物质的类别与其他三种不同。
① 、
、 、
、 、
、 ②
② 、
、 、
、 、
、 ③
③ 、
、 、
、 、
、
(1)三种物质依次是(填化学式):①______ ②______ ③______ 。
(2)这三种物质相互作用可生成一种新物质 ,该反应
,该反应______ (填“是”或“不是”)氧化还原反应。
Ⅱ.现有下列10种物质:①铝,②纯醋酸,③ ,④
,④ ,⑤
,⑤ ,⑥红褐色的氢氧化铁胶体,⑦稀盐酸,⑧
,⑥红褐色的氢氧化铁胶体,⑦稀盐酸,⑧ ,⑨碳酸钙,⑩乙醇
,⑨碳酸钙,⑩乙醇
(3)上述物质中属于电解质的是______ (填序号);属于酸性氧化物的是______ (填序号)。
(4)⑧在水中的电离方程式为:______ 。
(5)⑨和⑦混合,反应的离子方程式为:______ 。
(6)上述物质中有两种物质在水溶液中发生的反应可用离子反应 表示,请写出该离子反应对应的其中一个化学方程式
表示,请写出该离子反应对应的其中一个化学方程式______ 。
①
 、
、 、
、 、
、 ②
② 、
、 、
、 、
、 ③
③ 、
、 、
、 、
、
(1)三种物质依次是(填化学式):①
(2)这三种物质相互作用可生成一种新物质
 ,该反应
,该反应Ⅱ.现有下列10种物质:①铝,②纯醋酸,③
 ,④
,④ ,⑤
,⑤ ,⑥红褐色的氢氧化铁胶体,⑦稀盐酸,⑧
,⑥红褐色的氢氧化铁胶体,⑦稀盐酸,⑧ ,⑨碳酸钙,⑩乙醇
,⑨碳酸钙,⑩乙醇(3)上述物质中属于电解质的是
(4)⑧在水中的电离方程式为:
(5)⑨和⑦混合,反应的离子方程式为:
(6)上述物质中有两种物质在水溶液中发生的反应可用离子反应
 表示,请写出该离子反应对应的其中一个化学方程式
表示,请写出该离子反应对应的其中一个化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知25℃时部分弱电解质的电离平衡常数如表所示,请回答下列问题:
(1) 的第二级电离平衡常数的表达式
的第二级电离平衡常数的表达式
_______ 。
(2)一般情况下,当温度升高时,K_______ (填“增大”、“减小”或“不变”)。
(3)下列方法中,可以使
 溶液中
溶液中 电离程度增大的是_______。
电离程度增大的是_______。
(4)向 溶液中加入足量的
溶液中加入足量的 溶液,反应的离子方程式为
溶液,反应的离子方程式为_______ 。
(5)现取20mLpH=3的 溶液,加入
溶液,加入 的氨水,测得溶液导电性变化如图,则加入氨水前
的氨水,测得溶液导电性变化如图,则加入氨水前 的电离度为
的电离度为_______ 。

| 物质 |  |  |  |  |
| 电离常数(K) |  |  |   |   |
(1)
 的第二级电离平衡常数的表达式
的第二级电离平衡常数的表达式
(2)一般情况下,当温度升高时,K
(3)下列方法中,可以使

 溶液中
溶液中 电离程度增大的是_______。
电离程度增大的是_______。A.通入少量 | B.加入少量冰醋酸 |
| C.加入少量醋酸钠固体 | D.加入少量水 |
 溶液中加入足量的
溶液中加入足量的 溶液,反应的离子方程式为
溶液,反应的离子方程式为(5)现取20mLpH=3的
 溶液,加入
溶液,加入 的氨水,测得溶液导电性变化如图,则加入氨水前
的氨水,测得溶液导电性变化如图,则加入氨水前 的电离度为
的电离度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)甲溶液的pH是4,乙溶液的pH是5,甲溶液与乙溶液的c(H+)之比为_____ 。
A.10∶1 B.1∶10 C.2∶1 D.1∶2
(2)向0.1mol•L﹣1氨水溶液中加入少量的NH4Cl晶体时,会引起溶液中的_____ 。
A.pH增大 B.Kw减小 C.c(NH )减小 D.c(NH3•H2O)增大
)减小 D.c(NH3•H2O)增大
(3)在某温度下的水溶液中,c(H+)=1.0×10xmol/L,c(OH﹣)=1.0×10ymol/L,x与y的关系如图所示。 该温度下,当Fe3+ (Ksp[Fe(OH)3]=8.0×10﹣38)完全生成沉淀时,溶液pH 约为_____ 。( lg5≈0.7 )

A.3.3 B.5.7 C.4.3 D.10.7
(4)室温下,若溶液中水电离产生的c(OH﹣)=1.0×10﹣13mol•L﹣1,则该溶液的溶质可能是_____ 。
A.KNO3 B.HCl C.NH4Cl D.Na2CO3
(5)将下列物质的水溶液加热蒸干、再灼烧,最终能得到原物质的是_____ 。
A.AlCl3 B.NaHCO3 C.Na2SO3 D.Al2(SO4)3
A.10∶1 B.1∶10 C.2∶1 D.1∶2
(2)向0.1mol•L﹣1氨水溶液中加入少量的NH4Cl晶体时,会引起溶液中的
A.pH增大 B.Kw减小 C.c(NH
 )减小 D.c(NH3•H2O)增大
)减小 D.c(NH3•H2O)增大(3)在某温度下的水溶液中,c(H+)=1.0×10xmol/L,c(OH﹣)=1.0×10ymol/L,x与y的关系如图所示。 该温度下,当Fe3+ (Ksp[Fe(OH)3]=8.0×10﹣38)完全生成沉淀时,溶液pH 约为

A.3.3 B.5.7 C.4.3 D.10.7
(4)室温下,若溶液中水电离产生的c(OH﹣)=1.0×10﹣13mol•L﹣1,则该溶液的溶质可能是
A.KNO3 B.HCl C.NH4Cl D.Na2CO3
(5)将下列物质的水溶液加热蒸干、再灼烧,最终能得到原物质的是
A.AlCl3 B.NaHCO3 C.Na2SO3 D.Al2(SO4)3
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某小组探究 的性质。
的性质。
(1) 时,测得
时,测得 溶液的pH为2.88,
溶液的pH为2.88, 溶液的pH为x。
溶液的pH为x。
① 的电离方程式是
的电离方程式是__________ 。
②x的值最有可能是以下选项中的_________ (填字母)。
a.1.88 b.2.38 c.3.38 d.3.88
③将 溶液加水稀释,
溶液加水稀释, 的比值将
的比值将_______ (填“变大”、 “不变”或“变小”)。
(2)查阅资料, 时,几种弱酸的电离常数如下表
时,几种弱酸的电离常数如下表
①推测 时下列反应可能发生的是
时下列反应可能发生的是_________ (填字母)。
a.
b.
c.
②浓度均为 的
的 、
、 、
、 溶液中,pH最大的是
溶液中,pH最大的是____ (填化学式)。
 的性质。
的性质。(1)
 时,测得
时,测得 溶液的pH为2.88,
溶液的pH为2.88, 溶液的pH为x。
溶液的pH为x。①
 的电离方程式是
的电离方程式是②x的值最有可能是以下选项中的
a.1.88 b.2.38 c.3.38 d.3.88
③将
 溶液加水稀释,
溶液加水稀释, 的比值将
的比值将(2)查阅资料,
 时,几种弱酸的电离常数如下表
时,几种弱酸的电离常数如下表| 弱酸种类 |  |  |  |
电离常数 |  |  |  |
 时下列反应可能发生的是
时下列反应可能发生的是a.

b.

c.

②浓度均为
 的
的 、
、 、
、 溶液中,pH最大的是
溶液中,pH最大的是
您最近一年使用:0次