回答下列问题:
(1)下列变化中,涉及氧化还原反应的是_______ (填序号)。
①金属的冶炼 ②钢铁的锈蚀 ③食物的腐败 ④钟乳石的形成
(2)野外焊接铁轨常常采用铝热反应。已知铝热反应的化学方程式为 ,该反应所属基本反应类型是
,该反应所属基本反应类型是_______ (填4种基本反应类型中的一种),在反应中铁元素的化合价_______ (填“升高”或“降低”),该元素的原子_______ (填“失去”或“得到”)电子。该反应还原剂是_______ (填化学式,下同),氧化剂是_______ 。
(3)阅读下列材料,回答有关问题:一个体重50kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+转变成Fe2+,有利于人体吸收。
①在人体中进行Fe2+ 到Fe3+的转化时,其中的Fe2+作_______ 剂(填“氧化”或“还原”)。
②“服用维生素C,可使食物中的Fe3+转变成Fe2+”这句话指出,维生素C在这一反应中具_______ 性。(填“氧化”或“还原”)
(1)下列变化中,涉及氧化还原反应的是
①金属的冶炼 ②钢铁的锈蚀 ③食物的腐败 ④钟乳石的形成
(2)野外焊接铁轨常常采用铝热反应。已知铝热反应的化学方程式为
 ,该反应所属基本反应类型是
,该反应所属基本反应类型是(3)阅读下列材料,回答有关问题:一个体重50kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+转变成Fe2+,有利于人体吸收。
①在人体中进行Fe2+ 到Fe3+的转化时,其中的Fe2+作
②“服用维生素C,可使食物中的Fe3+转变成Fe2+”这句话指出,维生素C在这一反应中具
更新时间:2022-11-02 11:09:17
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】完成下列填空
(1)在3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O反应中,___________ 是氧化剂;___________ 元素被氧化;被还原的HNO3与参加反应的HNO3个数之比是___________ 。
(2)下列物质:①H2②铝③蔗糖④CO2⑤纯H2SO4⑥Ba(OH)2固体⑦稀硝酸⑧熔融Al2(SO4)3
①上述状态下可导电的是___________ ;(填序号,下同)属于电解质的是___________ ;
②上述物质中有两种物质之间可发生离子反应: ,对应的化学方程式为
,对应的化学方程式为___________ 。
(1)在3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O反应中,
(2)下列物质:①H2②铝③蔗糖④CO2⑤纯H2SO4⑥Ba(OH)2固体⑦稀硝酸⑧熔融Al2(SO4)3
①上述状态下可导电的是
②上述物质中有两种物质之间可发生离子反应:
 ,对应的化学方程式为
,对应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列问题。
(1)储氢纳米碳管研究成功体现了科技的进步。但用电弧法合成的碳纳米管常伴有大量的杂质一碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应方程式: 。
。
请回答下列问题:
①此反应的氧化剂是___________ ,氧化产物是___________ 。
② 在上述反应中表现出来的性质是
在上述反应中表现出来的性质是___________ (填选项序号)。
A.酸性 B.氧化性 C.吸水性 D.脱水性
已知碳与浓硫酸在加热条件下反应生成 、
、 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式_______ 。
(2)饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,其化学方程式为:
,其化学方程式为: 。请回答下列问题:
。请回答下列问题:
①上述反应中,被氧化的元素___________ ,还原产物是___________ 。
②用双线桥法表示反应中电子转移的方向和数目:___________ 。
③请配平下列离子方程式:



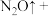
 ,
,___________ 。
(3)写出下列反应的离子方程式:
①用食醋除去水垢(水垢的主要成分为碳酸钙)___________ 。
②氢氧化铁溶于稀硫酸___________ 。
③硫酸铝溶液中加入氨水___________ 。
④钠与水的反应___________ 。
⑤在碱性条件下, 可将废水中的
可将废水中的 ,氧化为无毒的
,氧化为无毒的 、
、
___________ 。
(1)储氢纳米碳管研究成功体现了科技的进步。但用电弧法合成的碳纳米管常伴有大量的杂质一碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应方程式:
 。
。请回答下列问题:
①此反应的氧化剂是
②
 在上述反应中表现出来的性质是
在上述反应中表现出来的性质是A.酸性 B.氧化性 C.吸水性 D.脱水性
已知碳与浓硫酸在加热条件下反应生成
 、
、 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式(2)饮用水中的
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,其化学方程式为:
,其化学方程式为: 。请回答下列问题:
。请回答下列问题:①上述反应中,被氧化的元素
②用双线桥法表示反应中电子转移的方向和数目:
③请配平下列离子方程式:




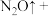
 ,
,(3)写出下列反应的离子方程式:
①用食醋除去水垢(水垢的主要成分为碳酸钙)
②氢氧化铁溶于稀硫酸
③硫酸铝溶液中加入氨水
④钠与水的反应
⑤在碱性条件下,
 可将废水中的
可将废水中的 ,氧化为无毒的
,氧化为无毒的 、
、
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】酒后驾车是马路第一杀手。已知酒精(C2H5OH)能与K2Cr2O7和H2SO4的混合溶液在一定条件下发生反应: 2K2Cr2O7+3C2H5OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O, 且知 Cr2O 和Cr3+在溶液中分别显橙色和绿色。回答下列问题:
和Cr3+在溶液中分别显橙色和绿色。回答下列问题:
(1)该反应_______ (填“是”或“不是”)氧化还原反应,判断的依据是_______ 。
(2)将上述化学方程式改写成离子方程式_______ 。
(3)能否用这一反应来检测司机是否酒后驾车_______ (填“能” 或“否”),理由是_______ 。
 和Cr3+在溶液中分别显橙色和绿色。回答下列问题:
和Cr3+在溶液中分别显橙色和绿色。回答下列问题:(1)该反应
(2)将上述化学方程式改写成离子方程式
(3)能否用这一反应来检测司机是否酒后驾车
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】“佛立苏”是一种常见补血剂,主要成分为FeSO4;FeSO4·7H2O俗称“绿矾”,在工业生产和日常生活中都有广泛的用途,回答下列问题:
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是______ (填字母)。
A.亚硝酸盐被还原B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+D.亚硝酸盐是还原剂
(2)已知Fe(OH)2是一种白色沉淀,极易被空气中的氧气氧化,反应的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3(红褐色沉淀),用双线桥法表示转移电子数和氧化还原反应______ 。
向FeSO4溶液中加入一小块金属钠,发现开始有气体和白色沉淀产生,过一段时间,白色沉淀变为红褐色,写出上述反应中涉及到的离子方程式________________________________ 。
(3)FeSO4可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾(K2FeO4),氧化性比Cl2、O2、ClO2、KMnO4更强,主要反应:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。
①上述反应中作还原剂的是______ (填化学式)。
②简要说明K2FeO4作为水处理剂时所起的作用____________ (写出一点即可)。
(4)将Na2O2固体加入酚酞溶液中产生的现象是_______ 。写出该反应的离子方程式______ 。
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是
A.亚硝酸盐被还原B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+D.亚硝酸盐是还原剂
(2)已知Fe(OH)2是一种白色沉淀,极易被空气中的氧气氧化,反应的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3(红褐色沉淀),用双线桥法表示转移电子数和氧化还原反应
向FeSO4溶液中加入一小块金属钠,发现开始有气体和白色沉淀产生,过一段时间,白色沉淀变为红褐色,写出上述反应中涉及到的离子方程式
(3)FeSO4可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾(K2FeO4),氧化性比Cl2、O2、ClO2、KMnO4更强,主要反应:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。
①上述反应中作还原剂的是
②简要说明K2FeO4作为水处理剂时所起的作用
(4)将Na2O2固体加入酚酞溶液中产生的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】完成下列问题。
(1)氧化还原反应的本质是_______ ,通常可用元素化合价的升降来判断氧化剂、还原剂。所含元素化合价升高的物质是_______ 剂,发生_______ 反应。在 反应中,
反应中,_______ 是氧化剂,_______ 是还原剂,_______ 元素被氧化,_______ 元素被还原,氧化产物是_______ 。
(2)在 、
、 、
、 、
、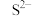 、S中,只有氧化性的是
、S中,只有氧化性的是_______ ,只有还原性的是_______ 即有氧化性又有还原性的是_______ 。
(1)氧化还原反应的本质是
 反应中,
反应中,(2)在
 、
、 、
、 、
、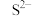 、S中,只有氧化性的是
、S中,只有氧化性的是
您最近一年使用:0次
【推荐2】氧化还原反应原理在生产,生活和科学研究中应用广泛。回答下列问题:
(1)误食 会导致血红蛋白中的
会导致血红蛋白中的 转化为
转化为 而中毒,可服用维生素C解毒。下列分析正确的是
而中毒,可服用维生素C解毒。下列分析正确的是_______ (填字母)
A. 被氧化 B. 维生素C有还原性 C.
被氧化 B. 维生素C有还原性 C. 是还原剂
是还原剂
(2)针对以下A~D四个涉及 的反应(未配平)填空:
的反应(未配平)填空:
A.
B.
C.
D.
① 仅体现还原性的反应是
仅体现还原性的反应是_______ (填字母,下同) 既体现氧化性,又体现还原性的反应是
既体现氧化性,又体现还原性的反应是_______  既不做氧化剂又不做还原剂的反应是
既不做氧化剂又不做还原剂的反应是_______ 。
② 有时可作为矿业废液的消毒剂,有“绿色氧化剂”的美称,如消除采矿业废液中的氧化物(如KCN),经以下反应实现
有时可作为矿业废液的消毒剂,有“绿色氧化剂”的美称,如消除采矿业废液中的氧化物(如KCN),经以下反应实现 ,则生成物A的化学式为
,则生成物A的化学式为_______ , 被称为“绿色氧化剂”的理由是
被称为“绿色氧化剂”的理由是_______ 。
(3)在 的反应中,氧化剂是
的反应中,氧化剂是_______ ,氧化反应的产物是_______ ,假设有56gFe与足量稀硝酸反应,生成的NO为_______ g。
(1)误食
 会导致血红蛋白中的
会导致血红蛋白中的 转化为
转化为 而中毒,可服用维生素C解毒。下列分析正确的是
而中毒,可服用维生素C解毒。下列分析正确的是A.
 被氧化 B. 维生素C有还原性 C.
被氧化 B. 维生素C有还原性 C. 是还原剂
是还原剂(2)针对以下A~D四个涉及
 的反应(未配平)填空:
的反应(未配平)填空:A.

B.

C.

D.

①
 仅体现还原性的反应是
仅体现还原性的反应是 既体现氧化性,又体现还原性的反应是
既体现氧化性,又体现还原性的反应是 既不做氧化剂又不做还原剂的反应是
既不做氧化剂又不做还原剂的反应是②
 有时可作为矿业废液的消毒剂,有“绿色氧化剂”的美称,如消除采矿业废液中的氧化物(如KCN),经以下反应实现
有时可作为矿业废液的消毒剂,有“绿色氧化剂”的美称,如消除采矿业废液中的氧化物(如KCN),经以下反应实现 ,则生成物A的化学式为
,则生成物A的化学式为 被称为“绿色氧化剂”的理由是
被称为“绿色氧化剂”的理由是(3)在
 的反应中,氧化剂是
的反应中,氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)如图为氯及其化合物的“价—类”二维图。

①填写二维图缺失的类别A_______ 和化学式B_______ 。
②某同学利用以下试剂研究HCl性质,进行了如下预测:
a.NaClO b. Fe c.NaOH d.KMnO4 e.CuO
从物质类别上看,HCl属于_______ ,可能与_______ 发生反应(填序号);
从化合价角度看,Cl-具有_______ 性,可能与_______ 发生反应(填序号)。
(2)①含有3.01×1023个H2SO4分子中含原子的数为_______ ,该H2SO4的质量为_______ g。
②12.4g Na2X含0.4mol Na+ ,则 Na2X的摩尔质量为_______ ,Na2X的化学式为_______ 。
③实验室用250mL一定物质的量浓度的稀硫酸与足量的铁屑反应,已知制得氢气标准状况下的体积为5.6L,计算参加反应的硫酸的物质的量浓度是_______ (要求写出计算步骤)。
(1)如图为氯及其化合物的“价—类”二维图。

①填写二维图缺失的类别A
②某同学利用以下试剂研究HCl性质,进行了如下预测:
a.NaClO b. Fe c.NaOH d.KMnO4 e.CuO
从物质类别上看,HCl属于
从化合价角度看,Cl-具有
(2)①含有3.01×1023个H2SO4分子中含原子的数为
②12.4g Na2X含0.4mol Na+ ,则 Na2X的摩尔质量为
③实验室用250mL一定物质的量浓度的稀硫酸与足量的铁屑反应,已知制得氢气标准状况下的体积为5.6L,计算参加反应的硫酸的物质的量浓度是
您最近一年使用:0次
【推荐1】回答下列问题:
(1)请配平以下的氧化还原方程式:。
①□ □
□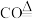 □
□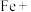 □
□
______
②□ □
□ □
□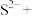 □
□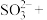 □
□
______
③□ □
□ □_______=□
□_______=□ □
□ □
□ (缺了一种反应物)
(缺了一种反应物)________
(2)已知还原性强弱顺序是 ,向含有
,向含有 、
、 、
、 的溶液中通入氯气,先被氧化的离子是
的溶液中通入氯气,先被氧化的离子是___________ 。
(3)高铁酸钠(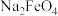 )被公认为绿色净水剂,比
)被公认为绿色净水剂,比 、
、 ,
, 氧化性更强,无二次污染:
氧化性更强,无二次污染:
①干法制备高铁酸钠的主要反应为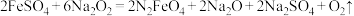 ,该反应中的氧化剂为
,该反应中的氧化剂为___________ ,氧化产物为___________ 。
②除了干法制备高铁酸钠,还可用湿法制备高铁酸钠,其反应物和生成物共有七种微粒: 、
、 、
、 、
、 、
、 、
、 、
、 ,写出该反应的离子方程式:
,写出该反应的离子方程式:___________ 。
(1)请配平以下的氧化还原方程式:。
①□
 □
□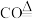 □
□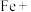 □
□
②□
 □
□ □
□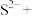 □
□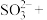 □
□
③□
 □
□ □_______=□
□_______=□ □
□ □
□ (缺了一种反应物)
(缺了一种反应物)(2)已知还原性强弱顺序是
 ,向含有
,向含有 、
、 、
、 的溶液中通入氯气,先被氧化的离子是
的溶液中通入氯气,先被氧化的离子是(3)高铁酸钠(
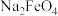 )被公认为绿色净水剂,比
)被公认为绿色净水剂,比 、
、 ,
, 氧化性更强,无二次污染:
氧化性更强,无二次污染:①干法制备高铁酸钠的主要反应为
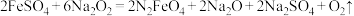 ,该反应中的氧化剂为
,该反应中的氧化剂为②除了干法制备高铁酸钠,还可用湿法制备高铁酸钠,其反应物和生成物共有七种微粒:
 、
、 、
、 、
、 、
、 、
、 、
、 ,写出该反应的离子方程式:
,写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】常见的发生氧化还原反应的离子
①MnO (H+)与
(H+)与_______ 等。
②NO (H+)与
(H+)与_______ 等。
③ClO-与_______ 等。
④Fe3+与_______ 等。
①MnO
 (H+)与
(H+)与②NO
 (H+)与
(H+)与③ClO-与
④Fe3+与
您最近一年使用:0次
【推荐3】反应体系中共有6种物质:MnSO4、KMnO4、K2SO4、SO2、H2SO4和H2O。其中SO2的还原性最强,KMnO4的氧化性最强。对此反应体系,请回答以下问题:
(1)请用这6种物质组成一个合理的化学反应,写出它的化学方程式并配平_______ 。
(2)反应中发生还原反应的过程是_____ → _____ ;被氧化的元素是_____ 。
(3)反应中的H2SO4是_________ (填编号)。
a. 还原剂 b. 反应物 c. 生成物 d. 氧化产物
(4)标准状况下,当有4.48 L SO2气体参加反应时,电子转移数目是______________ 个。
(5)反应过程中,物质的导电性逐渐_____ (填“增强”、“不变”或“减弱”),原因是____ 。
(1)请用这6种物质组成一个合理的化学反应,写出它的化学方程式并配平
(2)反应中发生还原反应的过程是
(3)反应中的H2SO4是
a. 还原剂 b. 反应物 c. 生成物 d. 氧化产物
(4)标准状况下,当有4.48 L SO2气体参加反应时,电子转移数目是
(5)反应过程中,物质的导电性逐渐
您最近一年使用:0次

 ;②
;②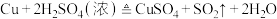 。请回答:
。请回答: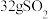 气体时,消耗
气体时,消耗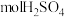 被还原,转移电子数目为
被还原,转移电子数目为

