下列依据热化学方程式得出的结论正确的是
| 选项 | 热化学方程式 | 结论 |
| A |   | 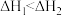 |
| B |  | P(s,白磷)比P(s,红磷)稳定 |
| C |  |  的燃烧热( 的燃烧热( )为 )为 |
| D |  | 将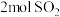 和 和 混合并充分反应,放出的热量为 混合并充分反应,放出的热量为 |
| A.A | B.B | C.C | D.D |
更新时间:2022-11-12 09:23:23
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】一些烷烃的燃烧热如下表:
下列表达正确的是
| 化合物 | 燃烧热/kJ·mol-1 | 化合物 | 燃烧热/kJ·mol-1 |
| 甲烷 | 891.0 | 正丁烷 | 2 878.0 |
| 乙烷 | 1 560.8 | 异丁烷 | 2 869.6 |
| 丙烷 | 2 221.5 | 2-甲基丁烷 | 3 531.3 |
下列表达正确的是
| A.正戊烷的燃烧热小于3531.3 kJ·mol-1 |
| B.稳定性:正丁烷<异丁烷 |
| C.乙烷的燃烧热化学方程式为:2C2H6(g)+7O2(g)=4CO2(g)+6H2O(g) ΔH=-1 560.8 kJ·mol-1 |
| D.相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列说法不正确的是( )
| A.核能、太阳能、氢能都是新能源 |
| B.已知反应 C(s,石墨)===C(s,金刚石)为吸热反应,可得结论:石墨比金刚石更稳定 |
| C.“开发利用新能源”“汽车尾气催化净化”都能提高空气质量 |
| D.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量更多 |
您最近一年使用:0次
【推荐1】下列依据热化学方程式得出的结论正确的是
| A.若C(石墨,s)=C(金刚石,s) ΔH>0,则石墨比金刚石稳定 |
| B.已知2SO2(g)+O2(g)⇌ 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 |
C.由C(s)+ O2(g)=CO(g)ΔH=+110.5kJ·mol-1,可知碳的燃烧热为110.5kJ·mol-1 O2(g)=CO(g)ΔH=+110.5kJ·mol-1,可知碳的燃烧热为110.5kJ·mol-1 |
| D.已知2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1>ΔH2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】胶状液氢(主要成分是 和
和 )有望用于未来的运载火箭和空间运输系统。实验测得:
)有望用于未来的运载火箭和空间运输系统。实验测得: 时,
时,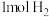 完全燃烧生成液态水,放出
完全燃烧生成液态水,放出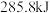 热量;
热量;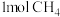 完全燃烧生成液态水和
完全燃烧生成液态水和 ,放出
,放出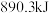 的热量。下列热化学方程式的书写中正确的是
的热量。下列热化学方程式的书写中正确的是
 和
和 )有望用于未来的运载火箭和空间运输系统。实验测得:
)有望用于未来的运载火箭和空间运输系统。实验测得: 时,
时,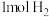 完全燃烧生成液态水,放出
完全燃烧生成液态水,放出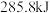 热量;
热量;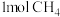 完全燃烧生成液态水和
完全燃烧生成液态水和 ,放出
,放出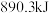 的热量。下列热化学方程式的书写中正确的是
的热量。下列热化学方程式的书写中正确的是A. 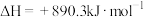 |
B. 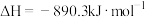 |
C. 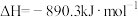 |
D. 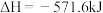 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】下列关于热化学反应的描述中正确的是
| A.若S(s)+O2(g)=SO2(g) ΔH1,S(g)+O2(g)=SO2(g) ΔH2,则ΔH1>ΔH2 |
B.燃料电池中将甲醇蒸气转化为氢气的热化学方程式是:CH3OH(g)+ O2(g)=CO2(g)+2H2(g) ΔH=-192.9kJ∙mol-1,则CH3OH(g)的燃烧热为192.9kJ∙mol-1 O2(g)=CO2(g)+2H2(g) ΔH=-192.9kJ∙mol-1,则CH3OH(g)的燃烧热为192.9kJ∙mol-1 |
| C.已知P4(白磷,s)=4P(红磷,s)ΔH<0,则白磷比红磷稳定 |
| D.化学键是指:生成1mol化学键时放出的热量,H-H:436kJ∙mol-1;Cl-Cl:243kJ∙mol-1;H-Cl:431kJ∙mol-1;则 H2(g)+Cl2(g)=2HCl(g) ΔH=247kJ∙mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】化学反应过程中既有物质的变化,又有能量的变化。关于下列热化学方程式的说法中,正确的是
(1)2H2(g) + O2(g) = 2H2O(g) △H1
(2)2H2(g) + O2(g) = 2H2O(l) △H2
(1)2H2(g) + O2(g) = 2H2O(g) △H1
(2)2H2(g) + O2(g) = 2H2O(l) △H2
| A.△H1 < △H2 | B.△H1 > △H2 |
| C.△H1 = △H2 | D.不能判断△H1与△H2的相对大小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】相同条件下,下列比较前者大于后者的是
A.熵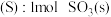 , , |
B.熵变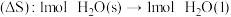 , , |
C.焓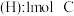 (s,石墨), (s,石墨), (s,金刚石) (s,金刚石) |
D.焓变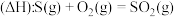 , , |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】25℃、101 kPa下,1 mol 氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是
| A.2H 2 (g) + O 2 (g) = 2H2O(1) △ H = -285.8kJ/mol |
| B.2H2 (g) + O2 (g) = 2H2O(1) △ H = +571.6 kJ/mol |
| C.2H2 (g) + O 2 (g) = 2H2O(g) △ H = -571.6 kJ/mol |
D.H2 (g) + O2 (g) = H2O(1) △ H = -285.8kJ/mol O2 (g) = H2O(1) △ H = -285.8kJ/mol |
您最近一年使用:0次



