某化合物A(由三种元素构成),为了探究其组成,进行了如下实验:
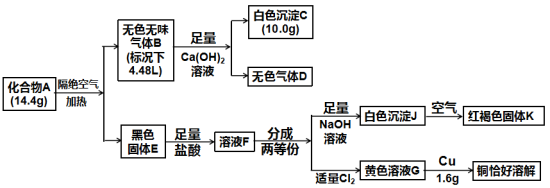
已知:气体D在标准状况下的密度为1.25g/L。试回答:
(1)白色沉淀C的化学式为_______ ,化合物A的化学式为_______ 。
(2)请写出白色沉淀J变成红褐色固体K的化学方程式_______ 。
(3)请写出溶液F中金属阳离子的检验方法_______ 。

已知:气体D在标准状况下的密度为1.25g/L。试回答:
(1)白色沉淀C的化学式为
(2)请写出白色沉淀J变成红褐色固体K的化学方程式
(3)请写出溶液F中金属阳离子的检验方法
20-21高一上·浙江湖州·阶段练习 查看更多[3]
更新时间:2022/10/30 20:34:53
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】某兴趣小组对化合物X开展探究实验。
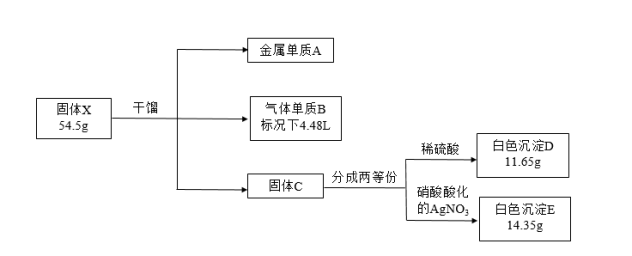
已知X是由三种元素组成的盐,金属单质A银白色常用于实验室做焰色反应实验,不溶于硝酸;气体B在标准状况下的密度为3.17 g/L;所加试剂均足量。
(1)X的化学式___________ ,固体C的电子式___________ 。
(2)金属A溶于王水(浓硝酸:浓盐酸=1:3)生成化合物X对应的酸和遇空气显红棕色的气体,写出金属A溶于王水的化学方程式___________ 。
(3)与B中元素同主族元素之间形成的化合物的性质与气体单质B相似,在碱性环境中,XO-→X-+XO ,非金属性越弱该反应越容易发生。写出该族第四周期与第五周期元素形成的化合物YZ与氢氧化钠溶液反应的离子方程式
,非金属性越弱该反应越容易发生。写出该族第四周期与第五周期元素形成的化合物YZ与氢氧化钠溶液反应的离子方程式___________ 。
(4)下列有关说法正确的是___________ 。
A.用金属A做焰色反应实验时,需用稀硫酸洗净
B.某试剂做焰色反应实验时,火焰黄色,证明一定有钠盐,但不一定有钾盐。
C.工业上使用阴离子交换膜电解饱和食盐水生产气体B
D.白色固体D可用于医疗上检查肠胃的内服药剂
E.白色沉淀E在光照下颜色会变深,可能溶于氨水

已知X是由三种元素组成的盐,金属单质A银白色常用于实验室做焰色反应实验,不溶于硝酸;气体B在标准状况下的密度为3.17 g/L;所加试剂均足量。
(1)X的化学式
(2)金属A溶于王水(浓硝酸:浓盐酸=1:3)生成化合物X对应的酸和遇空气显红棕色的气体,写出金属A溶于王水的化学方程式
(3)与B中元素同主族元素之间形成的化合物的性质与气体单质B相似,在碱性环境中,XO-→X-+XO
 ,非金属性越弱该反应越容易发生。写出该族第四周期与第五周期元素形成的化合物YZ与氢氧化钠溶液反应的离子方程式
,非金属性越弱该反应越容易发生。写出该族第四周期与第五周期元素形成的化合物YZ与氢氧化钠溶液反应的离子方程式(4)下列有关说法正确的是
A.用金属A做焰色反应实验时,需用稀硫酸洗净
B.某试剂做焰色反应实验时,火焰黄色,证明一定有钠盐,但不一定有钾盐。
C.工业上使用阴离子交换膜电解饱和食盐水生产气体B
D.白色固体D可用于医疗上检查肠胃的内服药剂
E.白色沉淀E在光照下颜色会变深,可能溶于氨水
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知某溶液中可能含有 、Cl-、
、Cl-、 、
、 、
、 、Fe3+、Al3+和K+中的几种,且所含阴离子的物质的量相等。为确定该溶液的成分,某学习小组做了如下实验:
、Fe3+、Al3+和K+中的几种,且所含阴离子的物质的量相等。为确定该溶液的成分,某学习小组做了如下实验:
①取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;
②将沉淀过滤、洗涤、灼烧,得到1.6 g固体;
③向上述滤液中加入足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。
请回答下列问题:
(1)结合①和②,判断原溶液中肯定含有的离子是______ ,可以排除的离子是_______ 。
(2)由③推知原溶液中一定有____ 离子,其物质的量为_____ mol。
(3)综合(1)、(2)及题干信息,结合溶液中电荷守恒知识,还可以排除的离子是____ 。该学习小组最终得出结论:该溶液由____ 种阳离子(填数字,下同)和____ 种阴离子组成。
 、Cl-、
、Cl-、 、
、 、
、 、Fe3+、Al3+和K+中的几种,且所含阴离子的物质的量相等。为确定该溶液的成分,某学习小组做了如下实验:
、Fe3+、Al3+和K+中的几种,且所含阴离子的物质的量相等。为确定该溶液的成分,某学习小组做了如下实验:①取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;
②将沉淀过滤、洗涤、灼烧,得到1.6 g固体;
③向上述滤液中加入足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。
请回答下列问题:
(1)结合①和②,判断原溶液中肯定含有的离子是
(2)由③推知原溶液中一定有
(3)综合(1)、(2)及题干信息,结合溶液中电荷守恒知识,还可以排除的离子是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】将下列离子 K+、Na+、Cu2+、H+、 、Cl-、
、Cl-、 、OH-按可能大量共存于同一溶液的情况,把它们分成 A、B 两组,每组中均含两种阳离子和两种阴离子。若在A 中滴入石蕊溶液,可观察到溶液从无色变为红色;若向 B中滴入酚酞试剂,可观察到溶液从无色变为红色。则:
、OH-按可能大量共存于同一溶液的情况,把它们分成 A、B 两组,每组中均含两种阳离子和两种阴离子。若在A 中滴入石蕊溶液,可观察到溶液从无色变为红色;若向 B中滴入酚酞试剂,可观察到溶液从无色变为红色。则:
A组一定含有的离子为__________ ,其余三种离子可能为__________ 。
B组一定含有的离子为__________ ,一定不含_________ 。
 、Cl-、
、Cl-、 、OH-按可能大量共存于同一溶液的情况,把它们分成 A、B 两组,每组中均含两种阳离子和两种阴离子。若在A 中滴入石蕊溶液,可观察到溶液从无色变为红色;若向 B中滴入酚酞试剂,可观察到溶液从无色变为红色。则:
、OH-按可能大量共存于同一溶液的情况,把它们分成 A、B 两组,每组中均含两种阳离子和两种阴离子。若在A 中滴入石蕊溶液,可观察到溶液从无色变为红色;若向 B中滴入酚酞试剂,可观察到溶液从无色变为红色。则:A组一定含有的离子为
B组一定含有的离子为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A∼I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。
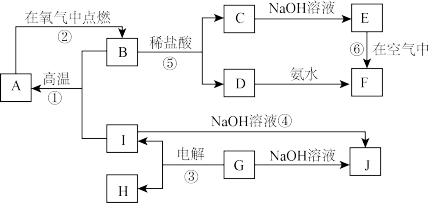
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中位置第___________ 周期、第___________ 族;
(2)写出反应①的化学方程式:___________ ;
(3)写出反应⑥的化学方程式:___________ ;
(4)写出反应③的电极方程式:阳极:___________ ;阴极:___________ 。
(5)J的化学式:___________ ,H的结构式:___________ 。

请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中位置第
(2)写出反应①的化学方程式:
(3)写出反应⑥的化学方程式:
(4)写出反应③的电极方程式:阳极:
(5)J的化学式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】碳酸亚铁(FeCO3)是生产补血剂的重要原料,制取碳酸亚铁的过程中涉及以下探究实验
实验一:
为探究某固体化合物X(仅含有三种元素)的组成和性质,设计并完成如下实验
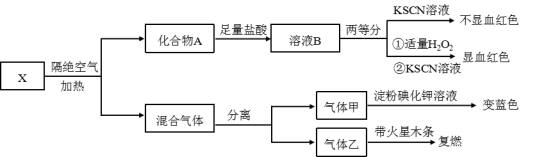
已知:气体甲、气体乙均为单质。
请回答:
(1)气体甲与碘化钾溶液反应的离子方程式为___________ 。化合物X含有的元素为___________ (写元素符号)。化合物A的化学式为___________ 。
实验二:
下图装置利用实验一所得溶液B制取FeCO3(白色固体,难溶于水):

装置丙中,先将导管移出液面通入一段时间气体,再向Na2CO3溶液(pH=11.9)通入一段时间CO2至其pH为7,滴加一定量B溶液产生白色沉淀和无色气体,过滤、洗涤、干燥,得到FeCO3固体。
请回答:
(2)试剂a是___________ 。向Na2CO3溶液通入CO2的目的是___________ 。丙装置中制取FeCO3的离子方程式为___________ 。
(3)不可用酸性高锰酸钾溶液检验溶液B中的金属阳离子的原因是___________ 。
(4)100mL 0.8mol/L B溶液完全反应,最终得到5克FeCO3固体,则产率为___________ (结果保留2位小数)。
实验一:
为探究某固体化合物X(仅含有三种元素)的组成和性质,设计并完成如下实验

已知:气体甲、气体乙均为单质。
请回答:
(1)气体甲与碘化钾溶液反应的离子方程式为
实验二:
下图装置利用实验一所得溶液B制取FeCO3(白色固体,难溶于水):

装置丙中,先将导管移出液面通入一段时间气体,再向Na2CO3溶液(pH=11.9)通入一段时间CO2至其pH为7,滴加一定量B溶液产生白色沉淀和无色气体,过滤、洗涤、干燥,得到FeCO3固体。
请回答:
(2)试剂a是
(3)不可用酸性高锰酸钾溶液检验溶液B中的金属阳离子的原因是
(4)100mL 0.8mol/L B溶液完全反应,最终得到5克FeCO3固体,则产率为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E五种物质均为中学化学中常见的化合物,已知A、B、C、D、E五种物质里含有相同的一种金属元素,并且A、B、C、D都可与物质M反应生成E,物质之间按箭头方向都可通过一步反应实现转化。实验室通常用碱B的澄清溶液检验CO2。
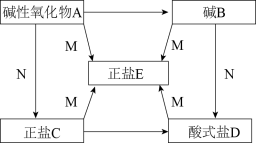
回答下列问题:
(1)写出物质的化学式:A__________ 、B__________ 、C__________ 、E__________ 。
(2)M属于__________ (填“酸”“碱”“盐”“酸性氧化物”或“碱性氧化物”)。
(3)写出正盐C转化为酸式盐D的化学方程式:____________________ 。
(4)写出碱B转化为酸式盐D的化学方程式:____________________ 。

回答下列问题:
(1)写出物质的化学式:A
(2)M属于
(3)写出正盐C转化为酸式盐D的化学方程式:
(4)写出碱B转化为酸式盐D的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】为探究难溶性盐X(仅含三种元素)的组成和性质,设计并完成如下实验:
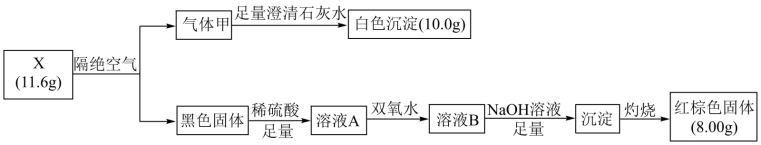
回答下列问题:
(1)气体甲的结构式___________ ,X的化学式是___________ 。
(2)写出溶液A中加一定量的双氧水后发生反应的离子方程式是___________ 。
(3)验证溶液B中可能含有的金属阳离子 ,下列检验试剂选用正确的是
,下列检验试剂选用正确的是___________ 。
A.用氯水、KSCN溶液检验是否有
B.用酸性 溶液检验是否有
溶液检验是否有
C.用 溶液检验是否有
溶液检验是否有

回答下列问题:
(1)气体甲的结构式
(2)写出溶液A中加一定量的双氧水后发生反应的离子方程式是
(3)验证溶液B中可能含有的金属阳离子
 ,下列检验试剂选用正确的是
,下列检验试剂选用正确的是A.用氯水、KSCN溶液检验是否有

B.用酸性
 溶液检验是否有
溶液检验是否有
C.用
 溶液检验是否有
溶液检验是否有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某同学利用如图所示装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。

(1)试管中发生反应的化学方程式为______________________________________________ 。
(2)该同学欲确定反应一段时间后试管中固体物质的成分,设计了如下方案:
①待试管冷却,取其中固体少许溶于稀盐酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红,则试管中固体是_________ (只有一个选项符合题意),若溶液未变红,则试管中固体是_________ (只有一个选项符合题意)。
A.一定有Fe3O4,可能有Fe B.只有Fe(OH)3 C.一定有Fe3O4和Fe
D.一定有Fe(OH)3,可能有Fe E.只有Fe3O4
(3)该同学按上述方案进行了实验,溶液未变红色,原因是________________________________ (用化学方程式表示)。

(1)试管中发生反应的化学方程式为
(2)该同学欲确定反应一段时间后试管中固体物质的成分,设计了如下方案:
①待试管冷却,取其中固体少许溶于稀盐酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红,则试管中固体是
A.一定有Fe3O4,可能有Fe B.只有Fe(OH)3 C.一定有Fe3O4和Fe
D.一定有Fe(OH)3,可能有Fe E.只有Fe3O4
(3)该同学按上述方案进行了实验,溶液未变红色,原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】某废旧金属材料中主要含Fe、Cu、Al、 、
、 、
、 、CuO(其余成分与酸碱都不反应)和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Al、Cu,绿矾等。回答下列问题:
、CuO(其余成分与酸碱都不反应)和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Al、Cu,绿矾等。回答下列问题:

(1)“焙烧”的目的主要是将金属单质转化为氧化物,同时除去___________ 。
(2)操作I和II均为___________ 。
(3)“碱浸”时发生反应的离子方程式为___________ 。
(4)滤渣II的化学成分为___________ 。
(5)滤液II制取绿矾晶体需先加入少量稀硫酸再经过蒸发浓缩、___________ 、过滤、洗涤,干燥得到绿矾晶体。
(6)绿矾在空气中容易被部分氧化为硫酸铁和氧化铁,现取被部分氧化的绿矾晶体溶于稀盐酸后,加入足量的BaCl2溶液,过滤得沉淀18.64g;再通入224mL(标准状况)氯气恰好将其中的 完全氧化。
完全氧化。
①为确定绿矾部分被氧化,应选择的最佳试剂是___________ (填标号)。
A.NaOH溶液 B. 酸性溶液 C.氯水 D.KSCN溶液
酸性溶液 C.氯水 D.KSCN溶液
②推测晶体中
___________ 。
 、
、 、
、 、CuO(其余成分与酸碱都不反应)和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Al、Cu,绿矾等。回答下列问题:
、CuO(其余成分与酸碱都不反应)和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Al、Cu,绿矾等。回答下列问题:
(1)“焙烧”的目的主要是将金属单质转化为氧化物,同时除去
(2)操作I和II均为
(3)“碱浸”时发生反应的离子方程式为
(4)滤渣II的化学成分为
(5)滤液II制取绿矾晶体需先加入少量稀硫酸再经过蒸发浓缩、
(6)绿矾在空气中容易被部分氧化为硫酸铁和氧化铁,现取被部分氧化的绿矾晶体溶于稀盐酸后,加入足量的BaCl2溶液,过滤得沉淀18.64g;再通入224mL(标准状况)氯气恰好将其中的
 完全氧化。
完全氧化。①为确定绿矾部分被氧化,应选择的最佳试剂是
A.NaOH溶液 B.
 酸性溶液 C.氯水 D.KSCN溶液
酸性溶液 C.氯水 D.KSCN溶液②推测晶体中

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】工业上通过电解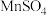 和
和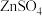 制取Zn和
制取Zn和 ,原料为软锰矿和闪锌矿,软锰矿中含
,原料为软锰矿和闪锌矿,软锰矿中含 约
约 ,
, 约
约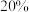 ,
, 约
约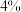 ,其余为水分,闪锌矿中含ZnS约
,其余为水分,闪锌矿中含ZnS约 ,FeS、CuS、
,FeS、CuS、 共约
共约 ,其余为水分.
,其余为水分.
I. 为了测量软锰矿中
为了测量软锰矿中 含量的测定,现将
含量的测定,现将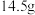 软锰矿溶于足量的稀硫酸中,加入足量的碘化钾晶体,充分反应后,过滤,将滤液加水稀释至1L,取
软锰矿溶于足量的稀硫酸中,加入足量的碘化钾晶体,充分反应后,过滤,将滤液加水稀释至1L,取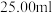 该溶液于锥形瓶中,滴入几滴淀粉溶液作指示剂,用
该溶液于锥形瓶中,滴入几滴淀粉溶液作指示剂,用 的标准
的标准 溶液滴定,消耗标准液
溶液滴定,消耗标准液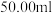 ,则软锰矿中
,则软锰矿中 含量
含量 ______  已知:
已知: ;
; 
Ⅱ 研人员开发了综合利用这两种资源的同槽酸浸工艺,工艺流程如图1所示.
研人员开发了综合利用这两种资源的同槽酸浸工艺,工艺流程如图1所示.
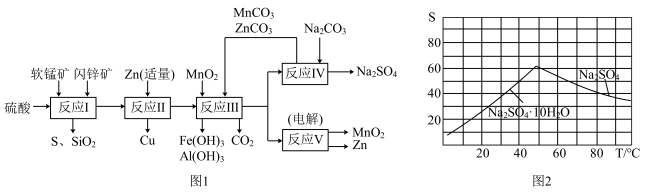
请回答下列问题:
 反应I的滤液中含有
反应I的滤液中含有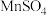 、
、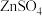 、
、 、
、 、
、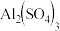 等.试完成反应I中生成
等.试完成反应I中生成 和
和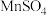 的化学方程
的化学方程
______ 
______ 
______ 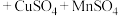 .
.
 反应Ⅱ加入适量锌的作用是
反应Ⅱ加入适量锌的作用是 ______ ;如果锌过量,还会进一步发生反应的离子方程式为 ______ .
 图2是
图2是 和
和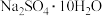 的溶解度曲线
的溶解度曲线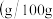 水
水 ,则Ⅳ中得到
,则Ⅳ中得到 固体的操作是:将分离出
固体的操作是:将分离出 和
和 后的滤液升温结晶
后的滤液升温结晶
______  用乙醇洗涤
用乙醇洗涤 干燥.用乙醇洗涤而不用水洗的原因是
干燥.用乙醇洗涤而不用水洗的原因是 ______ .
 用惰性电极电解
用惰性电极电解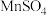 和
和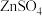 制得Zn和
制得Zn和 的总反应是:
的总反应是: ______ .
 本工艺可以循环利用的物质除
本工艺可以循环利用的物质除 、
、 、
、 以外,还有
以外,还有 ______  写化学式
写化学式 .
.
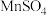 和
和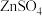 制取Zn和
制取Zn和 ,原料为软锰矿和闪锌矿,软锰矿中含
,原料为软锰矿和闪锌矿,软锰矿中含 约
约 ,
, 约
约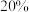 ,
, 约
约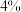 ,其余为水分,闪锌矿中含ZnS约
,其余为水分,闪锌矿中含ZnS约 ,FeS、CuS、
,FeS、CuS、 共约
共约 ,其余为水分.
,其余为水分.I.
 为了测量软锰矿中
为了测量软锰矿中 含量的测定,现将
含量的测定,现将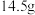 软锰矿溶于足量的稀硫酸中,加入足量的碘化钾晶体,充分反应后,过滤,将滤液加水稀释至1L,取
软锰矿溶于足量的稀硫酸中,加入足量的碘化钾晶体,充分反应后,过滤,将滤液加水稀释至1L,取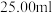 该溶液于锥形瓶中,滴入几滴淀粉溶液作指示剂,用
该溶液于锥形瓶中,滴入几滴淀粉溶液作指示剂,用 的标准
的标准 溶液滴定,消耗标准液
溶液滴定,消耗标准液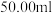 ,则软锰矿中
,则软锰矿中 含量
含量  已知:
已知: ;
; 
Ⅱ
 研人员开发了综合利用这两种资源的同槽酸浸工艺,工艺流程如图1所示.
研人员开发了综合利用这两种资源的同槽酸浸工艺,工艺流程如图1所示.
请回答下列问题:
 反应I的滤液中含有
反应I的滤液中含有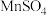 、
、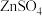 、
、 、
、 、
、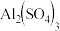 等.试完成反应I中生成
等.试完成反应I中生成 和
和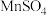 的化学方程
的化学方程


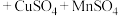 .
. 反应Ⅱ加入适量锌的作用是
反应Ⅱ加入适量锌的作用是  图2是
图2是 和
和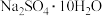 的溶解度曲线
的溶解度曲线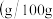 水
水 ,则Ⅳ中得到
,则Ⅳ中得到 固体的操作是:将分离出
固体的操作是:将分离出 和
和 后的滤液升温结晶
后的滤液升温结晶
 用乙醇洗涤
用乙醇洗涤 干燥.用乙醇洗涤而不用水洗的原因是
干燥.用乙醇洗涤而不用水洗的原因是  用惰性电极电解
用惰性电极电解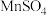 和
和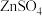 制得Zn和
制得Zn和 的总反应是:
的总反应是:  本工艺可以循环利用的物质除
本工艺可以循环利用的物质除 、
、 、
、 以外,还有
以外,还有  写化学式
写化学式 .
.
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某班化学兴趣小组的同学拟通过实验来探究菠菜中的营养成分。
已知信息:
①菠菜中含有草酸,草酸具有还原性。
②菠菜中含有丰富的铁元素,主要以难溶的 形式存在,其中铁元素为+2价。
形式存在,其中铁元素为+2价。
③赤血盐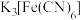 用于检验
用于检验 ,产生特征蓝色沉淀。
,产生特征蓝色沉淀。
I.水煮检验法:___________ 。
2.溶液A中未能检测出 的可能原因是
的可能原因是___________ 。
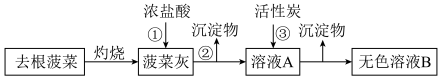
Ⅱ.灼烧检验法:___________ 。
4.甲同学取少量溶液B,滴加酸性 溶液,振荡后,溶液紫色消失,因此得出结论:溶液B含有
溶液,振荡后,溶液紫色消失,因此得出结论:溶液B含有 。乙同学认为甲同学的实验方法不严谨,理由是:
。乙同学认为甲同学的实验方法不严谨,理由是:___________ 。
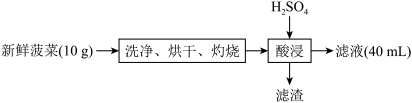
Ⅲ.分光光度法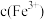 关系如下图。
关系如下图。 ,从中取出10mL待测液,测得待测液吸光度位于图中X点,试计算菠菜中所含铁元素的含量
,从中取出10mL待测液,测得待测液吸光度位于图中X点,试计算菠菜中所含铁元素的含量___________ mg/100g。(结果保留三位小数)
已知信息:
①菠菜中含有草酸,草酸具有还原性。
②菠菜中含有丰富的铁元素,主要以难溶的
 形式存在,其中铁元素为+2价。
形式存在,其中铁元素为+2价。③赤血盐
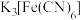 用于检验
用于检验 ,产生特征蓝色沉淀。
,产生特征蓝色沉淀。I.水煮检验法:

2.溶液A中未能检测出
 的可能原因是
的可能原因是Ⅱ.灼烧检验法:
4.甲同学取少量溶液B,滴加酸性
 溶液,振荡后,溶液紫色消失,因此得出结论:溶液B含有
溶液,振荡后,溶液紫色消失,因此得出结论:溶液B含有 。乙同学认为甲同学的实验方法不严谨,理由是:
。乙同学认为甲同学的实验方法不严谨,理由是:Ⅲ.分光光度法
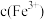 关系如下图。
关系如下图。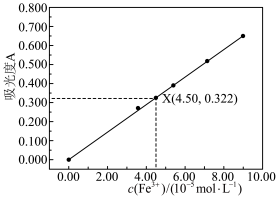
 ,从中取出10mL待测液,测得待测液吸光度位于图中X点,试计算菠菜中所含铁元素的含量
,从中取出10mL待测液,测得待测液吸光度位于图中X点,试计算菠菜中所含铁元素的含量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
真题
名校
【推荐3】化学小组用如下方法测定经处理后的废水中苯酚的含量(废水中不含干扰测定的物质)。
Ⅰ.用已准确称量的KBrO3固体配制一定体积的a mol·L−1 KBrO3标准溶液;
Ⅱ.取v1 mL上述溶液,加入过量KBr,加H2SO4酸化,溶液颜色呈棕黄色;
Ⅲ.向Ⅱ所得溶液中加入v2 mL废水;
Ⅳ.向Ⅲ中加入过量KI;
Ⅴ.用b mol·L−1 Na2S2O3标准溶液滴定Ⅳ中溶液至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗Na2S2O3溶液v3 mL。
已知:I2+2Na2S2O3=2NaI+ Na2S4O6
Na2S2O3和Na2S4O6溶液颜色均为无色
(1)Ⅰ中配制溶液用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和____________ 。
(2)Ⅱ中发生反应的离子方程式是_______________________________ 。
(3)Ⅲ中发生反应的化学方程式是_________________________________ 。
(4)Ⅳ中加KI前,溶液颜色须为黄色,原因是______________________________ 。
(5)KI与KBrO3物质的量关系为n(KI)≥6n(KBrO3)时,KI一定过量,理由是________ 。
(6)Ⅴ中滴定至终点的现象是_____________________________ 。
(7)废水中苯酚的含量为___________ g·L−1(苯酚摩尔质量:94 g·mol −1)。
(8)由于Br2具有____________ 性质,Ⅱ~Ⅳ中反应须在密闭容器中进行,否则会造成测定结果偏高。
Ⅰ.用已准确称量的KBrO3固体配制一定体积的a mol·L−1 KBrO3标准溶液;
Ⅱ.取v1 mL上述溶液,加入过量KBr,加H2SO4酸化,溶液颜色呈棕黄色;
Ⅲ.向Ⅱ所得溶液中加入v2 mL废水;
Ⅳ.向Ⅲ中加入过量KI;
Ⅴ.用b mol·L−1 Na2S2O3标准溶液滴定Ⅳ中溶液至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗Na2S2O3溶液v3 mL。
已知:I2+2Na2S2O3=2NaI+ Na2S4O6
Na2S2O3和Na2S4O6溶液颜色均为无色
(1)Ⅰ中配制溶液用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和
(2)Ⅱ中发生反应的离子方程式是
(3)Ⅲ中发生反应的化学方程式是
(4)Ⅳ中加KI前,溶液颜色须为黄色,原因是
(5)KI与KBrO3物质的量关系为n(KI)≥6n(KBrO3)时,KI一定过量,理由是
(6)Ⅴ中滴定至终点的现象是
(7)废水中苯酚的含量为
(8)由于Br2具有
您最近一年使用:0次



