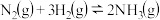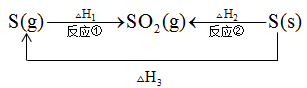下列说法正确的是
| A.在稀溶液中,1molH2SO4(aq)与1molBa(OH)2(aq)完全反应所放出的热量为中和热 |
| B.等质量的硫粉和硫蒸气分别完全燃烧,后者放出的热量更多 |
| C.乙炔(C2H2)的燃烧热为1299.6kJ•mol-1,则2C2H2(g)+5O2(g)=4CO2(g)+2H2O(g)的△H=-2599.2kJ•mol-1 |
| D.中和热测定实验中,可分多次把NaOH溶液倒入盛有稀盐酸的小烧杯中 |
更新时间:2022-11-13 17:51:43
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列热化学方程式书写中正确的是(ΔH的绝对值均正确):
| A.表达燃烧热:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ΔH=-1367.0kJ·mol-1 |
| B.在500℃、30MPa条件下,将0.5molN2和1.5molH2置于密闭容器中充分反应后生成NH3(g)时放出19.3kJ热量,该热化学方程式为:N2(g)+3H2(g)⇌2NH3(g) ΔH=-38.6 kJ·mol-1 |
| C.表达中和热:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1,据此可推出热化学方程式:H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) ΔH=-114.6kJ•mol﹣1 |
| D.已知热化学方程式:C(s)+O2(g)===CO2(g) ΔH1;C(s)+1/2O2(g)===CO(g) ΔH2;则ΔH1<ΔH2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列化学反应表示正确的是
A.H2S的燃烧热: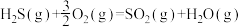 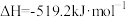 |
B.乙酸乙酯的制备: |
C.Na2S的水解反应: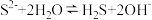 |
D.铅蓄电池充电时,与电源标识“+”相连的电极反应式: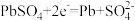 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是:
| A.由H原子形成1 mol H-H键要吸收热量 |
| B.所有燃烧反应都是放热反应 |
| C.在稀溶液中,1 mol酸与1 mol碱发生中和反应生成水时所释放的热量称为中和热 |
| D.在一定条件下,1mol H2 与足量的Cl2、Br2、I2 分别反应,放出热量关系是I2>Br2>Cl2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是
| A.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-801.3 kJ·mol-1,结论:CH4的燃烧热为-801.3 kJ·mol-1 |
| B.已知2KClO3(s)=2KCl(s)+3O2(g) ΔH=-78.03 kJ·mol-1,ΔS=+494.4 J·mol-1·k-1,结论:该反应在任何温度下都能自发进行 |
| C.稀溶液中有:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,结论:将盐酸与氨水的稀溶液混合后,若生成1 mol H2O,则会放出57.3 kJ的能量 |
| D.已知C(石墨,s)=C(金刚石,s) ∆H >0, 结论:相同条件下金刚石比石墨稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
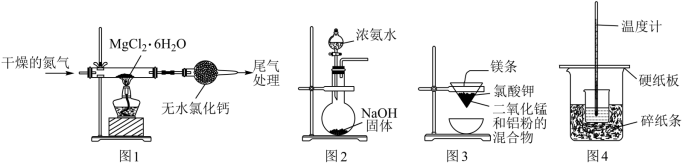
【推荐1】利用下列装置(夹持装置略)进行实验,不能 达到实验目的的是
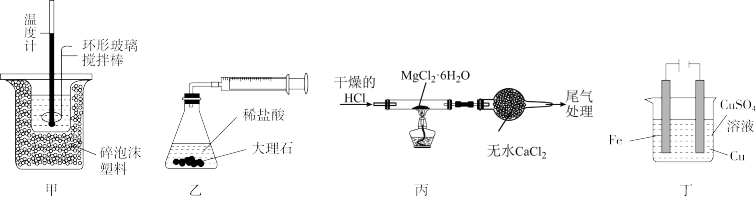

| A.用甲装置测定中和反应的反应热 | B.用乙装置测定反应速率 |
C.用丙装置制备无水 | D.用丁装置在铁上镀铜 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】对下列实验的描述正确的是


| A.图甲所示的实验:根据溶液颜色变化可比较Zn、Cu的金属活动性 |
| B.图乙所示的实验:根据小试管中液面的变化判断铁钉发生析氢腐蚀 |
| C.图丙所示的实验:根据温度计读数的变化用浓硫酸和NaOH反应测定中和热 |
| D.图丁所示的实验:根据两烧瓶中气体颜色的变化判断2NO2(g)⇌N2O4(g)是吸热反应 |
您最近一年使用:0次
【推荐1】热化学离不开实验,更离不开对反应热的研究。下列有关说法正确的是
|
|
|
| 图1 | 图2 | 图3 |
| A.向图1的试管A中加入某一固体和液体,若注射器的活塞右移,说明A中发生了放热反应 |
| B.将图1虚框中的装置换为图2装置,若注射器的活塞右移,说明锌粒和稀硫酸的反应为放热反应 |
C.由图3可知,反应①的 小于反应②的 小于反应②的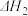 |
D.由图3可知,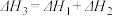 |
您最近一年使用:0次
【推荐2】下列说法或表示方法正确的是
A.由“C(石墨) C(金刚石)△H=+1.9 kJ/mol”可知金刚石比石墨稳定 C(金刚石)△H=+1.9 kJ/mol”可知金刚石比石墨稳定 |
| B.在101KPa时,1mol碳燃烧所放出的热量为碳的燃烧热 |
| C.相同的条件下,如果1 mol氢原子所具有的能量为E1,1 mol氢分子的能量为E2,则2E1﹥E2 |
| D.HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4 和Ca(OH)2 反应的中和热为△H=-(2×57.3)kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列说法或表示正确的是
| A.已知CH4(g)+2O2(g)=CO2(g)+2H2O(l);ΔH =-802.33kJ/mol,则CH4的燃烧热为802.33 kJ |
| B.已知S(g)+O2(g)=SO2(s);ΔH1,S(g)+O2(g)=SO2(g);ΔH2,则ΔH2<ΔH1 |
| C.在100 ℃、101kPa条件下,1mol液态水气化时需要吸收40.69 kJ的热量,则H2O(g)=H2O(l)的ΔH=+40.69 kJ·mol-1 |
| D.由C(石墨,s)= C(金刚石,s)ΔH= + 119 kJ/mol可知,石墨比金刚石稳定 |
您最近一年使用:0次

 ,则
,则

 和
和 反应的中和热
反应的中和热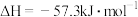 ,则
,则
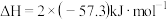
 燃烧热
燃烧热 是
是 ,则
,则 的
的

 和
和
 置于密闭的容器中充分反应生成
置于密闭的容器中充分反应生成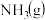 ,放热
,放热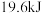 ,其热化学方程式为
,其热化学方程式为