根据元素周期表回答下列问题:
(1)第三周期中,原子半径(稀有气体元素除外)最小的元素是_______ ,非金属性最强的元素是_______ 。
(2)ⅦA族中,原子半径(稀有气体元素除外)最大的元素是_______ ,非金属性最弱的元素是_______ 。
(3)钠、硫、硅、锗四种元素的单质中,适合作半导体材料的是_______ 。
(1)第三周期中,原子半径(稀有气体元素除外)最小的元素是
(2)ⅦA族中,原子半径(稀有气体元素除外)最大的元素是
(3)钠、硫、硅、锗四种元素的单质中,适合作半导体材料的是
更新时间:2022-11-24 16:00:49
|
相似题推荐
填空题
|
容易
(0.94)
解题方法
【推荐1】用“>”或“<”填空:
| 原子半径 | 电负性 | 熔点 | 沸点 |
| Al | N | 金刚石 | CH4 |
您最近半年使用:0次
填空题
|
容易
(0.94)
【推荐2】用元素符号填空:在短周期元素中(稀有气体元素除外),
(1)原子半径最大的元素是___________ ;
(2)非金属性最强的元素是___________ ;
(3)最高价氧化物对应水化物中酸性最强的元素是___________ ;
(4)最高价氧化物对应水化物中碱性最强的元素是___________ 。
(1)原子半径最大的元素是
(2)非金属性最强的元素是
(3)最高价氧化物对应水化物中酸性最强的元素是
(4)最高价氧化物对应水化物中碱性最强的元素是
您最近半年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐1】O、P、S的原子半径由小到大的顺序为_______ 。
您最近半年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐2】我国科学家成功合成了含 N 的五氮阴离子盐,这是全氮含能材料研究领域中里程碑式的突破。
的五氮阴离子盐,这是全氮含能材料研究领域中里程碑式的突破。
(1)N 中,N 原子之间的相互作用是
中,N 原子之间的相互作用是_____ (填“离子键”或“共价键”)。
(2)砷(As)与氮位于同一主族,下列推断正确的是_____ (填序号)。
① 砷元素的最低负化合价为−3 价 ② 砷的最高价氧化物对应的水化物属于酸 ③ 热稳定性:AsH3>NH3
(3)非金属性O 强于N,用原子结构解释原因:_____ ,得电子能力O 大于N。
 的五氮阴离子盐,这是全氮含能材料研究领域中里程碑式的突破。
的五氮阴离子盐,这是全氮含能材料研究领域中里程碑式的突破。(1)N
 中,N 原子之间的相互作用是
中,N 原子之间的相互作用是(2)砷(As)与氮位于同一主族,下列推断正确的是
① 砷元素的最低负化合价为−3 价 ② 砷的最高价氧化物对应的水化物属于酸 ③ 热稳定性:AsH3>NH3
(3)非金属性O 强于N,用原子结构解释原因:
您最近半年使用:0次
填空题
|
容易
(0.94)
【推荐3】同一周期的主族元素,从左到右,电子层数_________ ,最外层电子数逐渐______ ,原子半径逐渐_________ ,失电子能力逐渐_________ ,得电子能力逐渐_____ ,金属性逐渐_____ ,非金属性逐渐______ ,最后以_____ 元素结束。同一主族的元素,从上到下,电子层数逐渐_________ ,最外层电子数_____________ ,原子半径逐渐_________ ,失电子能力逐渐_____ ,得电子能力逐渐_________ ,金属性逐渐_____ ,非金属性逐渐_________ 。
您最近半年使用:0次
填空题
|
容易
(0.94)
【推荐1】有下列四种微粒:① 、②
、②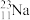 、③
、③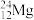 、④
、④
(1)按原子半径由大到小顺序排列的是________________________ (用序号回答,下同)
(2)微粒中质子数小于中子数的是______________________________
(3)在化合物中呈现的化合价的数值最多的是____________________
(4)能形成X2Y2型化合物的是___________ 。
 、②
、②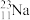 、③
、③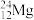 、④
、④
(1)按原子半径由大到小顺序排列的是
(2)微粒中质子数小于中子数的是
(3)在化合物中呈现的化合价的数值最多的是
(4)能形成X2Y2型化合物的是
您最近半年使用:0次
填空题
|
容易
(0.94)
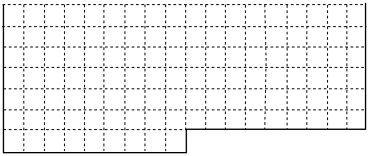
【推荐2】(1)表中的实线是元素周期表部分边界,请在表中用实线补全元素周期表边界________ 。
(2)元素甲是第三周期ⅥA族元素,请在方框中按氦元素的式样(如图)
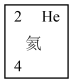
写出元素甲的原子序数、元素符号、元素名称、相对原子质量。
(3)元素乙的M层上有3个电子,则乙原子半径与甲原子半径比较:________ >________ (用元素符号表示),甲、乙的最高价氧化物水化物相互反应的离子方程式为:________
(4)元素周期表体现了元素周期律,即元素的性质随着_________ 的递增呈现____ 的变化。

(2)元素甲是第三周期ⅥA族元素,请在方框中按氦元素的式样(如图)

写出元素甲的原子序数、元素符号、元素名称、相对原子质量。
(3)元素乙的M层上有3个电子,则乙原子半径与甲原子半径比较:
(4)元素周期表体现了元素周期律,即元素的性质随着
您最近半年使用:0次
填空题
|
容易
(0.94)
【推荐3】根据微观结构回答下列问题:
(1)ⅥA族中,原子半径最小的元素是___________ (填元素符号)。
(2)已知碘原子结构示意图如图所示,则:

①碘在元素周期表中的位置为___________ ;
②碘的非金属性比氯___________ (填“强”或“弱”);
③碘元素的最高化合价为___________ ;
④碘的最高价氧化物对应的水化物的化学式为___________ ,属于___________ (填“离子”或“共价”)化合物;
⑤单质碘属于___________ (填“晶体”或“非晶体”);
⑥碘升华克服的作用力是___________ 。
(1)ⅥA族中,原子半径最小的元素是
(2)已知碘原子结构示意图如图所示,则:

①碘在元素周期表中的位置为
②碘的非金属性比氯
③碘元素的最高化合价为
④碘的最高价氧化物对应的水化物的化学式为
⑤单质碘属于
⑥碘升华克服的作用力是
您最近半年使用:0次



