根据你学过的知识,总结物质结构的研究对发现新物质和预测新物质性质的作用和意义_______ 。
更新时间:2022-11-25 09:13:56
|
相似题推荐
【推荐1】氮、磷、砷(As)、锑(Sb)、铋(Bi)、镆(Mc)为元素周期表中原子序数依次增大的同族元素。回答下列问题:
(1)砷在元素周期表中的位置_________ 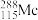 的中子数为
的中子数为______________________ 。
(2)热稳定性:NH3______________________ PH3(填“>”或“<”)。
(3)PH3和NH3与卤化氢的反应相似,产物的结构和性质也相似。下列对PH3与HI反应产物的推断正确的是____________ (填序号)。
a.不能与NaOH反应 b.含离子键、共价键 c.能与水反应
(1)砷在元素周期表中的位置
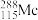 的中子数为
的中子数为(2)热稳定性:NH3
(3)PH3和NH3与卤化氢的反应相似,产物的结构和性质也相似。下列对PH3与HI反应产物的推断正确的是
a.不能与NaOH反应 b.含离子键、共价键 c.能与水反应
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】不同元素的原子在分子内吸引电子的能力大小可用数值表示,该数值称为电负性。一般认为:如果两个成键元素间的电负性差值大于1.7,原子之间通常形成离子键;如果两个成键元素间的电负性差值小于1.7,原子之间通常形成共价键。表中是某些元素的电负性值:
观察上述数据,回答下列问题:
(1)通过分析电负性值变化规律,确定Mg元素电负性值的最小范围:_______ 。
(2)请归纳元素的电负性和金属性、非金属性的关系_______ 。
(3)某有机化合物结构中含S-N键,其共用电子对偏向_______ (写原子名称)。
(4)从电负性角度,判断AlCl3是离子化合物,还是共价化合物的方法是_______ (写出判断的方法和结论);请设计一个实验方案证明上述所得到的结论:_______ 。
| 元素符号 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
| 电负性值 | 1.0 | 1.5 | 2.0 | 2.5 | 3.5 | 4.0 | 0.9 | 1.5 | 1.8 | 2.1 | 2.5 | 3.0 |
观察上述数据,回答下列问题:
(1)通过分析电负性值变化规律,确定Mg元素电负性值的最小范围:
(2)请归纳元素的电负性和金属性、非金属性的关系
(3)某有机化合物结构中含S-N键,其共用电子对偏向
(4)从电负性角度,判断AlCl3是离子化合物,还是共价化合物的方法是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学选修物质结构与性质某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。
(1)基态氮原子的核外电子排布式为________________ 。
(2)与N互为等电子体的离子有________ (任写一种)。
(3)工业上用氧化铝与氮气和碳在一定条件下反应生成X和CO,X的晶体结构如图所示,其化学式为_______ ,工业制备X的化学方程式为______________________ 。

(4)X晶体中包含的化学键类型为________ (填字母)。
X晶体中氮原子的杂化类型为________ 杂化。
(5)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,可能的原因是
____________________________________________________________________ 。
(6)若X的密度为ρ g·cm-3,则晶体中最近的两个Al原子的距离为____________ cm。(阿伏加德罗常数的值用NA表示)
(1)基态氮原子的核外电子排布式为
(2)与N互为等电子体的离子有
(3)工业上用氧化铝与氮气和碳在一定条件下反应生成X和CO,X的晶体结构如图所示,其化学式为

(4)X晶体中包含的化学键类型为
| A.共价键 | B.配位键 | C.离子键 | D.金属键 |
X晶体中氮原子的杂化类型为
(5)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,可能的原因是
(6)若X的密度为ρ g·cm-3,则晶体中最近的两个Al原子的距离为
您最近半年使用:0次




