北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
已知: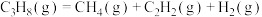
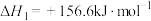
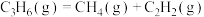
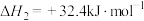
(1)丙烷分子中极性键和非极性键数目的比值为_______ 。
(2)丙烷的二氯代物有_______ 种。
(3)上述两个反应能在_______ 条件下自发进行。
(4)相同条件下,反应 的
的
_______  。
。
已知:
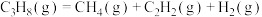
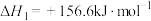
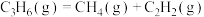
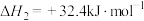
(1)丙烷分子中极性键和非极性键数目的比值为
(2)丙烷的二氯代物有
(3)上述两个反应能在
(4)相同条件下,反应
 的
的
 。
。
22-23高二上·上海宝山·期中 查看更多[2]
上海市上海交通大学附属中学2022-2023学年高二上学期期中考试化学试题(已下线)专题03 化学反应进行的方向和限度-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(上海专用)
更新时间:2022-11-25 19:19:40
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】请按要求作答。
(1)写出下列物质在水溶液中的电离方程式。
①NH3·H2O:_______ 。
②NaHSO4:_______ 。
(2)下列盐溶液中能发生水解的用离子方程式 表示,不能发生水解的请写上“不发生水解”字样,并说明溶液的酸碱性:
①CuCl2_______ ,溶液呈_______ 性;
②K2SO4_______ ,溶液呈_______ 性;
(3)明矾可用于净水,原因是(用离子方程式表示):_______
(4)纯碱可代替洗涤剂洗涤餐具,原因是(用离子方程式表示)_______
(5)已知下列热化学方程式:
 ①
①
 ②
②
 ③
③
写出FeO(s)被CO(g)还原成Fe(s)和CO2(g)的热化学方程式:_______ 。
(1)写出下列物质在水溶液中的电离方程式。
①NH3·H2O:
②NaHSO4:
(2)下列盐溶液中能发生水解的
①CuCl2
②K2SO4
(3)明矾可用于净水,原因是(用离子方程式表示):
(4)纯碱可代替洗涤剂洗涤餐具,原因是(用离子方程式表示)
(5)已知下列热化学方程式:
 ①
① ②
② ③
③写出FeO(s)被CO(g)还原成Fe(s)和CO2(g)的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程的热化学方程式为:
a.C(s)+O2(g)===CO2(g) ΔH=E1①
b.C(s)+H2O(g)===CO(g)+H2(g) ΔH=E2②
H2(g)+1/2O2(g)===H2O(g) ΔH=E3③
CO(g)+1/2O2(g)===CO2(g) ΔH=E4④
试回答下列问题:
(1)与途径a相比,途径b有较多的优点,即___________________________________ 。
(2)上述四个热化学方程式中ΔH>0的反应有_____________________________________ ___________________________________ 。
(3)等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是________ 。
A.a比b多 B.a比b少
C.a与b在理论上相同 D.两者无法比较
(4)根据能量守恒定律,E1、E2、E3、E4之间的关系为________________ 。
a.C(s)+O2(g)===CO2(g) ΔH=E1①
b.C(s)+H2O(g)===CO(g)+H2(g) ΔH=E2②
H2(g)+1/2O2(g)===H2O(g) ΔH=E3③
CO(g)+1/2O2(g)===CO2(g) ΔH=E4④
试回答下列问题:
(1)与途径a相比,途径b有较多的优点,即
(2)上述四个热化学方程式中ΔH>0的反应有
(3)等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是
A.a比b多 B.a比b少
C.a与b在理论上相同 D.两者无法比较
(4)根据能量守恒定律,E1、E2、E3、E4之间的关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2) 在催化剂的作用下合成甲醇,可能发生的反应如下:
I.CO(g)+H2O(g) CO2(g)+H2(g) △H1=-41.0kJ/mol
CO2(g)+H2(g) △H1=-41.0kJ/mol
II. CO(g) +2H2(g) CH3OH(g) △H2=-90. 0kJ/mol
CH3OH(g) △H2=-90. 0kJ/mol
III.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
回答下列问题:
(1)则△H3=______ ,在以上制备甲醇的两个反应中,反应II优于反应III,其原因为______ 。
(2)一定化例的合成气在装有催化剂的反应器中反应12小时,体系中甲醇的产率和催化剂的催化活性与温度的关系如图1所示。
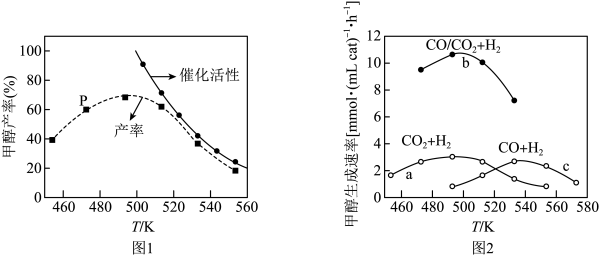
当温度为470K时,图中P点_____ (填“是”或“不是”)处于平衡状态。490K之后,甲醇产率下降的原因是____________ 。
(3)图2 为一定比例的CO2、H2,CO、H2,CO、CO2、.H2条件下甲醇生成速率与温度的关系。
①490K时,根据曲线a、c 判断合成甲醇的反应机理是______ (填“A"或“B").
A.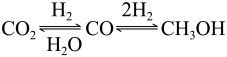 B.
B. 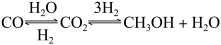
②490K时,曲线a 与曲线b相比,CO的存在使甲醇生成速率增大,结合反应I、III分析原因______________________ 。
(4)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的电极反应式为_____ 。
I.CO(g)+H2O(g)
 CO2(g)+H2(g) △H1=-41.0kJ/mol
CO2(g)+H2(g) △H1=-41.0kJ/molII. CO(g) +2H2(g)
 CH3OH(g) △H2=-90. 0kJ/mol
CH3OH(g) △H2=-90. 0kJ/mol III.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3回答下列问题:
(1)则△H3=
(2)一定化例的合成气在装有催化剂的反应器中反应12小时,体系中甲醇的产率和催化剂的催化活性与温度的关系如图1所示。

当温度为470K时,图中P点
(3)图2 为一定比例的CO2、H2,CO、H2,CO、CO2、.H2条件下甲醇生成速率与温度的关系。
①490K时,根据曲线a、c 判断合成甲醇的反应机理是
A.
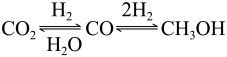 B.
B. 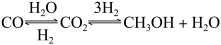
②490K时,曲线a 与曲线b相比,CO的存在使甲醇生成速率增大,结合反应I、III分析原因
(4)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】甲醇是一种重要的化工原料的具有开发和应用的广阔前景。工业上使用水煤气( CO 与H2的混合气体 )转化成甲醇,反应为CO(g)+2H2(g) CH3OH(g) △H。在体积可变的密闭容器中投入0.5mol CO和1.0 mol H2。实验测得平衡时CH3OH的物质的量随温度、压强的变化如图所示。
CH3OH(g) △H。在体积可变的密闭容器中投入0.5mol CO和1.0 mol H2。实验测得平衡时CH3OH的物质的量随温度、压强的变化如图所示。
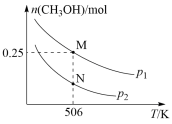
(1)根据图象判断△H_______ 0 (填“<”或“>”);该反应的自发的条件是__________ (填选项)。
a. 高温自发,低温不自发 b. 低温自发,高温不自发
c.高温、低温都自发 d. 高温、低温都不自发
(2)M点H2的转化率为__________ 。若点M对应混合气体的体积为1L,则506K时,该反应平衡常数K=__________ 。
(3)下列叙述能说明上述反应达到化学平衡状态的有__________ (填序号)。
a.v(H2)= 2v(CH3OH) b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变 d.混合气体的平均摩尔质量不在改变
(4)平衡后再加入0. 5mol CO和1.0 mol H2后重新到达平衡,则CO的转化率__________ (填“增大”“不变”或“减小”)。
(5)试判断p1__________ p2(填 “ > ” 、“<” 或 “=”),判断的依据是__________ 。
 CH3OH(g) △H。在体积可变的密闭容器中投入0.5mol CO和1.0 mol H2。实验测得平衡时CH3OH的物质的量随温度、压强的变化如图所示。
CH3OH(g) △H。在体积可变的密闭容器中投入0.5mol CO和1.0 mol H2。实验测得平衡时CH3OH的物质的量随温度、压强的变化如图所示。
(1)根据图象判断△H
a. 高温自发,低温不自发 b. 低温自发,高温不自发
c.高温、低温都自发 d. 高温、低温都不自发
(2)M点H2的转化率为
(3)下列叙述能说明上述反应达到化学平衡状态的有
a.v(H2)= 2v(CH3OH) b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变 d.混合气体的平均摩尔质量不在改变
(4)平衡后再加入0. 5mol CO和1.0 mol H2后重新到达平衡,则CO的转化率
(5)试判断p1
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知在 时,石灰石发生分解反应:
时,石灰石发生分解反应: ,则
,则
(1)该反应_______ (填“能”或“不能”)正向自发进行。
(2)若温度能决定反应方向,则该反应正向自发进行的最低温度为_______ 。
 时,石灰石发生分解反应:
时,石灰石发生分解反应: ,则
,则(1)该反应
(2)若温度能决定反应方向,则该反应正向自发进行的最低温度为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】在恒容密闭容器中,由 合成甲醇:
合成甲醇: ,在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示。
,在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示。
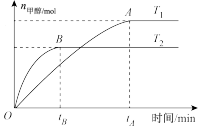
回答下列问题:
(1)从图中可知
___________  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
(2)该反应的平衡常数表达式为
___________ 。
(3)该反应在 时的平衡常数大小关系是
时的平衡常数大小关系是
___________  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
(4)该反应的焓变
___________ 0(填“>”“=”或“<”),判断的依据是___________ 。
(5)处于A点的反应体系从 变到
变到 ,达到平衡时
,达到平衡时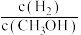 将
将___________ (填“增大”“减小”或“不变”)。
(6)在其他条件不变的情况下, 时该反应
时该反应 能否自发进行?
能否自发进行?___________ (填“能”“不能”或“不能判断”)。
 合成甲醇:
合成甲醇: ,在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示。
,在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示。
回答下列问题:
(1)从图中可知

 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。(2)该反应的平衡常数表达式为

(3)该反应在
 时的平衡常数大小关系是
时的平衡常数大小关系是
 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。(4)该反应的焓变

(5)处于A点的反应体系从
 变到
变到 ,达到平衡时
,达到平衡时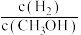 将
将(6)在其他条件不变的情况下,
 时该反应
时该反应 能否自发进行?
能否自发进行?
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】有机化合物的种类已经超过一亿种,化学工作者对有机的研究正在不断深入。
(1)科学家在-100 ℃的低温下合成了一种烃X,该分子的结构模型如图所示。
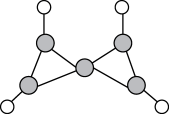
a.X的分子式为___________ 。
b.该X分子中每个碳原子均形成4个共价键,则1个X分子中含有___________ 个σ键,___________ 个π键。
c.1 mol X在一定条件下可与___________ mol H2发生反应。
d.该分子碳原子的杂化类型为___________ 。
(2)芯片制造过程需用到光刻胶。某光刻胶(一种高分子化合物)可由降冰片烯(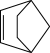 )与马来酸酐(
)与马来酸酐(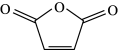 )共聚而成。反应的化学方程式为
)共聚而成。反应的化学方程式为___________ 。
(3)某烃A和炔烃B的混合物共1 L,完全燃烧生成相同状况下的二氧化碳1.4 L,水蒸气1.6 L,写出两种烃的结构简式A___________ ,B___________ 。
(4)有机物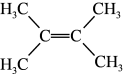 的名称为
的名称为___________ ,分子式为C4H8BrCl的有机物共有(不含立体异构) ___________ 种。
(5)写出符合下列条件的A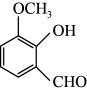 的同分异构体
的同分异构体___________
a.含有酚羟基 b.不含醛基 c.分子中有四种化学环境的氢
(1)科学家在-100 ℃的低温下合成了一种烃X,该分子的结构模型如图所示。

a.X的分子式为
b.该X分子中每个碳原子均形成4个共价键,则1个X分子中含有
c.1 mol X在一定条件下可与
d.该分子碳原子的杂化类型为
(2)芯片制造过程需用到光刻胶。某光刻胶(一种高分子化合物)可由降冰片烯(
 )与马来酸酐(
)与马来酸酐( )共聚而成。反应的化学方程式为
)共聚而成。反应的化学方程式为(3)某烃A和炔烃B的混合物共1 L,完全燃烧生成相同状况下的二氧化碳1.4 L,水蒸气1.6 L,写出两种烃的结构简式A
(4)有机物
 的名称为
的名称为(5)写出符合下列条件的A
 的同分异构体
的同分异构体a.含有酚羟基 b.不含醛基 c.分子中有四种化学环境的氢
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学工业为疫情防控提供了强有力的物质支撑,防护器材、消毒药剂等等都与化学有关,回答下列问题。
(1)口罩面罩所用的无纺布成分是聚丙烯,由丙烯制得聚丙烯的方程式是___________ ,一种口罩的滤材被提前注入了电荷,并且这部分电荷在正常储存时可以长时间存在,该滤材对___________ 成分的吸附效果较好。
a. b.胶体 c.水蒸气 d.NO
b.胶体 c.水蒸气 d.NO
(2)用于口罩灭菌处理的环氧乙烷,常用乙烯氧化法制备,其中一种目前比较认可的反应机理为


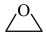


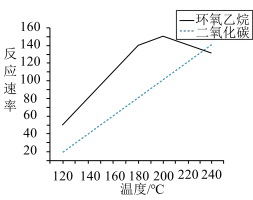
乙烯合成环氧乙烷的选择性为___________ %[选择性=  ]。氧化过程中,产物的生成速率与温度的关系如图,该反应适宜的反应温度为
]。氧化过程中,产物的生成速率与温度的关系如图,该反应适宜的反应温度为___________ ℃。
(3)过氧乙酸(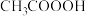 )也是一种常用的消毒剂,过氧乙酸中,极性键与非极性键数目之比为
)也是一种常用的消毒剂,过氧乙酸中,极性键与非极性键数目之比为___________ ,过氧乙酸的优点是杀菌速度快,缺点可能是___________ 。
(1)口罩面罩所用的无纺布成分是聚丙烯,由丙烯制得聚丙烯的方程式是
a.
 b.胶体 c.水蒸气 d.NO
b.胶体 c.水蒸气 d.NO(2)用于口罩灭菌处理的环氧乙烷,常用乙烯氧化法制备,其中一种目前比较认可的反应机理为





乙烯合成环氧乙烷的选择性为
 ]。氧化过程中,产物的生成速率与温度的关系如图,该反应适宜的反应温度为
]。氧化过程中,产物的生成速率与温度的关系如图,该反应适宜的反应温度为
(3)过氧乙酸(
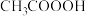 )也是一种常用的消毒剂,过氧乙酸中,极性键与非极性键数目之比为
)也是一种常用的消毒剂,过氧乙酸中,极性键与非极性键数目之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图表示不同类型共价键形成时电子云重叠情况:
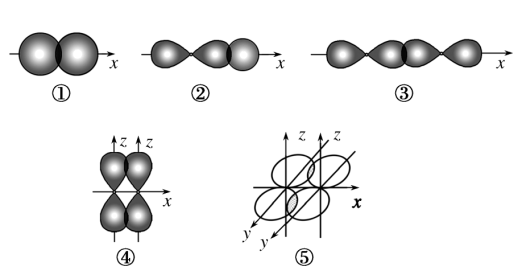
(1)其中形成的化学键属于轴对称的有_______ 。
(2)下列物质中,通过方式①化学键形成的是_______ ;通过方式②化学键形成的是_______ ;只通过方式③化学键形成的是_______ ;同时含有③、④、⑤三种方式化学键的物质是_______ 。
A. Cl2 B.HCl C.N2 D.H2
(3)甲、乙、丙三种有机物的结构如下:
甲: 乙:CH2=CH2丙:
乙:CH2=CH2丙:
①甲分子中有_______ 个σ键,_______ 个π键。
②乙分子中_______ (填“有”或“没有”)极性键,_______ (填“是”或“不是”)极性分子。
③丙分子中σ键与π键的数目之比为_______ 。

(1)其中形成的化学键属于轴对称的有
(2)下列物质中,通过方式①化学键形成的是
A. Cl2 B.HCl C.N2 D.H2
(3)甲、乙、丙三种有机物的结构如下:
甲:
 乙:CH2=CH2丙:
乙:CH2=CH2丙:
①甲分子中有
②乙分子中
③丙分子中σ键与π键的数目之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)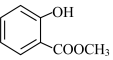 中含有的官能团的名称为
中含有的官能团的名称为_______ 。
(2)戊烷的某种同分异构体只有一种一氯代物,试书写它的结构简式:_______ 。
(3)某芳香烃的结构为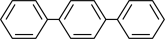 ,它的分子式为
,它的分子式为_______ ,一氯代物有_______ 种。
(1)
 中含有的官能团的名称为
中含有的官能团的名称为(2)戊烷的某种同分异构体只有一种一氯代物,试书写它的结构简式:
(3)某芳香烃的结构为
 ,它的分子式为
,它的分子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】萘、蒽、菲(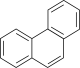 )是比较简单的稠环芳香烃,请回答以下问题。
)是比较简单的稠环芳香烃,请回答以下问题。
(1)在一定条件下,萘与浓硫酸、浓硝酸的混合酸作用可以得到两种萘的一硝基取代物,写出这两个反应的化学方程式____ 。
(2)蒽和菲之间存在何种关系____ ?
(3)菲的一氯取代产物可能有多少种____ ?写出它们的结构简式____ 。
 )是比较简单的稠环芳香烃,请回答以下问题。
)是比较简单的稠环芳香烃,请回答以下问题。(1)在一定条件下,萘与浓硫酸、浓硝酸的混合酸作用可以得到两种萘的一硝基取代物,写出这两个反应的化学方程式
(2)蒽和菲之间存在何种关系
(3)菲的一氯取代产物可能有多少种
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】CO2的有效利用可以缓解温室效应和能源短缺问题。
(1)CO2的分子结构决定了其性质和用途。
①CO2的电子式是_____________ 。
②在温度高于31.26 ℃、压强高于7.29×106Pa时,CO2处于超临界状态,称为超临界CO2流体,它可用作萃取剂提取草药中的有效成分。与用有机溶剂萃取相比,用超临界CO2萃取的优点有:___________ (答出一点即可)。
(2)中科院大连化学物理研究所的科研人员在新型纳米催化剂Na-Fe3O4和HMCM-22 的表面将CO2转化为烷烃,其过程如下图。
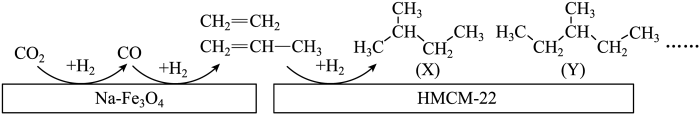
上图中CO2转化为CO的反应为:CO2(g)+H2(g) = CO(g)+H2O(g) △H= +41kJ/mol
已知:2CO2(g)+6H2(g) = C2H4(g)+4H2O(g) △H= -128kJ/mol
①则图中CO转化为C2H4的热化学方程式是____________________ 。
②关于X与Y的说法正确的是________ (填序号〕。
a.实验式相同 b.都有4种一氯代物
c.都易使酸性KMnO4溶液褪色 d.互为同系物
③催化剂中Fe3O4的制备方法如下:将一定比例的FeCl2和FeCl3溶于盐酸,然后在 60 ℃下逐滴加入NaOH溶液至pH≈10,继续搅拌,得Fe3O4。该反应的离子方程式是____________________ 。
(1)CO2的分子结构决定了其性质和用途。
①CO2的电子式是
②在温度高于31.26 ℃、压强高于7.29×106Pa时,CO2处于超临界状态,称为超临界CO2流体,它可用作萃取剂提取草药中的有效成分。与用有机溶剂萃取相比,用超临界CO2萃取的优点有:
(2)中科院大连化学物理研究所的科研人员在新型纳米催化剂Na-Fe3O4和HMCM-22 的表面将CO2转化为烷烃,其过程如下图。

上图中CO2转化为CO的反应为:CO2(g)+H2(g) = CO(g)+H2O(g) △H= +41kJ/mol
已知:2CO2(g)+6H2(g) = C2H4(g)+4H2O(g) △H= -128kJ/mol
①则图中CO转化为C2H4的热化学方程式是
②关于X与Y的说法正确的是
a.实验式相同 b.都有4种一氯代物
c.都易使酸性KMnO4溶液褪色 d.互为同系物
③催化剂中Fe3O4的制备方法如下:将一定比例的FeCl2和FeCl3溶于盐酸,然后在 60 ℃下逐滴加入NaOH溶液至pH≈10,继续搅拌,得Fe3O4。该反应的离子方程式是
您最近一年使用:0次



