不同元素的第一电离能 如下图所示。试根据元素在元素周期表中的位置,分析图中曲线的变化特点,并回答下列问题。
如下图所示。试根据元素在元素周期表中的位置,分析图中曲线的变化特点,并回答下列问题。
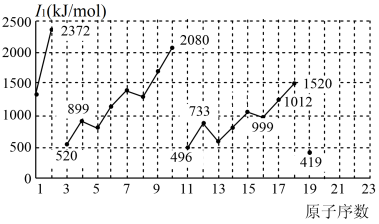
(1)总结同主族内不同元素的 变化的特点
变化的特点______ 。
(2)同周期内,随原子序数增大, 增大。但个别元素的
增大。但个别元素的 出现反常,试预测下列关系中正确的是
出现反常,试预测下列关系中正确的是_______ (填序号)。
① (砷)>
(砷)>  (硒) ②
(硒) ② (砷)<
(砷)<  (硒)
(硒)
③ (溴) >
(溴) >  (硒) ④
(硒) ④ (溴) <
(溴) <  (硒)
(硒)
(3)解释10号元素 较大的原因
较大的原因______ 。
(4)请估计1mol气态基态Ca原子失去最外层一个电子所需能量E的范围______ 。
 如下图所示。试根据元素在元素周期表中的位置,分析图中曲线的变化特点,并回答下列问题。
如下图所示。试根据元素在元素周期表中的位置,分析图中曲线的变化特点,并回答下列问题。
(1)总结同主族内不同元素的
 变化的特点
变化的特点(2)同周期内,随原子序数增大,
 增大。但个别元素的
增大。但个别元素的 出现反常,试预测下列关系中正确的是
出现反常,试预测下列关系中正确的是①
 (砷)>
(砷)>  (硒) ②
(硒) ② (砷)<
(砷)<  (硒)
(硒)③
 (溴) >
(溴) >  (硒) ④
(硒) ④ (溴) <
(溴) <  (硒)
(硒)(3)解释10号元素
 较大的原因
较大的原因(4)请估计1mol气态基态Ca原子失去最外层一个电子所需能量E的范围
更新时间:2022-11-27 16:22:57
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】如图是元素周期表的一部分:

(1)写出元素①的元素符号___________ ,与①同周期的主族元素中,第一电离能比①大的有___________ 种。该周期的某种元素基态原子的核外电子排布式为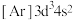 ,则该元素在元素周期表中的位置为
,则该元素在元素周期表中的位置为___________ 。
(2)基态锑(Sb)原子的价电子排布式为___________ 。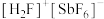 (氟酸锑)是一种超强酸,
(氟酸锑)是一种超强酸, 离子的空间构型为
离子的空间构型为___________ ,写出一种与 互为等电子体的分子
互为等电子体的分子___________ 。
(3)处于分界线的元素Al可形成多种化合物。
 中三种元素的基态原子的第一电离能从大到小的顺序是
中三种元素的基态原子的第一电离能从大到小的顺序是___________ (填元素符号)。
 中铝的杂化方式为
中铝的杂化方式为___________ ,其中阴离子的立体结构为___________ ,
(4)下列说法正确的是___________
a. 、SiC,
、SiC, 是空间构型均为正四面体的三种物质,键角与其他两种物质不同的是SiC
是空间构型均为正四面体的三种物质,键角与其他两种物质不同的是SiC
b.基态P原子中,电子占据的最高能级符号为M
c.Sb位于p区
d.升温实现液氨→氨气→氮气和氢气变化的阶段中,微粒间破坏的主要的作用力依次是氢键、极性共价键
(5)周期表中元素的性质呈现出周期性变化。元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能( )。第二周期部分元素的
)。第二周期部分元素的 变化趋势如图所示,其中除氮元素外,其他元素的
变化趋势如图所示,其中除氮元素外,其他元素的 自左而右依次增大的原因是
自左而右依次增大的原因是___________ ;氮元素的 呈现异常的原因是
呈现异常的原因是___________ 。


(1)写出元素①的元素符号
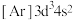 ,则该元素在元素周期表中的位置为
,则该元素在元素周期表中的位置为(2)基态锑(Sb)原子的价电子排布式为
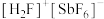 (氟酸锑)是一种超强酸,
(氟酸锑)是一种超强酸, 离子的空间构型为
离子的空间构型为 互为等电子体的分子
互为等电子体的分子(3)处于分界线的元素Al可形成多种化合物。
 中三种元素的基态原子的第一电离能从大到小的顺序是
中三种元素的基态原子的第一电离能从大到小的顺序是 中铝的杂化方式为
中铝的杂化方式为(4)下列说法正确的是
a.
 、SiC,
、SiC, 是空间构型均为正四面体的三种物质,键角与其他两种物质不同的是SiC
是空间构型均为正四面体的三种物质,键角与其他两种物质不同的是SiCb.基态P原子中,电子占据的最高能级符号为M
c.Sb位于p区
d.升温实现液氨→氨气→氮气和氢气变化的阶段中,微粒间破坏的主要的作用力依次是氢键、极性共价键
(5)周期表中元素的性质呈现出周期性变化。元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(
 )。第二周期部分元素的
)。第二周期部分元素的 变化趋势如图所示,其中除氮元素外,其他元素的
变化趋势如图所示,其中除氮元素外,其他元素的 自左而右依次增大的原因是
自左而右依次增大的原因是 呈现异常的原因是
呈现异常的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下图是元素周期表的一部分
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ||||||||||||||
| ⑥ | ⑦ | ⑧ | |||||||||||||||
| ⑨ | ⑩ |
(1)元素⑨的外围电子的电子排布图为
(2)元素③④⑤的电负性由大到小的顺序为
(3)如果在温度接近373K(100℃)时,根据M=m/n测定⑤的气态氢化物的相对分子质量,结果发现测定结果比理论值高,其原因是
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质。写出元素②的最高价氧化物的水化物与NaOH溶液反应的离子方程式
(5)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下面各题:
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
①在周期表中,最可能处于同一主族的是
②T元素最可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】决定物质性质的重要因素是物质结构。请回答下列问题:
(1)基态K原子中,核外电子占据最高能层的符号是_______ ,占据该能层电子的电子云轮廓图形状为______________ 。
(2)已知元素M是组成物质 的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号
的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号 至
至 表示)如表所示:
表示)如表所示:
元素M化合态常见化合价是_________ 价,其基态原子电子排布式为_______
(3) 的中心原子的杂化方式为
的中心原子的杂化方式为__________ ,键角为____________
(4)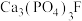 中非金属元素电负性由大到小的顺序为
中非金属元素电负性由大到小的顺序为_____________
(5)下列元素或化合物的性质变化顺序正确的是_______________
A.第一电离能: B.共价键的极性:
B.共价键的极性: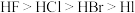
C.晶格能: D.热稳定性:
D.热稳定性: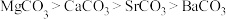
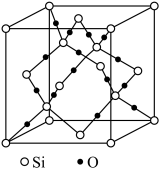
(6)如图是 晶胞,构成二氧化硅晶体结构的最小环是由
晶胞,构成二氧化硅晶体结构的最小环是由________ 个原子构成。已知晶胞参数为 ,则其晶胞密度为
,则其晶胞密度为________  。
。
(1)基态K原子中,核外电子占据最高能层的符号是
(2)已知元素M是组成物质
 的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号
的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号 至
至 表示)如表所示:
表示)如表所示: |  |  |  | 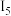 | |
电离能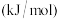 | 589.8 | 1145.4 | 4912.4 | 6491 | 8153 |
元素M化合态常见化合价是
(3)
 的中心原子的杂化方式为
的中心原子的杂化方式为(4)
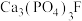 中非金属元素电负性由大到小的顺序为
中非金属元素电负性由大到小的顺序为(5)下列元素或化合物的性质变化顺序正确的是
A.第一电离能:
 B.共价键的极性:
B.共价键的极性: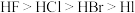
C.晶格能:
 D.热稳定性:
D.热稳定性: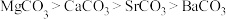
(6)如图是
 晶胞,构成二氧化硅晶体结构的最小环是由
晶胞,构成二氧化硅晶体结构的最小环是由 ,则其晶胞密度为
,则其晶胞密度为 。
。
您最近一年使用:0次



