X、Y、Z、R、Q是元素周期表中前四周期的元素,它们的原子序数依次增大且分别位于前四周期的各个周期中。对它们的性质及结构的描述如下:X原子的基态只有一种形状的电子云,并容易形成共价键;Y的基态原子有3个不同的能级,各能级中电子数相等;Z与Y同周期,其第一电离能高于同周期与之相邻的元素;R元素的电负性在同周期元素中最大;Q元素的基态原子在前四周期中未成对电子数最多。据此,请回答下列问题。
(1)写出X的元素符号______ ,基态Q原子的电子排布式______ 。
(2)R元素的基态原子核外电子共占据______ 个原子轨道?
(3)与Q同周期的元素的基态原子中最外层电子数与Q原子相同的元素有______ ?
(4)将X、Y、Z三种元素按电负性由大到小的顺序排列______ (用元素符号表示)。
(5)已知X、Y、Z组成的一种物质的结构式为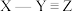 ,尝试推断该物质中Y元素的化合价
,尝试推断该物质中Y元素的化合价______ 。
(1)写出X的元素符号
(2)R元素的基态原子核外电子共占据
(3)与Q同周期的元素的基态原子中最外层电子数与Q原子相同的元素有
(4)将X、Y、Z三种元素按电负性由大到小的顺序排列
(5)已知X、Y、Z组成的一种物质的结构式为
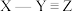 ,尝试推断该物质中Y元素的化合价
,尝试推断该物质中Y元素的化合价
20-21高二·全国·课时练习 查看更多[2]
更新时间:2022-11-27 16:22:57
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C为短周期元素,在周期表中所处的位置如图所示。A、C两元素的原子核外电子数之和等于B原子的质子数。
(1)写出A、B、C的元素符号_______ 、_______ 、_______ 。
(2)A元素位于周期表中第_______ 周期,第_______ 族;实验室对于实验结束后试管中残留的B物质用_______ 试剂清洗。(填化学式)
(3)C的原子结构示意图为_______ 。
(4)写出A的气态氢化物与其最高价氧化物对应的水化物反应的化学方程式_______ 。
(5)A、B、C三种元素所形成的气态氢化物中最稳定的是_______ 。(写出其氢化物的化学式)。
| A | C | |
| B |
(2)A元素位于周期表中第
(3)C的原子结构示意图为
(4)写出A的气态氢化物与其最高价氧化物对应的水化物反应的化学方程式
(5)A、B、C三种元素所形成的气态氢化物中最稳定的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表是元素周期表的一部分,对于表中元素①~⑧,填空回答:
(1)地壳中含量最多的元素是______ ,非金属性最强的元素是______ 。
(2)写出①的最简单的气态氢化物的电子式______ 。
(3)在第三周期主族元素中,单质氧化性最强的是_____ ,能形成的二元强酸是________ 。
(4)写出②的气态氢化物与②的最高价氧化物对应水化物反应的化学方程式_____ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)写出①的最简单的气态氢化物的电子式
(3)在第三周期主族元素中,单质氧化性最强的是
(4)写出②的气态氢化物与②的最高价氧化物对应水化物反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】几种主族元素在元素周期表中的位置如图,根据图中所示回答下列问题:
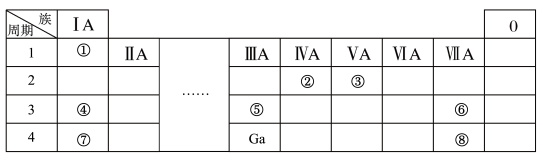
(1)①和④形成的是___________ (填“离子”或“共价”)化合物。
(2)图中某元素原子的最外电子层数是次外层电子数的2倍,该元素的一种核素的中子数为8,则该核素的质量数为___________ ,该元素的最高价氧化物电子式为___________ ,写出基于该最高价氧化物的物理性质的一种用途___________ 。
(3)⑤的单质与④的最高价氧化物对应水化物反应的离子方程式为___________ 。
(4)⑦的金属性强于④,从原子结构的角度解释其原因___________ 。
(5)设计实验比较⑧的单质和 的氧化性强弱,操作与现象是:取4mL KI溶液于试管中,
的氧化性强弱,操作与现象是:取4mL KI溶液于试管中,___________ 。
(6)金属镓(Ga)常用作光学玻璃、真空管、半导体的原料。根据Ga在上面元素周期表中的位置,预测Ga的化学性质
填写表格横线上物质的化学式,a是___________ ,b是___________ ,c是___________ 。

(1)①和④形成的是
(2)图中某元素原子的最外电子层数是次外层电子数的2倍,该元素的一种核素的中子数为8,则该核素的质量数为
(3)⑤的单质与④的最高价氧化物对应水化物反应的离子方程式为
(4)⑦的金属性强于④,从原子结构的角度解释其原因
(5)设计实验比较⑧的单质和
 的氧化性强弱,操作与现象是:取4mL KI溶液于试管中,
的氧化性强弱,操作与现象是:取4mL KI溶液于试管中,(6)金属镓(Ga)常用作光学玻璃、真空管、半导体的原料。根据Ga在上面元素周期表中的位置,预测Ga的化学性质
| 预测性质(所填物质类别不同) | 反应后可能的生成物(填化学式) |
Ga能与 反应 反应 | a___________ |
| Ga能与b___________反应 | 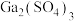 、c___________ 、c___________ |
| Ga能与NaOH溶液反应 | 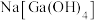 、 、 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E、F、G七种短周期主族元素的原子序数依次增大。A和E最外层电子数相同,短周期主族元素的原子中,E原子的半径最大;B、C和F在周期表中相邻,B、C同周期,C、F同主族,F原子的质子数是C原子质子数的2倍;A和C可形成两种常见的液态化合物X和Y(相对分子质量X<Y);D形成的分子为双原子分子。回答问题:
(1)D元素的名称为_________ ,F形成的离子的结构示意图为__________ 。
(2)元素E、F形成的化合物的电子式为_______ 。
(3)元素C、F氢化物的沸点C______ F(填“>”或“<”)。
(4)写出液态化合物Y的一种用途_________ 。
(5)用某种金属易拉罐与A、C、E组成的化合物的水溶液反应,产生的气体可充填气球,请写出该反应的离子方程式______ 。
(6)A、B、G三种元素两两组合形成的化合物在空气中相遇形成白烟,反应的化学方程式为_____ 。
(1)D元素的名称为
(2)元素E、F形成的化合物的电子式为
(3)元素C、F氢化物的沸点C
(4)写出液态化合物Y的一种用途
(5)用某种金属易拉罐与A、C、E组成的化合物的水溶液反应,产生的气体可充填气球,请写出该反应的离子方程式
(6)A、B、G三种元素两两组合形成的化合物在空气中相遇形成白烟,反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E是位于短周期的主族元素。已知:①热稳定性:HmD>HmC;②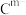 、
、 具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的
具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语 回答:
(1)HmDm的结构式___________________ 。
(2)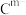 、
、 的还原性强的为:
的还原性强的为:_________ ,能证明其还原性强弱的离子方程式为_______ 。
(3)将E的单质通入A与D形成的化合物的水溶液中,其化学方程式为:_________________ 。
(4)常温下,将等物质的量浓度的HmC溶液和A的最高价氧化物对应的水化物溶液等体积混合,写出该反应的化学方程式__________________________________ 。在该溶液中溶质中含有的化学键类型是____________ 。
(5)在A、B、C、E单质中,符合下列转化关系的是_____________ (填元素符号)。

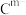 、
、 具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的
具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的(1)HmDm的结构式
(2)
 、
、 的还原性强的为:
的还原性强的为:(3)将E的单质通入A与D形成的化合物的水溶液中,其化学方程式为:
(4)常温下,将等物质的量浓度的HmC溶液和A的最高价氧化物对应的水化物溶液等体积混合,写出该反应的化学方程式
(5)在A、B、C、E单质中,符合下列转化关系的是

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】X、Y、Z、W、R、P、Q是短周期主族元素,部分信息如下表所示:
(1)R在自然界中有质量数为35和37的两种核素,它们之间的关系是互为___ 。
(2)Z的单质与水反应的化学方程式是___ ;R与Q两元素最高价氧化物水化物反应的离子方程式___ 。
(3)Y与R相比,非金属性较强的是___ (用元素符号表示),下列事实能证明这一结论的是___ (填字母序号)。
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性XR>YX4
c.Y与R形成的化合物中Y呈正价
(4)写出工业制取Y的单质的化学方程式___ 。
(5)反应3X2(g)+P2(g) 2PX3(g)过程中的能量变化如图所示回答下列问题:
2PX3(g)过程中的能量变化如图所示回答下列问题:
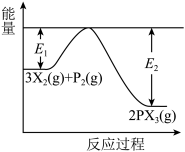
①该反应是___ 反应(填“吸热”“放热”);
②反应体系中加入催化剂对反应热是否有影响?___ ,原因是___ (从能量说明)
| X | Y | Z | W | R | P | Q | |
| 原子半径/nm | 0.154 | 0.074 | 0.099 | 0.075 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | -3,+5 | +3 | ||
| 其他 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
(1)R在自然界中有质量数为35和37的两种核素,它们之间的关系是互为
(2)Z的单质与水反应的化学方程式是
(3)Y与R相比,非金属性较强的是
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性XR>YX4
c.Y与R形成的化合物中Y呈正价
(4)写出工业制取Y的单质的化学方程式
(5)反应3X2(g)+P2(g)
 2PX3(g)过程中的能量变化如图所示回答下列问题:
2PX3(g)过程中的能量变化如图所示回答下列问题:
①该反应是
②反应体系中加入催化剂对反应热是否有影响?
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】已知A、B、C、D都是周期表中的短周期元素,它们的核电荷数依次增大。A原子、C原子的L能层中都有两个未成对的电子,C、D同主族。E、F都是第四周期元素,E原子核外有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满。根据以上信息填空:
(1)基态D原子中,电子占据的最高能层符号为____ ,D基态原子含有_____ 个未成对电子。
(2)E2+的价层电子排布图是_______ ,F原子的电子排布式是_____ 。
(3)A的最高价氧化物对应的水化物分子结构式为____ ,其中心原子采取的轨道杂化方式为____ ,B的气态氢化物的VSEPR模型为_____ 。
(4)化合物AC2、B2C和阴离子DAB-互为等电子体,它们结构相似,DAB-的结构式为____ 。
(5)配合物甲的焰色反应呈紫色,其内界由中心离子E3+与配位体AB-构成,配位数为6。甲的水溶液可以用于实验室中E2+的定性检验,检验E2+的离子方程式为______ 。
(1)基态D原子中,电子占据的最高能层符号为
(2)E2+的价层电子排布图是
(3)A的最高价氧化物对应的水化物分子结构式为
(4)化合物AC2、B2C和阴离子DAB-互为等电子体,它们结构相似,DAB-的结构式为
(5)配合物甲的焰色反应呈紫色,其内界由中心离子E3+与配位体AB-构成,配位数为6。甲的水溶液可以用于实验室中E2+的定性检验,检验E2+的离子方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】卤族元素包括F、Cl、Br等。
(1)如图曲线表示卤族元素某种性质随核电荷数的变化趋势,正确的是_______。
(2)利用“卤化硼法”可合成含B和N两种元素的功能陶瓷,图为其晶胞结构示意图,则每个晶胞中含有B原子(黑球)的个数为_______ ,该功能陶瓷的化学式为_______ 。

(3)BCl3和NCl3中心原子的杂化方式分别为_______ 和_______ ;写出一种与NCl3互为等电子体的离子_______ ;第一电离能介于B、N之间的第二周期元素有_______ 种。
(4)若BCl3的B原子与XYn的X原子通过配位键结合形成配合物,则该配合物中提供孤对电子的原子是_______ 。
(1)如图曲线表示卤族元素某种性质随核电荷数的变化趋势,正确的是_______。
A. | B. | C.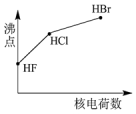 | D.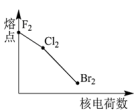 |

(3)BCl3和NCl3中心原子的杂化方式分别为
(4)若BCl3的B原子与XYn的X原子通过配位键结合形成配合物,则该配合物中提供孤对电子的原子是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子数相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2,其中C的常见化合价为+3,+2价。回答下列问题:
(1)C3+的电子排布式为___________ ,其单质的晶体中,原子间以___________ (填化学键类型)相互结合
(2)四种元素中第一电离能最小的是____ (填元素名称),电负性最大的元素的核外电子排布图为:____
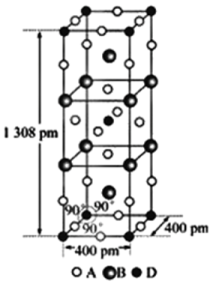
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。该化合物的化学式为___ ;D的配位数为___ ;
(1)C3+的电子排布式为
(2)四种元素中第一电离能最小的是
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。该化合物的化学式为

您最近一年使用:0次



