汽车剧烈碰撞时,安全气囊中发生反应: 。若还原产物为0.1 mol,则下列判断正确的是
。若还原产物为0.1 mol,则下列判断正确的是
 。若还原产物为0.1 mol,则下列判断正确的是
。若还原产物为0.1 mol,则下列判断正确的是| A.反应中NaN3是氧化剂 | B.反应生成N2的总物质的量为16 mol |
| C.氧化产物与还原产物的质量比为15:1 | D.反应过程中转移电子10 mol |
更新时间:2022-11-30 18:04:47
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】已知还原性:Fe2+>Br-,向100mlFeBr2溶液中通入3.36L(标准状况下)Cl2,反应后的溶液中Cl-和Br-的物质的量浓度相等,则原溶液中FeBr2的物质的量浓度为
| A.2mol/L | B.1.5mol/L | C.1mol/L | D.0.5mol/L |
您最近一年使用:0次
【推荐2】已知:氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:6Cl2+6Ca(OH)2 5CaCl2+Ca(ClO3)2+6H2O。实验室用足量石灰乳吸收从浓盐酸和 MnO2反应体系中导出的气体。生成物中 ClO-、
5CaCl2+Ca(ClO3)2+6H2O。实验室用足量石灰乳吸收从浓盐酸和 MnO2反应体系中导出的气体。生成物中 ClO-、 的物质的量(n)与反应时间(t)关系曲线为下图。下列说法正确的是
的物质的量(n)与反应时间(t)关系曲线为下图。下列说法正确的是

 5CaCl2+Ca(ClO3)2+6H2O。实验室用足量石灰乳吸收从浓盐酸和 MnO2反应体系中导出的气体。生成物中 ClO-、
5CaCl2+Ca(ClO3)2+6H2O。实验室用足量石灰乳吸收从浓盐酸和 MnO2反应体系中导出的气体。生成物中 ClO-、 的物质的量(n)与反应时间(t)关系曲线为下图。下列说法正确的是
的物质的量(n)与反应时间(t)关系曲线为下图。下列说法正确的是
A.图中曲线 I 表示 离子的物质的量随反应时间变化的关系 离子的物质的量随反应时间变化的关系 |
| B.反应消耗的 Ca(OH)2的物质的量为 0.25mol |
| C.若 n(Cl-)>n(ClO-),则产物一定为 Ca(ClO)2、Ca(ClO3)2、CaCl2 |
| D.若产物为 Ca(ClO)2、Ca(ClO3)2、CaCl2,则由 n(Cl-)和 n(ClO-)可计算吸收的 n(Cl2) |
您最近一年使用:0次
【推荐3】下列说法不正确的是
A.水热法制备Fe3O4纳米颗粒的反应为3Fe2++2S2O +O2+4OH-=Fe3O4+S4O +O2+4OH-=Fe3O4+S4O +2H2O,该反应中氧化剂和还原剂的物质的量之比为1:4 +2H2O,该反应中氧化剂和还原剂的物质的量之比为1:4 |
| B.在反应3BrF3+5H2O=HBrO3+Br2+9HF+O2↑中,若有3 mol水作还原剂时,被水还原的BrF3的物质的量为2mol |
| C.已知反应P+CuSO4+H2O→Cu3P+H3PO4+H2SO4(未配平),当反应中生成0.5molCu3P,参加反应的P为1.1mol |
| D.已知硝酸铵在400°C以上时,剧烈分解发生爆炸:4NH4NO3=3N2↑+2NO2↑+8H2O,其中被氧化的氮原子和被还原的氮原子的物质的量之比为3:1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】造纸、印刷等工业废水中含有大量的硫化物(主要成分为 ),可用如图转化方式除去,则下列说法错误的是
),可用如图转化方式除去,则下列说法错误的是
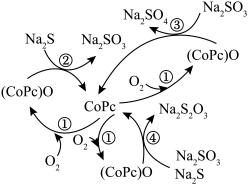
 ),可用如图转化方式除去,则下列说法错误的是
),可用如图转化方式除去,则下列说法错误的是
A. 溶液中存在 溶液中存在 |
B.反应②和③的转移电子数相等时,还原剂之比为 |
C.在废水处理过程中,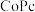 为催化剂, 为催化剂, 为氧化剂 为氧化剂 |
D.反应④中 与 与 等物质的量反应,反应的化学方程式为 等物质的量反应,反应的化学方程式为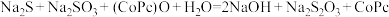 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】在一个氧化还原反应体系中反应物、生成物共六种粒子,Fe3+、NO3-、Fe2+、NH4+、H+、H2O,下列叙述正确的是( )
| A.该反应说明Fe(NO3)2溶液不宜加酸酸化 |
| B.该反应中氧化剂与还原剂物质的量之比为8:1 |
| C.若有1molNO3-发生还原反应,转移电子3mol |
| D.该反应能说明Fe3+的氧化性强于Fe2+ |
您最近一年使用:0次

 );②向(VO2)2SO4溶液中滴加浓盐酸,产生黄绿色气体,溶液变蓝。下列说法正确的是
);②向(VO2)2SO4溶液中滴加浓盐酸,产生黄绿色气体,溶液变蓝。下列说法正确的是



