亚硝酸钠(NaNO2)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生Na2O、N2和O2,亚硝酸钠水溶液呈碱性,能与AgNO3溶液反应生成难溶于水、易溶于酸的AgNO2.回答下列问题:
(1)下列方法不能用来区分固体NaNO2和NaCl的是_______(填序号)。
(2)误食NaNO2会导致人体血红蛋白中的Fe2+转化为Fe3+而中毒,该过程中NaNO2表现出的性
质与下列_______ (填空)反应中H2O2表现出的性质相同。
A.2H2O2 2H2O+O2↑
2H2O+O2↑
B.H2O2+Cl2=2HCl+O2↑
C. H2O2+H2SO4+2KI=2H2O+I2+K2SO4
D.5H2O2+2KMnO4+6HCl=2MnCl2+2KCl+5O2↑+8H2O
服用维生素C可将Fe3+转化为Fe2+从而解毒,维生素C的作用是_______ (填“氧化剂”“还原剂”或“既是氧化剂又是还原剂”)。
(3)可用Cl2将溶液中的NO 氧化为NO
氧化为NO ,同时生成Cl-,已知Cl2+NaNO2+H2O=2HCl+NaNO3,则该反应的离子方程式为
,同时生成Cl-,已知Cl2+NaNO2+H2O=2HCl+NaNO3,则该反应的离子方程式为_______ 。
(1)下列方法不能用来区分固体NaNO2和NaCl的是_______(填序号)。
| A.分别溶于水并滴加酚酞试液 | B.分别溶于水并滴加HNO3酸化的AgNO3溶液 |
| C.分别加强热并收集气体检验 | D.用筷子分别蘸取固体品尝味道 |
质与下列
A.2H2O2
 2H2O+O2↑
2H2O+O2↑ B.H2O2+Cl2=2HCl+O2↑
C. H2O2+H2SO4+2KI=2H2O+I2+K2SO4
D.5H2O2+2KMnO4+6HCl=2MnCl2+2KCl+5O2↑+8H2O
服用维生素C可将Fe3+转化为Fe2+从而解毒,维生素C的作用是
(3)可用Cl2将溶液中的NO
 氧化为NO
氧化为NO ,同时生成Cl-,已知Cl2+NaNO2+H2O=2HCl+NaNO3,则该反应的离子方程式为
,同时生成Cl-,已知Cl2+NaNO2+H2O=2HCl+NaNO3,则该反应的离子方程式为
更新时间:2022-12-02 15:02:57
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求写出以下离子方程式。
(1)碳酸氢钠溶液与氢氧化钠溶液反应______ 。
(2)氢氧化钙溶液与过量碳酸氢钠溶液反应______ 。
(3)钠与硫酸铜溶液反应______ 。
(4)制漂白粉的原理______ 。
(5)将铜片插入硝酸银溶液中:______ ;
(6)氯气与水反应:______ ;
(7)将氧化镁与稀盐酸混合:______ ;
(8)碳酸钡溶于稀盐酸中:______ ;
(9)向氢氧化钠溶液中通入过量CO2______ ;
(10)氯气通入NaOH溶液中:______ 。
(1)碳酸氢钠溶液与氢氧化钠溶液反应
(2)氢氧化钙溶液与过量碳酸氢钠溶液反应
(3)钠与硫酸铜溶液反应
(4)制漂白粉的原理
(5)将铜片插入硝酸银溶液中:
(6)氯气与水反应:
(7)将氧化镁与稀盐酸混合:
(8)碳酸钡溶于稀盐酸中:
(9)向氢氧化钠溶液中通入过量CO2
(10)氯气通入NaOH溶液中:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】写出下列反应的离子方程式:
(1)可溶性多元弱酸(或其酸酐)与碱溶液反应。如CO2通入NaOH溶液中:
①碱过量:___________ 。
②碱不足:___________ 。
(2)Ca(HCO3)2溶液与NaOH溶液反应:
①Ca(HCO3)2少量:___________ 。
②Ca(HCO3)2足量:___________ 。
(1)可溶性多元弱酸(或其酸酐)与碱溶液反应。如CO2通入NaOH溶液中:
①碱过量:
②碱不足:
(2)Ca(HCO3)2溶液与NaOH溶液反应:
①Ca(HCO3)2少量:
②Ca(HCO3)2足量:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】完成下列问题。
(1)①含0.4 mol K+的K2SO4中所含的 的物质的量是
的物质的量是_______ 。
②2.3 g金属钠中含电子的物质的量为_______ mol,在跟足量水反应中失去电子的物质的量为_______ mol。
(2)①48 g RO 中,核外电子总数比质子总数多6.02×1023个,则R元素的摩尔质量为
中,核外电子总数比质子总数多6.02×1023个,则R元素的摩尔质量为_______ 。
②有一真空瓶的质量为M1 g,该瓶充入空气后总质量为M2 g;在相同状况下,若改充某气体A后,总质量为M3 g,则A的相对分子质量为_______ 。
(3)一定量的氢气在氯气中燃烧,所得混合物用100 mL 3.00 mol/L的NaOH溶液(密度为1.12 g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.050 0 mol。
①原NaOH溶液的质量分数为_______ ;
②所得溶液中Cl-的物质的量为_______ mol。
(4)在下列物质中:Na2CO3、稀盐酸、 CaO、CO2、Fe。
①属于混合物的是_______ ;
②属于电解质的是_______ ;
③属于非电解质的是_______ ;
④稀盐酸和CaO反应的离子方程式_______ ;
(5)酸性KMnO4溶液氧化FeCl2溶液,请将该反应的离子方程式补充完整并配平:_______ 。
 +Fe2++______=Mn2++Fe3++_______
+Fe2++______=Mn2++Fe3++_______
(1)①含0.4 mol K+的K2SO4中所含的
 的物质的量是
的物质的量是②2.3 g金属钠中含电子的物质的量为
(2)①48 g RO
 中,核外电子总数比质子总数多6.02×1023个,则R元素的摩尔质量为
中,核外电子总数比质子总数多6.02×1023个,则R元素的摩尔质量为②有一真空瓶的质量为M1 g,该瓶充入空气后总质量为M2 g;在相同状况下,若改充某气体A后,总质量为M3 g,则A的相对分子质量为
(3)一定量的氢气在氯气中燃烧,所得混合物用100 mL 3.00 mol/L的NaOH溶液(密度为1.12 g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.050 0 mol。
①原NaOH溶液的质量分数为
②所得溶液中Cl-的物质的量为
(4)在下列物质中:Na2CO3、稀盐酸、 CaO、CO2、Fe。
①属于混合物的是
②属于电解质的是
③属于非电解质的是
④稀盐酸和CaO反应的离子方程式
(5)酸性KMnO4溶液氧化FeCl2溶液,请将该反应的离子方程式补充完整并配平:
 +Fe2++______=Mn2++Fe3++_______
+Fe2++______=Mn2++Fe3++_______
您最近一年使用:0次
【推荐1】氧化还原反应在生产生活中应用十分广泛,回答下列问题:
(1)在S2-、Fe2+、Mg2+、I-、H+、S粒子中,只有氧化性的是__ ,只有还原性的是__ ,既有氧化性又有还原性的是__ 。
(2)有下列三个在溶液中发生的氧化还原反应:
Ⅰ.2FeCl3+2KI=2FeCl2+2KCl+I2;
Ⅱ.2FeCl2+Cl2=2FeCl3;
Ⅲ.K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2↑,则
①FeCl3、I2、Cl2、K2Cr2O7的氧化性由强到弱依次是__ 。
②Cr2O 、I-在强酸性溶液中能否大量共存?
、I-在强酸性溶液中能否大量共存?___ (请先回答“能”或“否”,“能”不用解释,“否”需要加以解释)。
(3)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为3Cl2+8NH3=6NH4Cl+N2,该反应中氧化剂为__ (填化学式),标准状况下,每生成2.24LN2,反应中转移的电子的物质的量为__ mol。
(4)Mn2+、Bi3+、BiO 、MnO
、MnO 、H+、H2O组成的一个氧化还原反应体系中,发生BiO
、H+、H2O组成的一个氧化还原反应体系中,发生BiO →Bi3+的反应过程,将以上物质组成一个正确的离子方程式,并用单线桥标出电子转移方向和数目:
→Bi3+的反应过程,将以上物质组成一个正确的离子方程式,并用单线桥标出电子转移方向和数目:__ 。
(1)在S2-、Fe2+、Mg2+、I-、H+、S粒子中,只有氧化性的是
(2)有下列三个在溶液中发生的氧化还原反应:
Ⅰ.2FeCl3+2KI=2FeCl2+2KCl+I2;
Ⅱ.2FeCl2+Cl2=2FeCl3;
Ⅲ.K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2↑,则
①FeCl3、I2、Cl2、K2Cr2O7的氧化性由强到弱依次是
②Cr2O
 、I-在强酸性溶液中能否大量共存?
、I-在强酸性溶液中能否大量共存?(3)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为3Cl2+8NH3=6NH4Cl+N2,该反应中氧化剂为
(4)Mn2+、Bi3+、BiO
 、MnO
、MnO 、H+、H2O组成的一个氧化还原反应体系中,发生BiO
、H+、H2O组成的一个氧化还原反应体系中,发生BiO →Bi3+的反应过程,将以上物质组成一个正确的离子方程式,并用单线桥标出电子转移方向和数目:
→Bi3+的反应过程,将以上物质组成一个正确的离子方程式,并用单线桥标出电子转移方向和数目:
您最近一年使用:0次
【推荐2】(1)从氧化还原的角度分析水在下列化学反应中的作用(从氧化剂、还原剂角度分析)。
①电解水:_____________________________________________________ 。
②钠和水的反应(2Na+2H2O=2NaOH+H2↑):_______________________________ 。
③氟气和水反应(2F2+2H2O=4HF+O2):_______________________________ 。
④氯气和水反应(Cl2+H2O=HCl+HClO):______________________________ 。
(2)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。该反应体系中还原产物是________ ;若反应中转移了0.3 mol电子,则氧化产物的质量是________ g。
(3)将少量Cl2通入FeBr2的溶液中,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl−,这个事实说明具有还原性的粒子还原性强弱顺序为____________ 。足量Cl2通入FeBr2溶液中发生反应的离子方程式为________________ 。
①电解水:
②钠和水的反应(2Na+2H2O=2NaOH+H2↑):
③氟气和水反应(2F2+2H2O=4HF+O2):
④氯气和水反应(Cl2+H2O=HCl+HClO):
(2)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。该反应体系中还原产物是
(3)将少量Cl2通入FeBr2的溶液中,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl−,这个事实说明具有还原性的粒子还原性强弱顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知反应:①SO3+H2O=H2SO4 ②Cl2+H2O=HCl+HClO
③2F2+H2O=4HF+O2↑ ④2Na+2H2O=2NaOH+H2↑
⑤Na2O+H2O=2NaOH ⑥SiO2+2NaOH=Na2SiO3+H2O
⑦Fe2O3+3H2 2Fe+3H2O
2Fe+3H2O
(1)上述反应中,不属于氧化还原反应的有_________ (填序号,下同)
H2O被氧化的是_________________ ;H2O做氧化剂的是_________________ ;
属于氧化还原反应,但反应物中的H2O既不被氧化也不被还原的是_________ 。
(2)写出化学方程式①的离子方程式:____________________________________
(3)用单、双线桥法表示反应⑦电子转移的方向和数目:_____________________
③2F2+H2O=4HF+O2↑ ④2Na+2H2O=2NaOH+H2↑
⑤Na2O+H2O=2NaOH ⑥SiO2+2NaOH=Na2SiO3+H2O
⑦Fe2O3+3H2
 2Fe+3H2O
2Fe+3H2O(1)上述反应中,不属于氧化还原反应的有
H2O被氧化的是
属于氧化还原反应,但反应物中的H2O既不被氧化也不被还原的是
(2)写出化学方程式①的离子方程式:
(3)用单、双线桥法表示反应⑦电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在反应:K2Cr2O7+14HCl(浓)===2KCl+2CrCl3+3Cl2↑+7H2O中,用氧化还原反应的知识分析:____ 是氧化剂,_____ 是还原剂,____ 是还原产物,____ 是氧化产物,电子转移总数是___ e-,用“双线桥法”表示反应中电子转移的方向和数目:__________________________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】过渡元素现代社会得到广泛应用。请回答下列问题:
(1)稀土金属包括______ 、钇和钪,在合金中加入稀土金属,能大大改善合金的性能,稀土金属被称为“冶金工业的维生素”。
(2)钼系催化剂:(NH4)2O·4MoO3·2H2O主要用于石油炼制和化学工业中。高温用H2还原(NH4)2O·4MoO3·2H2O得金属钼,氧化剂与还原剂物质的量之比为______ 。
(3)ZnO、ZnS、Se共热可制备荧光材料ZnSe,同时产生了 ,写出该反应的化学方程式:
,写出该反应的化学方程式:______ 。
(4)高锰酸钾因其强氧化性和溶液颜色变化明显而被用于物质的鉴定。请写出SO2与酸性高锰酸钾溶液反应的离子方程式:______ 。(高锰酸根离子的还原产物为Mn2+)
(5)V2O5是化工生产中重要的催化剂,可用于制备硫酸和彩色玻璃。在硫酸酸化条件下,V2O5可与草酸(H2C2O4)溶液反应得到含VO2+的溶液,反应的离子方程式为______ 。
(6)镍主要用于合金(可用来制造货币等)及用作催化剂(如氢化的催化剂),常见化合价为+2价、+3价。已知镍的氢氧化物均不溶于水。请写出碱性条件下Ni2+与溴水反应的离子方程式:______ 。
(1)稀土金属包括
(2)钼系催化剂:(NH4)2O·4MoO3·2H2O主要用于石油炼制和化学工业中。高温用H2还原(NH4)2O·4MoO3·2H2O得金属钼,氧化剂与还原剂物质的量之比为
(3)ZnO、ZnS、Se共热可制备荧光材料ZnSe,同时产生了
 ,写出该反应的化学方程式:
,写出该反应的化学方程式:(4)高锰酸钾因其强氧化性和溶液颜色变化明显而被用于物质的鉴定。请写出SO2与酸性高锰酸钾溶液反应的离子方程式:
(5)V2O5是化工生产中重要的催化剂,可用于制备硫酸和彩色玻璃。在硫酸酸化条件下,V2O5可与草酸(H2C2O4)溶液反应得到含VO2+的溶液,反应的离子方程式为
(6)镍主要用于合金(可用来制造货币等)及用作催化剂(如氢化的催化剂),常见化合价为+2价、+3价。已知镍的氢氧化物均不溶于水。请写出碱性条件下Ni2+与溴水反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ. 与浓盐酸反应会生成
与浓盐酸反应会生成 ,该反应的化学方程式为
,该反应的化学方程式为
回答下列问题:
(1)浓盐酸在反应中显示出来的性质是_______(填字母)
(2)配平化学方程式:_______ 。
 _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
(3)某一反应体系有反应物和生成物共五种物质: 、
、 (Cr元素的化合价为+6)、
(Cr元素的化合价为+6)、 (Cr元素的化合价为+3)、
(Cr元素的化合价为+3)、 、
、 ,已知该反应中
,已知该反应中 只发生如下过程:
只发生如下过程:
①该反应中的还原剂是_______
②该反应中,发生还原反应的过程是_______
③写出该反应的化学方程式:_______
Ⅱ.下列几种导电性变化图像,把符合要求的图像序号填在相应的题目后面横线上
A. B.
B.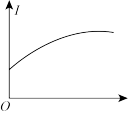 C.
C.
(4)①向 溶液中通入
溶液中通入 直至过量
直至过量_______ (提示: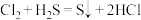 )
)
②向 溶液通入少量HCl
溶液通入少量HCl_______
③向氨水中通入HCl直至过量_______
④向饱和石灰水中不断通入
_______
 与浓盐酸反应会生成
与浓盐酸反应会生成 ,该反应的化学方程式为
,该反应的化学方程式为
回答下列问题:
(1)浓盐酸在反应中显示出来的性质是_______(填字母)
| A.只有还原性 | B.还原性和酸性 | C.只有氧化性 | D.氧化性和酸性 |
 _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
(3)某一反应体系有反应物和生成物共五种物质:
 、
、 (Cr元素的化合价为+6)、
(Cr元素的化合价为+6)、 (Cr元素的化合价为+3)、
(Cr元素的化合价为+3)、 、
、 ,已知该反应中
,已知该反应中 只发生如下过程:
只发生如下过程:
①该反应中的还原剂是
②该反应中,发生还原反应的过程是
③写出该反应的化学方程式:
Ⅱ.下列几种导电性变化图像,把符合要求的图像序号填在相应的题目后面横线上
A.
 B.
B. C.
C.
(4)①向
 溶液中通入
溶液中通入 直至过量
直至过量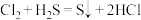 )
)②向
 溶液通入少量HCl
溶液通入少量HCl③向氨水中通入HCl直至过量
④向饱和石灰水中不断通入

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】只用一种试剂就能区别下列四种溶液:NaHCO3、NaCl、 Na2SO3、 BaCl2;则该试剂应是_____________ 溶液。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】NaNO2是一种白色易溶于水的固体,溶液呈碱性,其外观与氯化钠相似,有咸味,俗称工业盐;是一 种重要的化学试剂、漂白剂和食品添加剂。已知亚硝酸盐能被溴水氧化,在酸性条件下能氧化亚铁离子; 亚硝酸银是可溶于稀硝酸的白色沉淀。
请完成以下填空:
(1)N原子最外层电子的轨道排布式为_______ ;用一个事实说明氮和氧非金属强弱_______ 。
(2)酸性条件下,NaNO2溶液只能将I-氧化为I2,同时生成NO。写出此反应①的离子方程式并标出电子转移的方向和数目______ 。
(3)氯气、浓硝酸、酸性高锰酸钾等都是常用的强氧化剂,工业上氧化卤水中的I-提取单质I2选择了价格并不便宜的亚硝酸钠,可能的原因是_______ 。
(4)在盐酸溶液中加入亚硝酸钠溶液至中性,则c(Cl-)_____ c(HNO2)(填“<”、“>”或“=”)。
(5)设计一种鉴别亚硝酸钠和氯化钠的实验方案。_______
请完成以下填空:
(1)N原子最外层电子的轨道排布式为
(2)酸性条件下,NaNO2溶液只能将I-氧化为I2,同时生成NO。写出此反应①的离子方程式并标出电子转移的方向和数目
(3)氯气、浓硝酸、酸性高锰酸钾等都是常用的强氧化剂,工业上氧化卤水中的I-提取单质I2选择了价格并不便宜的亚硝酸钠,可能的原因是
(4)在盐酸溶液中加入亚硝酸钠溶液至中性,则c(Cl-)
(5)设计一种鉴别亚硝酸钠和氯化钠的实验方案。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】碘是人体不可缺少的元素,为了防止碘缺乏病,人们食用加碘盐。加碘盐就是在精盐中添加一定量的KIO3。某研究性学习小组利用下列反应原理检验某加碘盐中是否含碘:KIO3+KI+H2SO4—→K2SO4+I2+H2O。
(1)配平上述化学方程式并用双线桥表示反应中的电子转移情况。____________ 当有0.1 mol KIO3参加反应时,转移电子的数目为_________ 。
(2)向KI-H2SO4溶液中加入适量碘盐,充分振荡,将生成的碘单质与K2SO4溶液分离,实验操作方法是_________ ,主要仪器名称是_________ ,所需试剂是______ (填序号)。
A.酒精B.氯化钡溶液C.四氯化碳D.淀粉溶液
(3)通过上述实验,判断食盐中含碘的证据是__________________ 。
(1)配平上述化学方程式并用双线桥表示反应中的电子转移情况。
(2)向KI-H2SO4溶液中加入适量碘盐,充分振荡,将生成的碘单质与K2SO4溶液分离,实验操作方法是
A.酒精B.氯化钡溶液C.四氯化碳D.淀粉溶液
(3)通过上述实验,判断食盐中含碘的证据是
您最近一年使用:0次



