丁二酮肟常用于检验 。在稀氨水中,丁二酮肟与
。在稀氨水中,丁二酮肟与 反应生成鲜红色沉淀,其结构如图所示。下列说法正确的是
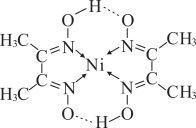
反应生成鲜红色沉淀,其结构如图所示。下列说法正确的是
 。在稀氨水中,丁二酮肟与
。在稀氨水中,丁二酮肟与 反应生成鲜红色沉淀,其结构如图所示。下列说法正确的是
反应生成鲜红色沉淀,其结构如图所示。下列说法正确的是
A. 与4个 与4个 原子共平面 原子共平面 |
B. 的价电子排布式为 的价电子排布式为 |
| C.该结构中存在的化学键有极性键、配位键和氢键 |
| D.丁二酮肟中,C、N、O的第一电离能及电负性均依次增大 |
更新时间:2022-12-16 07:41:14
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】根据下表提供的信息(部分短周期元素的原子半径及主要化合价),下列判断正确的是
元素代号 | A | B | C | D | E |
原子半径/nm |
|
|
|
|
|
主要化合价 |
|
|
|
|
|
| A.C为Mg | B.B的最高价氧化物能不溶于强碱 |
C.非金属性: | D.元素的第一电离能: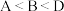 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列比较正确的是
| A.第一电离能:I1(P)>I1(S) | B.离子半径: r(Al3+)>r(O2-) |
| C.能量: E(3p)> E(4s) | D.电负性: P>O |
您最近一年使用:0次
【推荐1】W、X、Y、Z为原子序数依次增大的短周期元素,X是元素周期表中电负性最强的元素,X和Z同主族,W和Y同主族,这四种元素组成的两种化合物的结构如图所示。下列说法正确的是
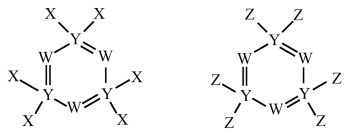

| A.最简单氢化物的稳定性:X>W>Y | B.最高价含氧酸的酸性:W>Y>Z |
| C.WZ3的空间结构为平面三角形 | D.电负性:Z>X>W |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】图表资料可以为我们提供很多信息,下列关于图表提供的资料或应用的说法中,不正确的是:
| A.利用元素周期表可以预测新元素的原子结构和性质 |
| B.根据酸、碱、盐的溶解性表,可确定酸、碱、盐的溶解度 |
| C.根据电负性表,可判定2种元素形成的化学键是离子键还是共价键 |
| D.核磁共振氢谱可以用来测定分子中H原子种类和个数比 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】将 置于浓盐酸中,可形成亮黄色的
置于浓盐酸中,可形成亮黄色的 。下列说法正确的是
。下列说法正确的是
 置于浓盐酸中,可形成亮黄色的
置于浓盐酸中,可形成亮黄色的 。下列说法正确的是
。下列说法正确的是A. 中的配位键是 中的配位键是 键 键 |
B. 中 中 提供孤对电子 提供孤对电子 |
| C.加水稀释亮黄色溶液后,溶液可能变黄色 |
D. 溶于浓盐酸只发生物理变化 溶于浓盐酸只发生物理变化 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】某化合物的分子结构如图所示,其分子内不含有
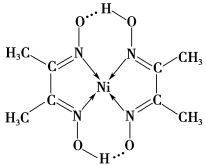

| A.离子键 | B.共价键 |
| C.极性键 | D.配位键 |
您最近一年使用:0次



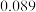
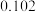
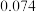



 、
、 、
、
 比
比 的酸性强的原因是
的酸性强的原因是 键的键能比
键的键能比 键的键能大
键的键能大 ②CH4③OH-④
②CH4③OH-④ ⑤Fe(CO)5⑥Fe(SCN)3⑦H3O+⑧Ag(NH3)2OH⑨[B(OH)4]-
⑤Fe(CO)5⑥Fe(SCN)3⑦H3O+⑧Ag(NH3)2OH⑨[B(OH)4]-

