实验室欲配制100 mL 1.0 mol·L-1的Na2CO3溶液。
(1)配制上述溶液,下列没有用到的仪器是_______(填字母)。
(2)除上述仪器外,还一定用到的玻璃仪器是_______ 。
(3)用托盘天平称取Na2CO3·10H2O固体的质量为_______ g,从下表中选择称量Na2CO3·10H2O固体所需要的仪器_______ (填字母)。
(4)下列情况使所配溶液的浓度如何变化?
①未洗涤溶解Na2CO3·10H2O的烧杯_______ (填“偏大”“偏小”或“不变”,下同)。
②容量瓶使用前用蒸馏水洗过,内壁附有水珠_______ 。
③定容时加蒸馏水超过了刻度线,将多出的液体吸出_______ 。
④定容时俯视容量瓶刻度线_______ 。
(1)配制上述溶液,下列没有用到的仪器是_______(填字母)。
| A.烧杯 | B.大试管 | C.胶头滴管 | D.100 mL容量瓶 |
(3)用托盘天平称取Na2CO3·10H2O固体的质量为
| 名称 | 托盘天平(带砝码) | 烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |  |  |  |  |  |
| 标号 | a | b | c | d | e | f |
①未洗涤溶解Na2CO3·10H2O的烧杯
②容量瓶使用前用蒸馏水洗过,内壁附有水珠
③定容时加蒸馏水超过了刻度线,将多出的液体吸出
④定容时俯视容量瓶刻度线
更新时间:2022-12-05 20:52:25
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】硫代硫酸钠(Na2S2O3)商品名“海波”,俗名“大苏打”,分析化学上常用于滴定实验。某化学兴趣小组在实验室制备硫代硫酸钠晶体并探究其化学性质
已知:Na2SO3 + S = Na2S2O3
I.制备Na2S2O3
(1)如图,组装好仪器,检验完气密性(气密性良好),各装置试剂均装入后的下一步操作是______
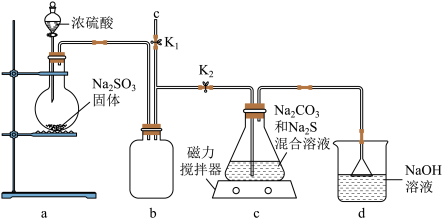
(2)反应开始后,C中发生了多个化学反应。写出其中任意一个非氧化还原反应的方程式_____________
(3)装置c中反应结束后, 先关闭分液漏斗旋塞,在e处连 接盛NaOH溶液的注射器,再关闭K2打开K1,其目的是______ 。待c中溶液冷却后,倒入蒸发皿,通过加热蒸发、冷却结晶和干燥等操作获得Na2S2O3·5H2O晶体。
Ⅱ.探究Na2S2O3的部分化学性质
【提出假设】
假设一:Na2S2O3与Na2SO4结构相似,化学性质也应该相似,因此室温时Na2S2O3溶液pH=7。
假设二:从S元素的化合价推测Na2S2O3具有较强的还原性。
(4)【验证假设】配制适量Na2S2O3溶液,进行如下实验(请填空)
【实验结论】_____________
Ⅲ:用Na2S2O3的溶液测定溶液中ClO2的物质的量浓度,可进行以下实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100 mL试样。
步骤2:量取V1mL试样加入到锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,摇匀,在暗处静置30分钟。(已知:ClO2+I-+H+—I2+Cl-+H2O 未配平)
步骤3:以淀粉溶液作指示剂,用c mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL。(已知:I2+2S2O =2I-+S4O
=2I-+S4O )
)
(5)根据上述步骤计算出原ClO2溶液的物质的量浓度为_______ mol·L-1(用含字母的代数式表示)
已知:Na2SO3 + S = Na2S2O3
I.制备Na2S2O3
(1)如图,组装好仪器,检验完气密性(气密性良好),各装置试剂均装入后的下一步操作是

(2)反应开始后,C中发生了多个化学反应。写出其中任意一个非氧化还原反应的方程式
(3)装置c中反应结束后, 先关闭分液漏斗旋塞,在e处连 接盛NaOH溶液的注射器,再关闭K2打开K1,其目的是
Ⅱ.探究Na2S2O3的部分化学性质
【提出假设】
假设一:Na2S2O3与Na2SO4结构相似,化学性质也应该相似,因此室温时Na2S2O3溶液pH=7。
假设二:从S元素的化合价推测Na2S2O3具有较强的还原性。
(4)【验证假设】配制适量Na2S2O3溶液,进行如下实验(请填空)
| 实验操作 | 实验现象 | 现象解释(用离子方程式表示) | |
| 假设一 | 溶液pH=8 | ||
| 假设二 | 向溴水中滴入适量Na2S2O3溶液 | 溴水褪色 |
Ⅲ:用Na2S2O3的溶液测定溶液中ClO2的物质的量浓度,可进行以下实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100 mL试样。
步骤2:量取V1mL试样加入到锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,摇匀,在暗处静置30分钟。(已知:ClO2+I-+H+—I2+Cl-+H2O 未配平)
步骤3:以淀粉溶液作指示剂,用c mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL。(已知:I2+2S2O
 =2I-+S4O
=2I-+S4O )
)(5)根据上述步骤计算出原ClO2溶液的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】已知某“84消毒液”瓶体部分标签如图1所示,该“84消毒液”通常稀释100倍(体积之比)后使用。回答下列问题:

(1)该“84消毒液”的物质的量浓度约为____ (结果精确到0.1)mol•L-1。
(2)某同学取100mL该“84消毒液”,稀释100倍后用于消毒,稀释后的溶液中c(Na+)=____ mol•L-1。
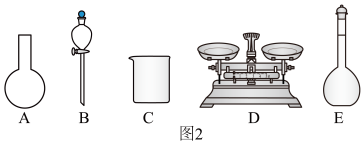
(3)该同学参阅此“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。下列说法正确的是____ (填字母)。
(4)若出现如下情况,对所配溶液浓度将有何影响?(填“偏高”、“偏低”或“无影响”)
①定容时仰视容量瓶刻度线____ 。
②向容量瓶中转移溶液时,不慎有液滴掉在容量瓶外面____ 。
③容量瓶在使用前刚刚配制完一定物质的量浓度的“84消毒液”而未洗净____ 。
④定容摇匀后发现液面低于容量瓶的刻度线,再用胶头滴管加水至刻度线____ 。
(5)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组用98%(ρ=1.84g•cm-3)的浓硫酸配制2L2.3mol•L-1的稀硫酸用于增强“84消毒液”的消毒能力,需用浓硫酸的体积为____ mL。

(1)该“84消毒液”的物质的量浓度约为
(2)某同学取100mL该“84消毒液”,稀释100倍后用于消毒,稀释后的溶液中c(Na+)=
(3)该同学参阅此“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。下列说法正确的是

| A.如图2所示的仪器中,有三种是不需要的,还需要一种玻璃仪器 |
| B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制 |
| C.需要称量NaClO固体的质量为123.0g |
| D.配制该溶液的操作顺序:计算→称量→溶解→移液→洗涤→定容→摇匀 |
①定容时仰视容量瓶刻度线
②向容量瓶中转移溶液时,不慎有液滴掉在容量瓶外面
③容量瓶在使用前刚刚配制完一定物质的量浓度的“84消毒液”而未洗净
④定容摇匀后发现液面低于容量瓶的刻度线,再用胶头滴管加水至刻度线
(5)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组用98%(ρ=1.84g•cm-3)的浓硫酸配制2L2.3mol•L-1的稀硫酸用于增强“84消毒液”的消毒能力,需用浓硫酸的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】“84消毒液”是家居常用的防疫用品,某小组同学查看包装说明,得到如下信息:
该小组同学进行了如下实验.回答下列问题:
(1)稀释:将“84消毒液”原液稀释配制成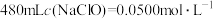 的溶液。
的溶液。
①稀释过程中,需要用到的玻璃仪器有烧杯、玻璃棒、量筒、_________ 、__________ 。
②稀释时,需要取用__________  “84消毒液”原液。
“84消毒液”原液。
③下列操作会使溶液中 浓度偏高的是
浓度偏高的是____________ (填标号)。
A.取用久置的“84消毒液”原液进行稀释
B.定容时,俯视刻度线
C.量取“84消毒液”原液时,仰视读数
D.定容摇匀后,液面低于刻度线,再加水至刻度线
(2)利用如图所示装置探究84消毒液与洁厕灵的反应:

①将注射器中的洁厕灵注入试管中,可观察到试管内产生_____ 色气体,pH试纸________ ,淀粉KI试纸上发生的离子反应方程式为___________ 。
②棉花团蘸取的溶液A是___________ ,其作用是_________________ 。
③该小组查资料得:“84消毒液”也不能与双氧水混合,两者混合会产生一种无色无味气体,使其消毒能力大大降低,写出该反应的化学方程式__________________ 。
| 84消毒液 【有效成分】  【规格】  【浓度】 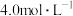 注:①按一定比例稀释后使用 ②不得与酸性产品(如洁厕灵)同时使用 |
(1)稀释:将“84消毒液”原液稀释配制成
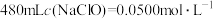 的溶液。
的溶液。①稀释过程中,需要用到的玻璃仪器有烧杯、玻璃棒、量筒、
②稀释时,需要取用
 “84消毒液”原液。
“84消毒液”原液。③下列操作会使溶液中
 浓度偏高的是
浓度偏高的是A.取用久置的“84消毒液”原液进行稀释
B.定容时,俯视刻度线
C.量取“84消毒液”原液时,仰视读数
D.定容摇匀后,液面低于刻度线,再加水至刻度线
(2)利用如图所示装置探究84消毒液与洁厕灵的反应:

①将注射器中的洁厕灵注入试管中,可观察到试管内产生
②棉花团蘸取的溶液A是
③该小组查资料得:“84消毒液”也不能与双氧水混合,两者混合会产生一种无色无味气体,使其消毒能力大大降低,写出该反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】用质量分数为36.5%的盐酸(密度为1.16g·cm-3)配制1mol·L-1的稀盐酸。现实验室仅需要这种盐酸220mL,试回答下列问题:
(1)配制稀盐酸时,应选用容量为_____ mL的容量瓶。
(2)计算已知盐酸的物质的量浓度为__________ 。
(3)经计算需要_____ mL浓盐酸,在量取时宜选用下列量筒中的________ 。
A 5mL B 10mL C 25mL D 50mL
(4)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入相应规格的容量瓶中。
②往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2cm时,改用胶头滴管加蒸馏水,使溶液的液面与瓶颈的刻度标线相切。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是__________ (填序号)。
(5)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,其配制的稀盐酸浓度是______ (填“偏高”、“偏低”或“无影响”).若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶,则配制的稀盐酸浓度是______ (填“偏高”、“偏低”或“无影响”)。
(1)配制稀盐酸时,应选用容量为
(2)计算已知盐酸的物质的量浓度为
(3)经计算需要
A 5mL B 10mL C 25mL D 50mL
(4)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入相应规格的容量瓶中。
②往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2cm时,改用胶头滴管加蒸馏水,使溶液的液面与瓶颈的刻度标线相切。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是
(5)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,其配制的稀盐酸浓度是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】“84消毒液”是一种以NaClO为主的高效消毒剂,被广泛用于宾馆、旅游、医院、食品加工行业、家庭等的卫生消毒。某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:

(1)此“84消毒液”的物质的量浓度约为________ 。(计算结果保留一位小数)
(2)某同学量取100mL此“84消毒液”,按说明要求稀释后用于消毒,则稀释后的溶液中c(Na+)=___ mol/L。
(3)该同学参阅读该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为24%的消毒液。
①如图所示的仪器中配制溶液需要使用的是________________ (填仪器序号),还缺少的玻璃仪器是______________ 。
②该同学配制此溶液需称取称量NaClO固体的质量为_________________ g。
(4)若实验遇下列情况,导致所配溶液的物质的量浓度偏高的是____________ (填序号)。
a.定容时俯视刻度线 b.转移前,容量瓶内有蒸馏水
c.未冷至室温就转移定容 d.定容时水多加了,用胶头滴管吸出
84消毒液 【有效成分】NaClO 【规格】1000mL 【质量分数】24% 【密度】1.18g/cm3 |

(1)此“84消毒液”的物质的量浓度约为
(2)某同学量取100mL此“84消毒液”,按说明要求稀释后用于消毒,则稀释后的溶液中c(Na+)=
(3)该同学参阅读该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为24%的消毒液。
①如图所示的仪器中配制溶液需要使用的是
②该同学配制此溶液需称取称量NaClO固体的质量为
(4)若实验遇下列情况,导致所配溶液的物质的量浓度偏高的是
a.定容时俯视刻度线 b.转移前,容量瓶内有蒸馏水
c.未冷至室温就转移定容 d.定容时水多加了,用胶头滴管吸出
您最近一年使用:0次



