氧化镁是优质的耐高温材料。某兴趣小组利用菱镁矿(主要成分为MgCO3,还含有少量SiO2、Al2O3等杂质)设计制备氧化镁的流程如图:

(1)步骤(Ⅰ)中分离操作的名称是_______ 。
(2)步骤(I)分离出的滤渣中主要含有_______ ,它属于_______ (填“酸性”或“碱性”)氧化物。
(3)写出步骤(II)生成Mg(OH)2的离子方程式:_______ 。

(1)步骤(Ⅰ)中分离操作的名称是
(2)步骤(I)分离出的滤渣中主要含有
(3)写出步骤(II)生成Mg(OH)2的离子方程式:
更新时间:2022-12-23 23:45:57
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】某一元素具有如下性质,请你推测该元素在元素周期表中的位置。
(1)其最高价氧化物既可以溶于浓盐酸,也可以溶于NaOH溶液。
(2)其最高价氧化物对应的水化物既可以与酸反应,也可以与碱反应。
(3)1mol该元素最高价氧化物对应的水化物在与盐酸反应时,最多能消耗4molHCl。_____
(1)其最高价氧化物既可以溶于浓盐酸,也可以溶于NaOH溶液。
(2)其最高价氧化物对应的水化物既可以与酸反应,也可以与碱反应。
(3)1mol该元素最高价氧化物对应的水化物在与盐酸反应时,最多能消耗4molHCl。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D、E、F、G七种物质都是日常生活和生产中常见的物质,各物质间存在如下转化关系(反应的条件已省略)
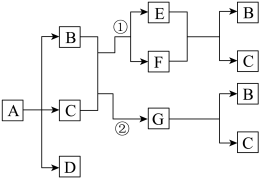
已知:B、C两种物质在不同情况下可分别发生①和②两个反应;A-G七种物质都是由非金属元素组成的,其中只有一种物质是盐,一种物质是单质;且B的相对分子质量大于C。
(1)请写出下列物质的化学式:A_______ ;G_______ ;
(2)请写出E+F→B+C的化学方程式:_______ 。

已知:B、C两种物质在不同情况下可分别发生①和②两个反应;A-G七种物质都是由非金属元素组成的,其中只有一种物质是盐,一种物质是单质;且B的相对分子质量大于C。
(1)请写出下列物质的化学式:A
(2)请写出E+F→B+C的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】I.某小河边有四座工厂:甲、乙、丙、丁(如图所示,河水自甲厂向下流)。已知,它们所排出的废液里分别含有 、
、 、
、 、HCl中的一种。某环保小组对河水监测时发现:
、HCl中的一种。某环保小组对河水监测时发现:
①甲处河水呈乳白色
②乙处河水呈红褐色浑浊状
③丙处河水由浑浊变澄清
④丁处河水产生气泡,河水仍澄清。

(1)各工厂排放的废液分别含有:甲厂:___________ 、乙厂:___________ 、丙厂:___________ 、丁厂:___________ (填化学式)。
(2)丙处河水变澄清的原因为___________ (用离子方程式进行说明)。
(3)丁处河水产生气泡的原因为___________ (用离子方程式进行说明)。
Ⅱ.磷元素的含氧酸有 (磷酸)、
(磷酸)、 (亚磷酸)、(次磷酸)等多种。其中次磷酸与过量NaOH溶液反应生成次磷酸钠(
(亚磷酸)、(次磷酸)等多种。其中次磷酸与过量NaOH溶液反应生成次磷酸钠( )的化学方程式为
)的化学方程式为 ,则
,则
(4) 中磷元素的化合价是
中磷元素的化合价是___________ ;
(5)上述反应___________ (填“属于”或“不属于”)氧化还原反应;
(6) 属于
属于___________ (填“正盐”、“酸式盐”或“碱式盐”)。
(7) (亚磷酸)具有较强的还原性,能被酸性
(亚磷酸)具有较强的还原性,能被酸性 溶液氧化为
溶液氧化为 (磷酸),其中涉及的离子方程式为:
(磷酸),其中涉及的离子方程式为:___________ 。
 、
、 、
、 、HCl中的一种。某环保小组对河水监测时发现:
、HCl中的一种。某环保小组对河水监测时发现:①甲处河水呈乳白色
②乙处河水呈红褐色浑浊状
③丙处河水由浑浊变澄清
④丁处河水产生气泡,河水仍澄清。

(1)各工厂排放的废液分别含有:甲厂:
(2)丙处河水变澄清的原因为
(3)丁处河水产生气泡的原因为
Ⅱ.磷元素的含氧酸有
 (磷酸)、
(磷酸)、 (亚磷酸)、(次磷酸)等多种。其中次磷酸与过量NaOH溶液反应生成次磷酸钠(
(亚磷酸)、(次磷酸)等多种。其中次磷酸与过量NaOH溶液反应生成次磷酸钠( )的化学方程式为
)的化学方程式为 ,则
,则(4)
 中磷元素的化合价是
中磷元素的化合价是(5)上述反应
(6)
 属于
属于(7)
 (亚磷酸)具有较强的还原性,能被酸性
(亚磷酸)具有较强的还原性,能被酸性 溶液氧化为
溶液氧化为 (磷酸),其中涉及的离子方程式为:
(磷酸),其中涉及的离子方程式为:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】金属镍广泛应用于制造记忆合金、储氢合金以及用作加氢反应的催化剂,是重要的战略物资,但资源匮乏。从某废镍渣(含 、NiO、FeO、
、NiO、FeO、 )中回收金属镍并转化为
)中回收金属镍并转化为 的流程如图所示:
的流程如图所示:
(1)“滤液A”中主要溶质的化学式为________ 。
(2)“焙烧”后金属元素以硫酸盐的形式存在,写出NiO与 反应的化学方程式:
反应的化学方程式:_______ 。
(3)使用95℃热水“溶解”后过滤,所得“滤渣”的主要成分的化学式是______ 。
(4)①“萃取”时发生反应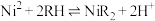 (RH为萃取剂),一定条件下,萃取平衡时,
(RH为萃取剂),一定条件下,萃取平衡时, ,则
,则 的苯取率为
的苯取率为_______ 。
②反萃取获得 ,溶液的实验操作是
,溶液的实验操作是______ 。
(5) 在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料
在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料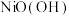 ,该反应的离子方程式为
,该反应的离子方程式为_________ 。
(6)镍能形成多种不同的化合物。图a是镍的一种配合物结构,图b是镍的一种氧化物的结构,下列说法不正确的是_________(填字母)。
 、NiO、FeO、
、NiO、FeO、 )中回收金属镍并转化为
)中回收金属镍并转化为 的流程如图所示:
的流程如图所示:
(1)“滤液A”中主要溶质的化学式为
(2)“焙烧”后金属元素以硫酸盐的形式存在,写出NiO与
 反应的化学方程式:
反应的化学方程式:(3)使用95℃热水“溶解”后过滤,所得“滤渣”的主要成分的化学式是
(4)①“萃取”时发生反应
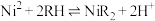 (RH为萃取剂),一定条件下,萃取平衡时,
(RH为萃取剂),一定条件下,萃取平衡时, ,则
,则 的苯取率为
的苯取率为②反萃取获得
 ,溶液的实验操作是
,溶液的实验操作是(5)
 在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料
在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料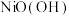 ,该反应的离子方程式为
,该反应的离子方程式为(6)镍能形成多种不同的化合物。图a是镍的一种配合物结构,图b是镍的一种氧化物的结构,下列说法不正确的是_________(填字母)。
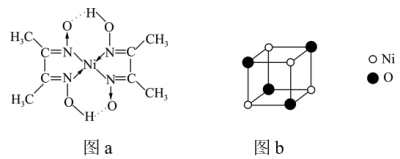
A.图a中,电负性 |
| B.图a分子中存在的化学键有共价键、配位键、氢键 |
| C.图b是氧化镍(NiO)的一个晶胞 |
D.氧化镍中 、 、 的配位数都是6 的配位数都是6 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
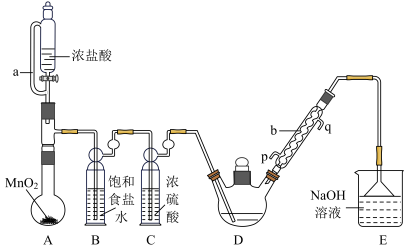
【推荐2】实验室制备三氯乙醛(CCl3CHO)的反应原理为C2H5OH+4Cl2→CCl3CHO+5HCl,可能发生的副反应是C2H5OH+HCl→C2H5Cl+H2O。某探究小组模拟制备三氯乙醛的实验装置如图所示(夹持、加热装置均略去)。
回答下列问题:
(1)用仪器a代替普通分液漏斗的目的是_______________ 。
(2)装置A中MnO2可以用KMnO4代替,反应可以在常温下进行,试写出反应的离子方程式________________ 。
(3)仪器b中冷凝水应从_______ (填“p”或“q”)口进。
(4)若撤去装置B,对实验的影响是______________ 。
(5)已知:CCl3CHO+OH-→CHCl3+HCOO-;HCOO-+I2=H++2I-+CO2↑;I2+2S2O =2I-+S4O
=2I-+S4O 。称取0.40 g产品,配成待测溶液,加入20.00 mL 0.100 mol/L碘标准溶液,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,并立即用0.020 mol/L的Na2S2O3溶液滴定至终点。重复上述操作3次,平均消耗Na2S2O3溶液20.00 mL。滴定时所用指示剂是
。称取0.40 g产品,配成待测溶液,加入20.00 mL 0.100 mol/L碘标准溶液,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,并立即用0.020 mol/L的Na2S2O3溶液滴定至终点。重复上述操作3次,平均消耗Na2S2O3溶液20.00 mL。滴定时所用指示剂是________ ,达到滴定终点时的现象是______________ ,测得该产品的纯度为_____ 。若滴定管用蒸馏水洗净后没有用Na2S2O3溶液润洗,则测定结果将_______ (填“偏大”、“偏小”或“不变”)。

回答下列问题:
(1)用仪器a代替普通分液漏斗的目的是
(2)装置A中MnO2可以用KMnO4代替,反应可以在常温下进行,试写出反应的离子方程式
(3)仪器b中冷凝水应从
(4)若撤去装置B,对实验的影响是
(5)已知:CCl3CHO+OH-→CHCl3+HCOO-;HCOO-+I2=H++2I-+CO2↑;I2+2S2O
 =2I-+S4O
=2I-+S4O 。称取0.40 g产品,配成待测溶液,加入20.00 mL 0.100 mol/L碘标准溶液,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,并立即用0.020 mol/L的Na2S2O3溶液滴定至终点。重复上述操作3次,平均消耗Na2S2O3溶液20.00 mL。滴定时所用指示剂是
。称取0.40 g产品,配成待测溶液,加入20.00 mL 0.100 mol/L碘标准溶液,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,并立即用0.020 mol/L的Na2S2O3溶液滴定至终点。重复上述操作3次,平均消耗Na2S2O3溶液20.00 mL。滴定时所用指示剂是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】某无色透明溶液中可能大量存在 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种离子。
中的几种离子。
(1)不做任何实验就可以肯定原溶液中不存在的离子是______ 。
(2)取少量原溶液,向其中加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,说明原溶液中肯定存在的离子是______ ,有关离子方程式为______
(3)向(2)的滤液中加入过量NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子是______ 。有关离子方程式为______ 。
(4)该溶液中可能存在的离子是______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种离子。
中的几种离子。(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,向其中加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,说明原溶液中肯定存在的离子是
(3)向(2)的滤液中加入过量NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子是
(4)该溶液中可能存在的离子是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】硼化铬(CrB)可用作耐磨、抗高温氧化涂层和核反应堆中的中子吸收涂层。以高铝铬铁矿(主要含 和
和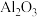 ,还含
,还含 、FeO、MgO、
、FeO、MgO、 )为原料制备硼化铬和铝的工艺流程如下。
)为原料制备硼化铬和铝的工艺流程如下。
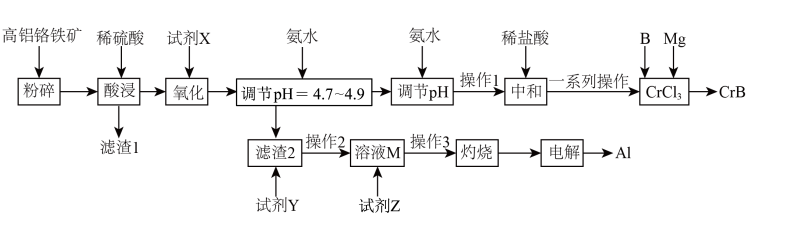
下表列出了相关金属离子生成氢氧化物沉淀的pH:
请回答下列问题:
(1)“氧化”的目的是将溶液中的 转化为
转化为 ,试剂X可选用
,试剂X可选用 或
或 ,若氧化等物质的量的
,若氧化等物质的量的 ,需要消耗
,需要消耗 和
和 的质量比为
的质量比为___________ 。
(2)试剂Y是___________ ,操作1的名称是___________ 。
(3)向M溶液中加入过量试剂Z发生反应的离子方程式为___________ 。
(4)第二次加氨水调节pH的范围是___________ ;加稀盐酸中和前,需要洗涤沉淀,证明沉淀洗涤干净的操作方法是___________ 。
(5)硼化铬是在650℃时由金属镁与硼、氯化铬的混合物制得的,写出该反应的化学方程式:___________ 。
 和
和 ,还含
,还含 、FeO、MgO、
、FeO、MgO、 )为原料制备硼化铬和铝的工艺流程如下。
)为原料制备硼化铬和铝的工艺流程如下。
下表列出了相关金属离子生成氢氧化物沉淀的pH:
| 金属离子 |  |  |  |  |  |
| 开始沉淀的pH | 2.3 | 10.4 | 4.9 | 7.5 | 3.4 |
| 沉淀完全的Ph | 4.1 | 12.4 | 6.8 | 9.7 | 4.7 |
(1)“氧化”的目的是将溶液中的
 转化为
转化为 ,试剂X可选用
,试剂X可选用 或
或 ,若氧化等物质的量的
,若氧化等物质的量的 ,需要消耗
,需要消耗 和
和 的质量比为
的质量比为(2)试剂Y是
(3)向M溶液中加入过量试剂Z发生反应的离子方程式为
(4)第二次加氨水调节pH的范围是
(5)硼化铬是在650℃时由金属镁与硼、氯化铬的混合物制得的,写出该反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】以红土镍矿(主要含有Fe2O3、FeO、NiO、SiO2等)为原料,获取净水剂黄钠铁矾[NaFe(SO4)2(OH)6]和纳米镍粉的部分工艺流程如下:
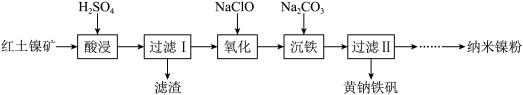
(1)“酸浸”过程,为提高铁和镍元素的浸出率,可采取的措施有___________ (写出两种)。
(2)“过滤Ⅰ”滤渣的主要成分是______ 。
(3)“氧化”过程欲使0.3molFe2+转变为Fe3+,则需氧化剂NaClO至少为________ mol。
(4)“沉铁”过程中加入碳酸钠调节浴液的pH至2,生成黄钠铁矾沉淀,写出该反应的化学方程式______ 。若碳酸钠过多会导致生成的沉淀由黄钠铁矾转变为_____ (填化学式)。
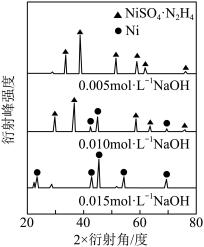
(5)向“过滤Ⅱ”所得滤液(富含Ni2+)中加入N2H4·H2O,在不同浓度的氢氧化钠溶液中反应,含镍产物的XRD图谱如下图所示(XRD图谱可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。欲制得高纯纳米镍粉最适宜的NaOH的物质的量浓度为_____ 。写出该条件下制备纳米镍粉同时生成N2的离子方程式_____ 。
(6)高铁酸盐也是一种优良的含铁净水剂,J.C.Poggendor早在1841年利用纯铁作电极插入浓的NaOH溶液电解制得Na2FeO4,阳极生成FeO42-的电极反应式为______ ;Deininger等对其进行改进,在阴、阳电极间设置阳离子交换膜,有效提高了产率,阳离子交换膜的作用是_______ 。

(1)“酸浸”过程,为提高铁和镍元素的浸出率,可采取的措施有
(2)“过滤Ⅰ”滤渣的主要成分是
(3)“氧化”过程欲使0.3molFe2+转变为Fe3+,则需氧化剂NaClO至少为
(4)“沉铁”过程中加入碳酸钠调节浴液的pH至2,生成黄钠铁矾沉淀,写出该反应的化学方程式
(5)向“过滤Ⅱ”所得滤液(富含Ni2+)中加入N2H4·H2O,在不同浓度的氢氧化钠溶液中反应,含镍产物的XRD图谱如下图所示(XRD图谱可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。欲制得高纯纳米镍粉最适宜的NaOH的物质的量浓度为

(6)高铁酸盐也是一种优良的含铁净水剂,J.C.Poggendor早在1841年利用纯铁作电极插入浓的NaOH溶液电解制得Na2FeO4,阳极生成FeO42-的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】从铝土矿(主要成分是 、含有
、含有 、
、 杂质)中提取
杂质)中提取 的两种工艺流程如图所示:
的两种工艺流程如图所示:

请回答下列问题:
(一)流程甲中:
(1)加入过量盐酸,滤液B的成分为___________ (写化学式)。
(2)写出固体A的一种用途___________ 。
(3)沉淀C的主要成分有___________ (写化学式)。
(二)流程乙中:
(4)加入过量烧碱时,滤液Y的成分___________ (写化学式)。
(5)滤液Y中通入的 ,能否用盐酸代替?
,能否用盐酸代替?___________ (填“能”或“不能”)
(6)将一定质量的铁铝合金投入 溶液中,恰好完全反应,生成
溶液中,恰好完全反应,生成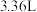 氢气(标准状况),请计算原
氢气(标准状况),请计算原 溶液的物质的量浓度(假设合金中其他成分不与
溶液的物质的量浓度(假设合金中其他成分不与 反应)
反应)___________ 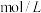 。
。
 、含有
、含有 、
、 杂质)中提取
杂质)中提取 的两种工艺流程如图所示:
的两种工艺流程如图所示:
请回答下列问题:
(一)流程甲中:
(1)加入过量盐酸,滤液B的成分为
(2)写出固体A的一种用途
(3)沉淀C的主要成分有
(二)流程乙中:
(4)加入过量烧碱时,滤液Y的成分
(5)滤液Y中通入的
 ,能否用盐酸代替?
,能否用盐酸代替?(6)将一定质量的铁铝合金投入
 溶液中,恰好完全反应,生成
溶液中,恰好完全反应,生成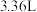 氢气(标准状况),请计算原
氢气(标准状况),请计算原 溶液的物质的量浓度(假设合金中其他成分不与
溶液的物质的量浓度(假设合金中其他成分不与 反应)
反应)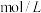 。
。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】石墨在材料领域有重要应用。某初级石墨中含SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质。设计的提纯和综合应用工艺如下:
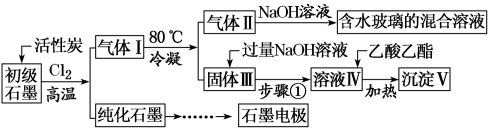
(注:SiCl4的沸点是57.6ºC,金属氯化物的沸点均高于150ºC)
(1)向反应器中通入Cl2前,需通一段时间的N2,主要目的是_______ 。
(2)高温反应后,石墨中的氧化物杂质均转变为相应的氯化物。气体I中的氯化物主要为_______ 。由气体II中某物质得到水玻璃的化学方程式为_______ 。
(3)步骤①为:搅拌、_______ 。
(4)由溶液IV生成沉淀V的总反应的离子方程式为_______ 。100 kg初级石墨最多可获得V的质量为_______ kg。

(注:SiCl4的沸点是57.6ºC,金属氯化物的沸点均高于150ºC)
(1)向反应器中通入Cl2前,需通一段时间的N2,主要目的是
(2)高温反应后,石墨中的氧化物杂质均转变为相应的氯化物。气体I中的氯化物主要为
(3)步骤①为:搅拌、
(4)由溶液IV生成沉淀V的总反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】三氧化钼(MoO3)和五氧化二钒(V2O5)是石油炼制中的重要催化剂,可利用炼油废催化剂(主要成分为V2O5、V2O4、MoO3,还有少量的Al2O3、Fe2O3、有机物等)来制备。工艺流程图如图:

已知:溶液中五价钒的存在形态如图所示:

(1)“焙烧”的目的是______ 。
(2)滤渣的主要成分是______ 。
(3)向滤液①中加H2O2的作用是______ (用离子方程式表示);有人提出用HNO3代替H2O2和盐酸,你认为是否合理,理由是______ 。
(4)除了调控滤液①pH为8外,还需要控制溶液中钒的总浓度不超过______ mol•L-1;通过计算说明此时铝元素有无完全沉淀______ 。(已知:Al(OH)3+OH- [Al(OH)4]- K=100.63;溶液中离子浓度小于10-5mol•L-1为沉淀完全)
[Al(OH)4]- K=100.63;溶液中离子浓度小于10-5mol•L-1为沉淀完全)
(5)NH4VO3受热分解的化学方程式为______ 。

已知:溶液中五价钒的存在形态如图所示:

(1)“焙烧”的目的是
(2)滤渣的主要成分是
(3)向滤液①中加H2O2的作用是
(4)除了调控滤液①pH为8外,还需要控制溶液中钒的总浓度不超过
 [Al(OH)4]- K=100.63;溶液中离子浓度小于10-5mol•L-1为沉淀完全)
[Al(OH)4]- K=100.63;溶液中离子浓度小于10-5mol•L-1为沉淀完全)(5)NH4VO3受热分解的化学方程式为
您最近一年使用:0次

 、
、


