铁是人类较早使用的金属之一,运用所学知识,回答下列问题。电子工业常用 30%的 FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中存在Fe3+的试剂是_______ (填化学式)溶液,证明 Fe3+存在的现象是_______ 。
(2)写出 FeCl3溶液与金属铜发生反应的离子方程式_______ 。
(3)某工程师为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤:
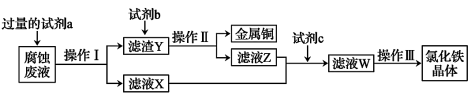
回答下列问题:
①试剂a是_______ ,操作I用到的玻璃仪器有烧杯、玻璃棒和_______ 。
②滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为_______ 。
③上述流程中操作III包括_______ 、过滤、洗涤。
(1)检验溶液中存在Fe3+的试剂是
(2)写出 FeCl3溶液与金属铜发生反应的离子方程式
(3)某工程师为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤:

回答下列问题:
①试剂a是
②滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为
③上述流程中操作III包括
更新时间:2022-12-13 09:42:42
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】Ⅰ.某工厂的酸性废水中主要含有 、
、 等离子,为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾 (
等离子,为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾 ( )。
)。
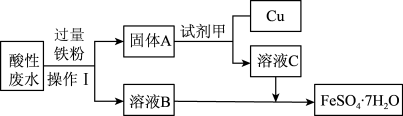
(1)操作Ⅰ是_______ ;试剂甲是_______ (填化学式)。
(2)获得的 需密闭保存,原因是
需密闭保存,原因是_______ 。
(3)绿矾可消除某种酸性工业废水中+6价铬( )的污染,使之转化为毒性较小的
)的污染,使之转化为毒性较小的 ,该反应的离子方程式是
,该反应的离子方程式是_______ 。
(4)黄铜是铜锌合金,是用来制造铜钱的原料,能鉴别黄铜中有金属锌的试剂是_______ 。
Ⅱ.某小组为探究 、
、 、
、 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:
【查阅资料】稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。氧化性强弱探究:
【分析与解释】
(5)实验Ⅰ中a试管中反应的离子方程式是_______ 。
(6)①甲同学认为:实验Ⅱ观察到_______ 现象,得出氧化性 。
。
②乙同学对上述实验进行反思,认为实验Ⅱ不能充分证明氧化性 ;他补做了实验Ⅲ。补做实验Ⅲ的目的是
;他补做了实验Ⅲ。补做实验Ⅲ的目的是_______ 。
 、
、 等离子,为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾 (
等离子,为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾 ( )。
)。
(1)操作Ⅰ是
(2)获得的
 需密闭保存,原因是
需密闭保存,原因是(3)绿矾可消除某种酸性工业废水中+6价铬(
 )的污染,使之转化为毒性较小的
)的污染,使之转化为毒性较小的 ,该反应的离子方程式是
,该反应的离子方程式是(4)黄铜是铜锌合金,是用来制造铜钱的原料,能鉴别黄铜中有金属锌的试剂是
Ⅱ.某小组为探究
 、
、 、
、 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:【查阅资料】稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。氧化性强弱探究:
| 实验Ⅰ | 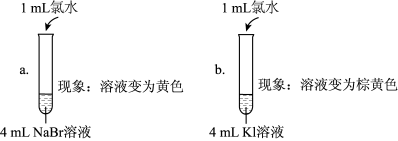 |
| 实验Ⅱ | 取a中的黄色溶液少许,加入KI溶液,再加入淀粉溶液 |
| 实验Ⅲ | 另取a中的黄色溶液少许,先加入足量的NaBr固体,充分振荡,然后加入KI溶液和淀粉溶液 |
(5)实验Ⅰ中a试管中反应的离子方程式是
(6)①甲同学认为:实验Ⅱ观察到
 。
。②乙同学对上述实验进行反思,认为实验Ⅱ不能充分证明氧化性
 ;他补做了实验Ⅲ。补做实验Ⅲ的目的是
;他补做了实验Ⅲ。补做实验Ⅲ的目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】《我在故宫修文物》展示了专家精湛的技艺和对传统文化的热爱与坚守,也令人体会到化学方法在文物保护中的巨大作用。某博物馆修复出土铁器的过程如下:
(1)检测锈蚀产物
铁器在具有O2、____ 等环境中容易被腐蚀。
(2)分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
①Fe转化为Fe2+。
②FeO(OH)和Fe2+反应形成致密的Fe3O4保护层,Fe2+的作用是____ (填字母)。
a.氧化剂 b.还原剂 c.既不是氧化剂也不是还原剂
(3)研究发现,Cl-对铁的腐蚀会造成严重影响。化学修复:脱氯、还原,形成Fe3O4保护层,方法如下:
将铁器浸没在盛有0.5mol·L-1Na2SO3、0.5mol·L-1NaOH溶液的容器中,缓慢加热至60~90℃。一段时间后,取出器物,用NaOH溶液洗涤至无Cl-。
①检测洗涤液中Cl-的方法是:____ 。
②脱氯反应:FeOCl+OH-===FeO(OH)+Cl-。离子反应的本质是离子浓度的减小,比较FeOCl与FeO(OH)溶解度的大小:____ 。
③Na2SO3还原FeO(OH)形成Fe3O4的离子方程式是:____ 。
(1)检测锈蚀产物
| 主要成分的化学式 | |||
| Fe3O4 | Fe2O3·H2O | FeO(OH) | FeOCl |
(2)分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
①Fe转化为Fe2+。
②FeO(OH)和Fe2+反应形成致密的Fe3O4保护层,Fe2+的作用是
a.氧化剂 b.还原剂 c.既不是氧化剂也不是还原剂
(3)研究发现,Cl-对铁的腐蚀会造成严重影响。化学修复:脱氯、还原,形成Fe3O4保护层,方法如下:
将铁器浸没在盛有0.5mol·L-1Na2SO3、0.5mol·L-1NaOH溶液的容器中,缓慢加热至60~90℃。一段时间后,取出器物,用NaOH溶液洗涤至无Cl-。
①检测洗涤液中Cl-的方法是:
②脱氯反应:FeOCl+OH-===FeO(OH)+Cl-。离子反应的本质是离子浓度的减小,比较FeOCl与FeO(OH)溶解度的大小:
③Na2SO3还原FeO(OH)形成Fe3O4的离子方程式是:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】五氧化二钽(Ta2O5)主要用作钽酸锂单晶和制造高折射低色散特种光学玻璃等。一种以含钽废料(主要成分为NaTaO3、SiO2以及少量的FeO、Fe2O3、Al2O3等)为原料制备Ta2O5的工艺流程如图所示:
(1)“酸溶”时,Fe2O3发生反应的基本反应类型为_______ ,滤渣的主要成分是 _______ (填化学式)。
(2)“氧化”时,发生反应的离子方程式为_______ 。
(3)常温下,“调pH”时,若过滤出沉淀后溶液的pH=5,Al3+是否沉淀完全?_______ (请写出简要步骤)。已知:常温下,Ksp[Al(OH)3]=1.9×10﹣33,溶液中离子浓度小于或等于1×10﹣5时可视为沉淀完全。
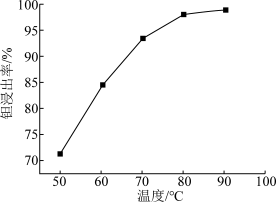
(4)“浸钽”时,加入4g/L的HF溶液,浸出时间为4h,钽的浸出率随温度的变化如图所示,该HF溶液的物质的量浓度为_______ mol/L,浸出的最佳温度为 _______ ℃;“调pH”后,溶液中溶质主要为NaTaO3,写出“浸钽”时生成H2TaF7的离子方程式:_______ 。_______ 。

(1)“酸溶”时,Fe2O3发生反应的基本反应类型为
(2)“氧化”时,发生反应的离子方程式为
(3)常温下,“调pH”时,若过滤出沉淀后溶液的pH=5,Al3+是否沉淀完全?
(4)“浸钽”时,加入4g/L的HF溶液,浸出时间为4h,钽的浸出率随温度的变化如图所示,该HF溶液的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】化学实验室产生的废液中含有大量会污染环境的物质,为了保护环境,这些废液必须经处理后才能排放。某化学实验室产生的废液中含有两种金属离子:Fe3+、Cu2+,化学小组设计了如图所示的方案对废液进行处理,以回收金属,保护环境。
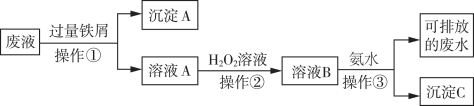
(1)操作①的名称是___________ 。加入铁屑先发生的离子反应为:________
(2)沉淀A中含有的金属单质有___________ 。
(3)操作②中观察到的实验现象是___________ 。
(4)检验溶液B中含有的金属阳离子常用的试剂是____________ 。
(5)操作③中发生反应的离子方程式为__________ 。

(1)操作①的名称是
(2)沉淀A中含有的金属单质有
(3)操作②中观察到的实验现象是
(4)检验溶液B中含有的金属阳离子常用的试剂是
(5)操作③中发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知A是一种红棕色金属氧化物,B、D是金属单质,C是两性金属氧化物,J是一种难溶于水的白色化合物,受热后容易发生分解。
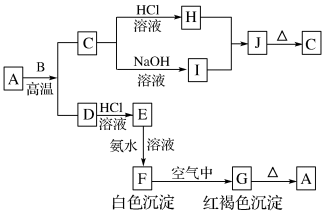
已知:
(1)写出下列物质的化学式:C___________ 、E___________ 、G___________ 。
(2)按要求写方程式:
①F→G的化学方程式:___________ ;
②E→F的离子方程式:___________ ;
③C→I的离子方程式:___________ ;
④B与 溶液反应的离子方程式:
溶液反应的离子方程式:___________ 。
⑤检验E中阳离子的具体操作为___________ 。
⑥检验H中阴离子的具体操作为___________ 。

已知:

(1)写出下列物质的化学式:C
(2)按要求写方程式:
①F→G的化学方程式:
②E→F的离子方程式:
③C→I的离子方程式:
④B与
 溶液反应的离子方程式:
溶液反应的离子方程式:⑤检验E中阳离子的具体操作为
⑥检验H中阴离子的具体操作为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C、F是无色无味的气体,M为红褐色。请回答下列问题:
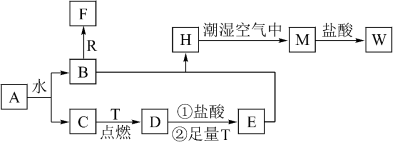
(1)A的电子式是_______ ,R元素在元素周期表中位置为_______ 。
(2)A与水反应的离子方程式为_______ 。
(3)检验W溶液中金属阳离子的操作方法是_______ 。
(4)反应②可能发生反应的离子方程式为_______ 。
(5)H生成M的反应中氧化剂是_______ ,反应的化学方程式为_______ 。

(1)A的电子式是
(2)A与水反应的离子方程式为
(3)检验W溶液中金属阳离子的操作方法是
(4)反应②可能发生反应的离子方程式为
(5)H生成M的反应中氧化剂是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某实验小组对FeCl3溶液与Na2SO3溶液的反应进行探究。
已知:铁氰化钾的化学式为K3[Fe(CN)6],用于检验Fe2+,遇Fe2+离子产生蓝色沉淀
【实验1】
(1)配制FeCl3溶液时,先将FeCl3溶于浓盐酸,再稀释至指定浓度。从化学平衡角度说明浓盐酸的作用:__________ 。
【探究现象i产生的原因】
(2)甲同学认为发生反应:2Fe3++3 +6H2O
+6H2O 2Fe(OH)3(胶体)+3H2SO3;他取少量红褐色溶液于试管中,继续滴加1mol/LNa2SO3溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是
2Fe(OH)3(胶体)+3H2SO3;他取少量红褐色溶液于试管中,继续滴加1mol/LNa2SO3溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是_______ (填化学式)。
(3)乙同学认为还发生了氧化还原反应。他取少许红褐色溶液于试管中,加入______ ,有白色沉淀产生,证明产物中含有 。
。
丙同学认为乙同学的实验不严谨,因为在上述过程中 可能被其它物质氧化。为了进一步确认
可能被其它物质氧化。为了进一步确认 被氧化的原因,丙同学设计了实验2。
被氧化的原因,丙同学设计了实验2。
【实验2】用如图装置(a、b均为石墨电极)进行实验。闭合开关后灵敏电流计指针偏转。
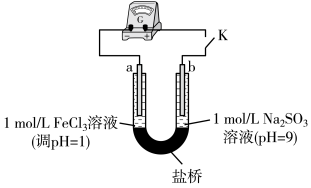
(4)实验2中正极的电极反应式为______ 。丙同学又用铁氰化钾溶液检验正极的产物,观察到有蓝色沉淀产生。他得出的结论是___________ 。
【解释现象ii产生的原因】
(5)综合上述结果,请从平衡移动角度解释,现象ii产生的原因为___________________ 。
已知:铁氰化钾的化学式为K3[Fe(CN)6],用于检验Fe2+,遇Fe2+离子产生蓝色沉淀
【实验1】
| 装置 | 实验现象 |
 | 现象i:一开始溶液颜色加深,由棕黄色变为红褐色。 现象ii:一段时间后溶液颜色变浅,变为浅黄色。 |
【探究现象i产生的原因】
(2)甲同学认为发生反应:2Fe3++3
 +6H2O
+6H2O 2Fe(OH)3(胶体)+3H2SO3;他取少量红褐色溶液于试管中,继续滴加1mol/LNa2SO3溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是
2Fe(OH)3(胶体)+3H2SO3;他取少量红褐色溶液于试管中,继续滴加1mol/LNa2SO3溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是(3)乙同学认为还发生了氧化还原反应。他取少许红褐色溶液于试管中,加入
 。
。丙同学认为乙同学的实验不严谨,因为在上述过程中
 可能被其它物质氧化。为了进一步确认
可能被其它物质氧化。为了进一步确认 被氧化的原因,丙同学设计了实验2。
被氧化的原因,丙同学设计了实验2。【实验2】用如图装置(a、b均为石墨电极)进行实验。闭合开关后灵敏电流计指针偏转。

(4)实验2中正极的电极反应式为
【解释现象ii产生的原因】
(5)综合上述结果,请从平衡移动角度解释,现象ii产生的原因为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】兴趣小组探究SO2气体还原Fe3+、I2,它们使用的药品和装置如图所示:
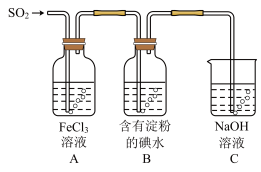
(1)SO2气体和Fe3+反应的氧化产物、还原产物分别是________ 、________
(2)下列实验方案适用于在实验室制取所需SO2的是________ 。
A.Na2SO3溶液与HNO3 B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧 D.铜与浓H2SO4共热
(3)装置C的作用是__________________________________________________ 。
(4)装置B中反应的离子方程式_________________________________________________ 。
(5)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入酸性KMnO4溶液,紫红色褪去。
方案②:往第二份试液中加入NaOH溶液,产生白色沉淀,并迅速转为灰绿,最后呈红褐色。
方案③:往第三份试液中加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是方案_____ ,原因是_______________________________

(1)SO2气体和Fe3+反应的氧化产物、还原产物分别是
(2)下列实验方案适用于在实验室制取所需SO2的是
A.Na2SO3溶液与HNO3 B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧 D.铜与浓H2SO4共热
(3)装置C的作用是
(4)装置B中反应的离子方程式
(5)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入酸性KMnO4溶液,紫红色褪去。
方案②:往第二份试液中加入NaOH溶液,产生白色沉淀,并迅速转为灰绿,最后呈红褐色。
方案③:往第三份试液中加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是方案
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知A为常见金属,有以下物质相互转化:
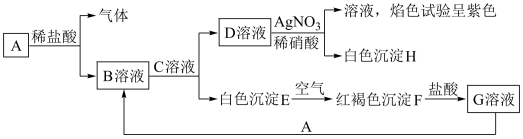
试回答下列问题:
(1)写出C的化学式:___________ 。
(2)用AgNO3溶液检验B溶液中的阴离子时,加HNO3的原因是:___________ 。
(3)写出由E转变成F的化学方程式:___________ ,E转变成F发生颜色变化,其过渡颜色为___________ 色。
(4)做D溶液的焰色试验时除了铂丝、酒精灯、烧杯,还需要的实验仪器是___________ 。
(5)写出用稀KMnO4酸性溶液鉴别B溶液的现象是:___________ 。
(6)向G溶液中加入A的有关反应的离子方程式:___________ 。

试回答下列问题:
(1)写出C的化学式:
(2)用AgNO3溶液检验B溶液中的阴离子时,加HNO3的原因是:
(3)写出由E转变成F的化学方程式:
(4)做D溶液的焰色试验时除了铂丝、酒精灯、烧杯,还需要的实验仪器是
(5)写出用稀KMnO4酸性溶液鉴别B溶液的现象是:
(6)向G溶液中加入A的有关反应的离子方程式:
您最近一年使用:0次



