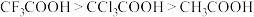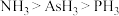下列说法正确的是
①常温下白磷可自燃而氮气需在放电时才与氧气反应,则非金属性:P>N
②第IA族元素铯的两种同位素137Cs比133Cs多4个质子
③因为氧化性:HClO>稀H2SO4,所以非金属性:Cl>S
④离子化合物中既可以含有极性共价键又可以含有非极性共价键
⑤C、P、S、Cl的最高价氧化物对应水化物的酸性逐渐增强
⑥从上到下,卤族元素的非金属性逐渐减弱,所以酸性HCl>HI
⑦离子半径:K+>Cl->S2-
①常温下白磷可自燃而氮气需在放电时才与氧气反应,则非金属性:P>N
②第IA族元素铯的两种同位素137Cs比133Cs多4个质子
③因为氧化性:HClO>稀H2SO4,所以非金属性:Cl>S
④离子化合物中既可以含有极性共价键又可以含有非极性共价键
⑤C、P、S、Cl的最高价氧化物对应水化物的酸性逐渐增强
⑥从上到下,卤族元素的非金属性逐渐减弱,所以酸性HCl>HI
⑦离子半径:K+>Cl->S2-
| A.②③④⑤⑥⑦ | B.④⑤ | C.②③④⑦ | D.④⑤⑥ |
更新时间:2022-12-13 21:44:06
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】某主族元素R原子的质量数为32,已知R离子含有16个中子和18个电子,下列关于R元素的叙述错误的是
| A.R元素属于ⅣA族 |
| B.R元素在周期表里处于第3周期 |
| C.R元素最高价氧化物对应水化物的分子式为H2RO4 |
| D.R元素气态氢化物的分子式为H2R |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列结论错误的是。
①粒子半径:K+>Al3+>S2->Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I-
④第一电离能:Cl>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO
⑥电负性:O>N>P>Si
①粒子半径:K+>Al3+>S2->Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I-
④第一电离能:Cl>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO
⑥电负性:O>N>P>Si
| A.① | B.①③⑤ | C.②④⑤⑥ | D.①③ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、V、W五种短周期元素,原子序数依次增大,其中Z的原子半径最大,Z的单质在W的单质中燃烧产生黄色火焰;五种元素可以组成一种有机盐(如图所示)。下列说法正确的是
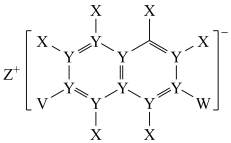

| A.X与W形成的分子中各原子最外层均满足8电子稳定结构 |
| B.简单离子半径的大小关系为:V>W>Z |
| C.热稳定性:X与V组成的二元化合物>X与W组成的二元化合物 |
| D.V与W所形成的含氧酸均为强酸 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】欲进行下列实验,其方案设计合理的是
A.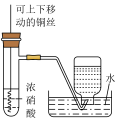 试剂NO2 试剂NO2 |
B. 证明碳酸酸性强于硅酸 证明碳酸酸性强于硅酸 |
C. 比较N、C、Si非金属性的强弱 比较N、C、Si非金属性的强弱 |
D. 比较NaHCO3和Na2CO3的溶解度 比较NaHCO3和Na2CO3的溶解度 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、W是原子序数依次增大的短周期元素,X与W同主族,且W原子核内质子数是X原子核外电子数的两倍,Y是同周期元素中原子半径最大的,Y、Z、W的最高价氧化物对应的水化物可两两反应生成盐和水,甲是Z、W两种元素形成的化合物。下列说法错误的是
| A.X单质的氧化性强于W单质 |
| B.Z的合金在生产生活中用途广泛 |
| C.可以在水溶液中利用复分解反应制备甲 |
| D.离子半径:W>X>Y>Z |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】有A、B、C、D、E五种短周期元素,原子序数依次增大,其中A与C、B与D分别为同族元素,A与B可形成原子数之比为1∶1的共价化合物X,B、C、D、E四种元素可以组成如图结构的离子化合物Y。下列说法不正确的是
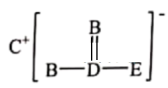
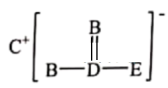
| A.原子半径:C>D>E |
| B.D与E的最高价氧化物对应水化物均为强酸 |
| C.元素A与其他四种元素均可组成共价化合物 |
D.化合物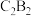 可以与 可以与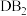 发生氧化还原反应 发生氧化还原反应 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列物质中,既含有离子键又含有共价键的是:
| A.HCl | B.NaOH | C.CaCl2 | D.CO2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列有关化学用语的表示正确的是
A.NaCl的电离方程式为: |
B. 电子式为: 电子式为: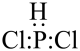 |
C.Li在空气中燃烧产物的化学式为: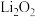 |
D. 氧化 氧化 生成单质硫: 生成单质硫: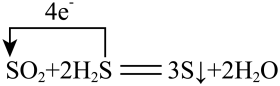 |
您最近半年使用:0次