现有下列5种物质:① SO2、② NO2、③ HCl、④ HClO、⑤Al2O3。有颜色的气体是___________ ,遇氨气产生白烟的气体是___________ ,因见光而分解的是___________ ,能使品红溶液褪色且加热后又恢复红色的是___________ ,属于两性氧化物的是__________ 。
更新时间:2022-12-18 17:04:26
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某化学兴趣小组在探究次氯酸钠溶液的性质时发现:往过量 FeSO4溶液中滴入几滴NaClO溶液,并加入适量硫酸,溶液立即变黄。请你协助他们完成该反应还原产物的部分探究过程。
(1)溶液变黄,说明反应生成了_________ (离子符号),可以通过加入____________ (试剂名称)进行检验。
(2)甲同学推测该反应的还原产物为Cl2;乙同学推测该反应的还原产物为________ (填微粒)。
(3)你认为甲同学的推测是否正确?____________ (填“正确”或“不正确”).
(4)假设乙同学的推测是正确。写出过量 FeSO4溶液中,滴入几滴NaClO溶液,并加入适量硫酸的离子方程式:___________________________________________________ 。
(1)溶液变黄,说明反应生成了
(2)甲同学推测该反应的还原产物为Cl2;乙同学推测该反应的还原产物为
(3)你认为甲同学的推测是否正确?
(4)假设乙同学的推测是正确。写出
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】为抗击新冠肺炎经常对环境进行消毒,常用药物如:高锰酸钾、漂白粉、氯气等。
(1)新制氯水中含有多种微粒,将紫色石蕊试液滴入氯水中,溶液显红色起作用的微粒是___________ (填化学符号,下同);过一会儿,溶液颜色逐渐褪去,起作用的微粒是___________ 。
(2)工业上利用氯气和石灰乳反应制取漂白粉,漂白粉的有效成分为___________ (填化学式)。向漂白粉清液中滴加碳酸钠溶液,有白色沉淀生成,写出发生反应的离子方程式___________ 。
(3)已知高锰酸钾与浓盐酸混合能产生氯气,化学反应方程式为: (浓)
(浓)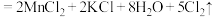 ,回答下列问题:
,回答下列问题:
①用双线桥标出电子转移的方向和数目___________
 (浓)
(浓)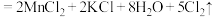
(在线桥上标出化合价升或降、得或失电子数以及被氧化或被还原)
②结合所学知识及本题信息比较氧化性强弱:
___________ 
___________  (填“>”,“<”或“=”)。
(填“>”,“<”或“=”)。
③反应中氯化氢表现出的性质是___________ 。(填写字母)
a.还原性 b.酸性 c.氧化性
④若生成标准状况下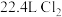 ,则转移电子总数是
,则转移电子总数是___________ 。
(1)新制氯水中含有多种微粒,将紫色石蕊试液滴入氯水中,溶液显红色起作用的微粒是
(2)工业上利用氯气和石灰乳反应制取漂白粉,漂白粉的有效成分为
(3)已知高锰酸钾与浓盐酸混合能产生氯气,化学反应方程式为:
 (浓)
(浓)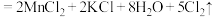 ,回答下列问题:
,回答下列问题:①用双线桥标出电子转移的方向和数目
 (浓)
(浓)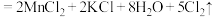
(在线桥上标出化合价升或降、得或失电子数以及被氧化或被还原)
②结合所学知识及本题信息比较氧化性强弱:


 (填“>”,“<”或“=”)。
(填“>”,“<”或“=”)。③反应中氯化氢表现出的性质是
a.还原性 b.酸性 c.氧化性
④若生成标准状况下
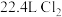 ,则转移电子总数是
,则转移电子总数是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求回答下列问题.
(1)请写出 在水溶液中的电离方程式
在水溶液中的电离方程式_____________________________________
(2)写出次氯酸见光分解的化学方程式_____________________________________
(3)纯净的 在氯气中安静地燃烧,发出
在氯气中安静地燃烧,发出_____________ 火焰
(4)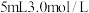 的
的 溶液加水稀释至
溶液加水稀释至 ,此时溶液中
,此时溶液中 的物质的量浓度为
的物质的量浓度为_____________
(5)若 某气体中含有的分子数为b个,则
某气体中含有的分子数为b个,则 该气体在标准状况下的体积为
该气体在标准状况下的体积为_____________________ (设 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
(6)高铁酸钾 是一种新型的净水剂,可以通过下述反应制取:
是一种新型的净水剂,可以通过下述反应制取:
①该反应中氧化剂是_____________ (用化学式表示),被氧化的元素是______________________
②用“单线桥”在方程式中标出电子转移的情况:_________________________________
(1)请写出
 在水溶液中的电离方程式
在水溶液中的电离方程式(2)写出次氯酸见光分解的化学方程式
(3)纯净的
 在氯气中安静地燃烧,发出
在氯气中安静地燃烧,发出(4)
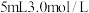 的
的 溶液加水稀释至
溶液加水稀释至 ,此时溶液中
,此时溶液中 的物质的量浓度为
的物质的量浓度为(5)若
 某气体中含有的分子数为b个,则
某气体中含有的分子数为b个,则 该气体在标准状况下的体积为
该气体在标准状况下的体积为 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)(6)高铁酸钾
 是一种新型的净水剂,可以通过下述反应制取:
是一种新型的净水剂,可以通过下述反应制取:
①该反应中氧化剂是
②用“单线桥”在方程式中标出电子转移的情况:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点。
(1)烟气脱硫、脱硝的环境意义是______________________ ;
(2)一种选择性催化脱硝(NO2)的原理为:6NO2+8NH3 7N2+12H2O
7N2+12H2O
① 上述反应中被还原的元素是_________ (填元素符号),反应中每转移3mol电子,生成标准状况下N2的体积为____________ ;
② 超音速飞机排放的尾气是平流层中NOx的主要来源.它们破坏臭氧层的主要机理为:
Ⅰ 、O3 O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2
O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2
上述反应中NOx所起的作用是_____________ ;
(3)下表列出了2种燃煤烟气脱硫方法的原理。
①方法Ⅰ中用氨水吸收燃煤烟气中的SO2转化为NH4HSO3,是利用了SO2的___________ 性质(选填字母编号)。
A.漂白性 B.氧化性 C.还原性 D.酸性氧化物
C.还原性 D.酸性氧化物
②方法Ⅰ中氨水吸收燃煤烟气中SO2的化学反应为:2NH3+SO2+H2O=(NH4)2SO3
(NH4)2SO3+SO2+H2O=2NH4HSO3,能提高燃煤烟气中SO2去除率的措施有______ (填字母).
A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D.通入空气使HSO3-转化为SO42-
③采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的CO2,原因是_________________ (用离子方程式表示)。
(1)烟气脱硫、脱硝的环境意义是
(2)一种选择性催化脱硝(NO2)的原理为:6NO2+8NH3
 7N2+12H2O
7N2+12H2O① 上述反应中被还原的元素是
② 超音速飞机排放的尾气是平流层中NOx的主要来源.它们破坏臭氧层的主要机理为:
Ⅰ 、O3
 O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2
O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2上述反应中NOx所起的作用是
(3)下表列出了2种燃煤烟气脱硫方法的原理。
方法Ⅰ | 用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4 |
方法Ⅱ | 用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫 |
①方法Ⅰ中用氨水吸收燃煤烟气中的SO2转化为NH4HSO3,是利用了SO2的
A.漂白性 B.氧化性
 C.还原性 D.酸性氧化物
C.还原性 D.酸性氧化物②方法Ⅰ中氨水吸收燃煤烟气中SO2的化学反应为:2NH3+SO2+H2O=(NH4)2SO3
(NH4)2SO3+SO2+H2O=2NH4HSO3,能提高燃煤烟气中SO2去除率的措施有
A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D.通入空气使HSO3-转化为SO42-
③采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的CO2,原因是
您最近一年使用:0次
【推荐2】如何除去下列气体中的杂质气体?写出所需除杂试剂及发生反应的化学方程式(括号内为杂质)。
(1)SO2(HCl):试剂_____________ ;_____________________________________ ;
(2)CO2(HCl):试剂_____________ ;_____________________________________ ;
(1)SO2(HCl):试剂
(2)CO2(HCl):试剂
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:

(1)反应Ⅰ的化学方程式是_______________________ 。
反应Ⅲ的化学方程式是____________________ 。
(2)SO2的排放是形成酸雨的原因之一,我们把pH小于_____ 的雨称为酸雨。
(3)反应Ⅰ得到的产物用I2进行分离。该产物的溶液在过量I2的存在下会分成两层,分别是含低浓度I2的H2SO4层和高浓度的I2的HI层。
①根据上述事实,下列说法正确的是____________ (选填序号)。
a.两层溶液的密度存在差异
b.加I2前,H2SO4溶液和HI溶液不互溶
c.I2在HI溶液中比在H2SO4溶液中易溶
②分离两层液体用到的玻璃仪器主要有_____________________ 。
③辨别两层溶液的方法是____________ 。
④经检测,H2SO4层中c(H+):c(SO42-)=2.06:1。其比值大于2的原因是__________________________ 。
(4)反应Ⅱ:2H2SO4(l)→2SO2(g)+O2(g)+2H2O(g),已知生成9 g水蒸气吸收137.5 KJ的热量,写出该反应的热化学方程式_______________________ 。

(1)反应Ⅰ的化学方程式是
反应Ⅲ的化学方程式是
(2)SO2的排放是形成酸雨的原因之一,我们把pH小于
(3)反应Ⅰ得到的产物用I2进行分离。该产物的溶液在过量I2的存在下会分成两层,分别是含低浓度I2的H2SO4层和高浓度的I2的HI层。
①根据上述事实,下列说法正确的是
a.两层溶液的密度存在差异
b.加I2前,H2SO4溶液和HI溶液不互溶
c.I2在HI溶液中比在H2SO4溶液中易溶
②分离两层液体用到的玻璃仪器主要有
③辨别两层溶液的方法是
④经检测,H2SO4层中c(H+):c(SO42-)=2.06:1。其比值大于2的原因是
(4)反应Ⅱ:2H2SO4(l)→2SO2(g)+O2(g)+2H2O(g),已知生成9 g水蒸气吸收137.5 KJ的热量,写出该反应的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】SO2、SO3均为硫的氧化物,请回答下列问题。
(1)关于SO2和SO3,下列说法正确的是_______ (填字母)。
a.都是酸性氧化物
b.都有氧化性
c.硫在纯氧中燃烧生成SO3
d.都能使品红溶液褪色
(2)工业尾气中排放的SO2会导致酸雨,请从化合价和物质类别的角度,各列举一种试剂处理尾气中的SO2:_______ 、_______ 。
(3)将SO2通入FeCl3溶液中,下列实验事实能够证实SO2具有还原性的是_______ (填字母)。
a.反应后溶液由黄色变为浅绿色
b.取反应后的溶液少许,加入BaCl2溶液,产生白色沉淀
c.取反应后的溶液少许,加入Ba(OH)2溶液,产生沉淀,加入足量盐酸后,沉淀部分溶解
(1)关于SO2和SO3,下列说法正确的是
a.都是酸性氧化物
b.都有氧化性
c.硫在纯氧中燃烧生成SO3
d.都能使品红溶液褪色
(2)工业尾气中排放的SO2会导致酸雨,请从化合价和物质类别的角度,各列举一种试剂处理尾气中的SO2:
(3)将SO2通入FeCl3溶液中,下列实验事实能够证实SO2具有还原性的是
a.反应后溶液由黄色变为浅绿色
b.取反应后的溶液少许,加入BaCl2溶液,产生白色沉淀
c.取反应后的溶液少许,加入Ba(OH)2溶液,产生沉淀,加入足量盐酸后,沉淀部分溶解
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氨基磺酸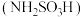 可用于合成除草剂、防火剂、甜味剂、防腐剂、金属清洗剂等,是一种常见的化工原料。
可用于合成除草剂、防火剂、甜味剂、防腐剂、金属清洗剂等,是一种常见的化工原料。
(1)由尿素 与发烟硫酸(用
与发烟硫酸(用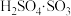 表示,)在40~70℃下进行磺化反应生成氨基磺酸,则该反应的化学方程式为
表示,)在40~70℃下进行磺化反应生成氨基磺酸,则该反应的化学方程式为_______ 。
(2)氨基磺酸在高温时的分解反应为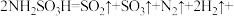
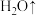 。
。
①检验该混合产物中含有 的试剂是
的试剂是_______ (填序号)。
A.品红溶液 B. 溶液 C.溴水 D.碳酸氢钠溶液
溶液 C.溴水 D.碳酸氢钠溶液
②高温时,该反应中转移2mol电子时,生成气体的总物质的量是_______ mol。
(3)硝酸与氨基磺酸能反应生成硫酸、水和一种氮氧化合物。
①0.5mol该氮氧化合物中氮元素的质量比氧元素的多6g,则该氮氧化合物的化学式为_______ 。
②下列有关浓硫酸和浓硝酸的说法正确的是_______ (填序号)。
A.浓硫酸可用于干燥 、
、 、HI
、HI
B.常温下,浓硫酸和浓硝酸均能将铝“钝化”,均体现其强氧化性
C.浓硫酸和浓硝酸分别长期露置在空气中,两者浓度变小的原理不同
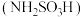 可用于合成除草剂、防火剂、甜味剂、防腐剂、金属清洗剂等,是一种常见的化工原料。
可用于合成除草剂、防火剂、甜味剂、防腐剂、金属清洗剂等,是一种常见的化工原料。(1)由尿素
 与发烟硫酸(用
与发烟硫酸(用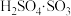 表示,)在40~70℃下进行磺化反应生成氨基磺酸,则该反应的化学方程式为
表示,)在40~70℃下进行磺化反应生成氨基磺酸,则该反应的化学方程式为(2)氨基磺酸在高温时的分解反应为
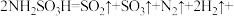
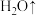 。
。①检验该混合产物中含有
 的试剂是
的试剂是A.品红溶液 B.
 溶液 C.溴水 D.碳酸氢钠溶液
溶液 C.溴水 D.碳酸氢钠溶液②高温时,该反应中转移2mol电子时,生成气体的总物质的量是
(3)硝酸与氨基磺酸能反应生成硫酸、水和一种氮氧化合物。
①0.5mol该氮氧化合物中氮元素的质量比氧元素的多6g,则该氮氧化合物的化学式为
②下列有关浓硫酸和浓硝酸的说法正确的是
A.浓硫酸可用于干燥
 、
、 、HI
、HIB.常温下,浓硫酸和浓硝酸均能将铝“钝化”,均体现其强氧化性
C.浓硫酸和浓硝酸分别长期露置在空气中,两者浓度变小的原理不同
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据相应信息回答有关问题。
I.物质结构和规律推断
如图为周期表中短周期的一部分,已知A是地壳中含量最多的元素。
(1)比较A、C的原子半径大小_______ (用原子符号表示)。
(2)比较C、D的简单氢化物的稳定性_______ (用化学式表示)。
II.实验操作和现象分析
(3)配制100ml0.1mol/L的NaOH溶液时,若仰视定容,则所配溶液的物质的量浓度_______ (填“偏大”、“偏小”或“不变")。
(4)将适量Ba(OH)2•8H2O晶体与NH4Cl晶体放入烧杯中,用玻璃棒快速搅拌,试着拿起烧杯观察,晶体变成糊状,此外还可观察到_______ 等现象。
III物质性质和成分探究
(5)将二氧化硫气体通入到品红溶液中,溶液褪色,体现了二氧化硫的_______ 性。
(6)在实验室,浓硝酸保存在棕色试剂瓶中,因浓硝酸见光或受热易分解,产生有刺激性气味的红棕色气体,该气体为_______ (用化学式表示)。
I.物质结构和规律推断
如图为周期表中短周期的一部分,已知A是地壳中含量最多的元素。
| A | ||
| B | C | D |
(1)比较A、C的原子半径大小
(2)比较C、D的简单氢化物的稳定性
II.实验操作和现象分析
(3)配制100ml0.1mol/L的NaOH溶液时,若仰视定容,则所配溶液的物质的量浓度
(4)将适量Ba(OH)2•8H2O晶体与NH4Cl晶体放入烧杯中,用玻璃棒快速搅拌,试着拿起烧杯观察,晶体变成糊状,此外还可观察到
III物质性质和成分探究
(5)将二氧化硫气体通入到品红溶液中,溶液褪色,体现了二氧化硫的
(6)在实验室,浓硝酸保存在棕色试剂瓶中,因浓硝酸见光或受热易分解,产生有刺激性气味的红棕色气体,该气体为
您最近一年使用:0次



