按要求回答下列问题.
(1)请写出 在水溶液中的电离方程式
在水溶液中的电离方程式_____________________________________
(2)写出次氯酸见光分解的化学方程式_____________________________________
(3)纯净的 在氯气中安静地燃烧,发出
在氯气中安静地燃烧,发出_____________ 火焰
(4)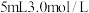 的
的 溶液加水稀释至
溶液加水稀释至 ,此时溶液中
,此时溶液中 的物质的量浓度为
的物质的量浓度为_____________
(5)若 某气体中含有的分子数为b个,则
某气体中含有的分子数为b个,则 该气体在标准状况下的体积为
该气体在标准状况下的体积为_____________________ (设 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
(6)高铁酸钾 是一种新型的净水剂,可以通过下述反应制取:
是一种新型的净水剂,可以通过下述反应制取:
①该反应中氧化剂是_____________ (用化学式表示),被氧化的元素是______________________
②用“单线桥”在方程式中标出电子转移的情况:_________________________________
(1)请写出
 在水溶液中的电离方程式
在水溶液中的电离方程式(2)写出次氯酸见光分解的化学方程式
(3)纯净的
 在氯气中安静地燃烧,发出
在氯气中安静地燃烧,发出(4)
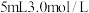 的
的 溶液加水稀释至
溶液加水稀释至 ,此时溶液中
,此时溶液中 的物质的量浓度为
的物质的量浓度为(5)若
 某气体中含有的分子数为b个,则
某气体中含有的分子数为b个,则 该气体在标准状况下的体积为
该气体在标准状况下的体积为 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)(6)高铁酸钾
 是一种新型的净水剂,可以通过下述反应制取:
是一种新型的净水剂,可以通过下述反应制取:
①该反应中氧化剂是
②用“单线桥”在方程式中标出电子转移的情况:
更新时间:2024-01-27 22:35:08
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】按要求完成下列填空:
(1)画出S2-结构示意图:___ 。
(2)某种核素质量数37,中子数20,其原子符号:___ 。
(3)某金属氯化物MCl240.5g中含有0.6molCl-,则M的摩尔质量为___ 。
(4)100mL0.25mol/LBaCl2溶液中Cl-的物质的量浓度为___ ;若将上述溶液稀释至500mL,Cl-的物质的量浓度为___ 。
(1)画出S2-结构示意图:
(2)某种核素质量数37,中子数20,其原子符号:
(3)某金属氯化物MCl240.5g中含有0.6molCl-,则M的摩尔质量为
(4)100mL0.25mol/LBaCl2溶液中Cl-的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某化学课外活动小组从实验室取出硫酸试剂,试剂瓶上标签的部分内容如图所示。该小组欲使用240mL 0.2mol·L-1的稀硫酸溶液。配制稀硫酸溶液时:

(1)配制稀硫酸所用容量瓶的规格为___________ mL。
(2)所需试剂瓶内浓硫酸的浓度为___________ mol·L-1,配制该稀硫酸溶液时所需要称量的浓硫酸的体积为___________ mL。
(3)下列为该小组的操作,可能导致配制溶液浓度偏高的是___________ 。
A.移液前未冷却至室温
B.定容时加水多了,用滴管吸出
C.定容时俯视刻度线
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(4)如图是该小组转移溶液的示意图,图中的错误是___________ 。


(1)配制稀硫酸所用容量瓶的规格为
(2)所需试剂瓶内浓硫酸的浓度为
(3)下列为该小组的操作,可能导致配制溶液浓度偏高的是
A.移液前未冷却至室温
B.定容时加水多了,用滴管吸出
C.定容时俯视刻度线
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(4)如图是该小组转移溶液的示意图,图中的错误是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.现有物质①铜、②干冰、③盐酸、④液态硫酸、⑤蔗糖、⑥NaHSO4固体、⑦红褐色的氢氧化铁胶体、⑧熔融的NaCl
(1)能导电的是___________ ;(填序号)属于电解质的是___________ 。(填序号)
(2)写出属于酸式盐的物质溶于水后的电离方程式:___________ 。
II.写出下列物质的电子式。
(3)① Na2O2___________ ;
② HClO___________ 。
III.写出相应的电极反应和总化学反应方程式。
(4)工业制备金属铝的总化学反应方程式:___________ 。
(5)电解稀的氢氧化钠溶液:阳极反应为___________ ;总反应方程式为___________ 。
(1)能导电的是
(2)写出属于酸式盐的物质溶于水后的电离方程式:
II.写出下列物质的电子式。
(3)① Na2O2
② HClO
III.写出相应的电极反应和总化学反应方程式。
(4)工业制备金属铝的总化学反应方程式:
(5)电解稀的氢氧化钠溶液:阳极反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求写出相应的方程式
(1)FeSO4的电离方程式________ 。
(2)Na在空气中点燃的化学方程式________ 。
(3)Al(OH)3溶解于NaOH溶液的离子方程式________ 。
(1)FeSO4的电离方程式
(2)Na在空气中点燃的化学方程式
(3)Al(OH)3溶解于NaOH溶液的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氧化还原反应是一类重要的化学反应,在工农业生产、日常生活中都有广泛的用途。亚硝酸钠(NaNO2)像食盐一样有咸味,但有很强的毒性,误食NaNO2会使人中毒。已知亚硝酸钠能发生如下反应: 2NaNO2+4HI=2NO↑+2NaI+I2+2H2O
(1)用双线桥法标出该反应中电子转移的方向及数目:_______ ,被氧化的原子与被还原的原子数目之比为______ ,在参加反应的HI中,起还原剂(被氧化)作用的HI与起酸的作用的HI的质量比为______ 。
(2)自来水中的 对人类健康会产生危害,碱性条件下用Al粉还原
对人类健康会产生危害,碱性条件下用Al粉还原 ,产物是N2,发生的反应可表示如下,完成方程式并配平。
,产物是N2,发生的反应可表示如下,完成方程式并配平。
____ Al+___  +
+_____ =____  +
+____ N2↑+____
(3)请将5种物质N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个配平的化学方程式。
________ +________ →________ +________ +_____ +_____ H2O
(1)用双线桥法标出该反应中电子转移的方向及数目:
(2)自来水中的
 对人类健康会产生危害,碱性条件下用Al粉还原
对人类健康会产生危害,碱性条件下用Al粉还原 ,产物是N2,发生的反应可表示如下,完成方程式并配平。
,产物是N2,发生的反应可表示如下,完成方程式并配平。 +
+ +
+(3)请将5种物质N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个配平的化学方程式。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)在Al、Fe2+、H+、S2-、SO2五种微粒中,只有氧化性的是_________ ,只有还原性的是______________ 既有氧化性又有还原性的是______________ 。
(2)有下列反应:Fe+Cu2+=Fe2++Cu;2Fe3++Cu=2Fe2++Cu2+;在Cu2+、Fe2+、Fe3+中,其氧化性由强到弱顺序为_______________ 。
(3)根据反应MnO2+4HCl MnCl2+Cl2↑+2H2O,回答下列问题:
MnCl2+Cl2↑+2H2O,回答下列问题:
①还原产物是____________
②该反应中盐酸的作用是________________ (填字母)
A.只氧化性B.只有酸性C.只有还原性 D.有氧化性也有酸性E.有还原性也有酸性
③ 用单线桥(或者双线桥)表示上述反应电子转移的方向和数目_______________
MnO2+ 4HCl=MnCl2+Cl2↑+2H2O
④该反应中氧化剂与还原剂物质的量之比为____________ 。
⑤如果该反应转移电子lmol,则生成标准状况下的气体体积为__________ L
(2)有下列反应:Fe+Cu2+=Fe2++Cu;2Fe3++Cu=2Fe2++Cu2+;在Cu2+、Fe2+、Fe3+中,其氧化性由强到弱顺序为
(3)根据反应MnO2+4HCl
 MnCl2+Cl2↑+2H2O,回答下列问题:
MnCl2+Cl2↑+2H2O,回答下列问题:①还原产物是
②该反应中盐酸的作用是
A.只氧化性B.只有酸性C.只有还原性 D.有氧化性也有酸性E.有还原性也有酸性
③ 用单线桥(或者双线桥)表示上述反应电子转移的方向和数目
MnO2+ 4HCl=MnCl2+Cl2↑+2H2O
④该反应中氧化剂与还原剂物质的量之比为
⑤如果该反应转移电子lmol,则生成标准状况下的气体体积为
您最近一年使用:0次
【推荐3】回答下列问题:
(1)高铁酸盐是一种新型、高效、多功能绿色水处理剂,工业上可用湿法制备高铁酸钾。化学反应原理为:2Fe(OH)3+3ClO-+4OH-=2FeO +3Cl-+5H2O。
+3Cl-+5H2O。
①FeO 中铁元素化合价为
中铁元素化合价为____ ,在该反应中氧化剂是____ ,还原剂是____ ,氧化产物是____ 。
②请用双线桥表示反应中电子转移情况:____ 。
③根据化合价,推测FeO 能和下列
能和下列____ 反应(填序号)。
A.KMnO4 B.SO2 C.H2S D.O2
(2)Co2O3、Co3+均属于极强的氧化剂,在生产中有着重要的应用。一定条件下,Co3+与过量Na2S2O3溶液反应后生成Co2+和SO ,写出该反应的离子方程式
,写出该反应的离子方程式____ 。设计实验证明反应后溶液中含有SO :
:____ 。(已知:S2O 与H+反应生成S、SO2,BaS2O3不溶于水)
与H+反应生成S、SO2,BaS2O3不溶于水)
(1)高铁酸盐是一种新型、高效、多功能绿色水处理剂,工业上可用湿法制备高铁酸钾。化学反应原理为:2Fe(OH)3+3ClO-+4OH-=2FeO
 +3Cl-+5H2O。
+3Cl-+5H2O。①FeO
 中铁元素化合价为
中铁元素化合价为②请用双线桥表示反应中电子转移情况:
③根据化合价,推测FeO
 能和下列
能和下列A.KMnO4 B.SO2 C.H2S D.O2
(2)Co2O3、Co3+均属于极强的氧化剂,在生产中有着重要的应用。一定条件下,Co3+与过量Na2S2O3溶液反应后生成Co2+和SO
 ,写出该反应的离子方程式
,写出该反应的离子方程式 :
: 与H+反应生成S、SO2,BaS2O3不溶于水)
与H+反应生成S、SO2,BaS2O3不溶于水)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】“生活无处不化学”,请你回答下列问题。
(1)厨房中的调味品①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。主要成分中具有碱性的是_______ (填序号,下同);属于盐类的是_______ ;相互间能发生反应的是_______ 。
(2)使用“84”消毒液(含NaClO)时,按一定比例与水混合,并在空气中浸泡一段时间,使NaClO与H2O及空气中的CO2充分反应,目的是得到杀菌消毒的效果更好的_______ (填物质名称),该反应的离子方程式是1ClO-+1CO2+1H2O=_______+_______。_______
(1)厨房中的调味品①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。主要成分中具有碱性的是
(2)使用“84”消毒液(含NaClO)时,按一定比例与水混合,并在空气中浸泡一段时间,使NaClO与H2O及空气中的CO2充分反应,目的是得到杀菌消毒的效果更好的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氯气是一种重要的化工原料,它的发现和研究经过了化学家们的不懈努力。
(1)舍勒发现氯气的方法是实验室制取氯气(如图1)的主要方法之一。
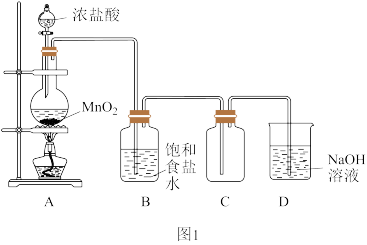
①装置A中发生反应的化学方程式为_________ 。
②装置B中饱和食盐水的作用是_________ 。
(2)泰纳将氯气通入石灰水,并进一步改进,制得了我们现在常用的漂白粉。漂白粉溶于水后,会与空气中的 反应产生具有漂白、杀菌作用的
反应产生具有漂白、杀菌作用的_________ (填化学式)。
(3)贝托莱发现氯气能溶于水。同学们利用数字化实验探究氯水失效的原因,进行实验:用强光照射盛有新制氯水的密闭广口瓶,并用传感器测定广口瓶中氯离子浓度和广口瓶中氧气的体积分数,得到如图2曲线。
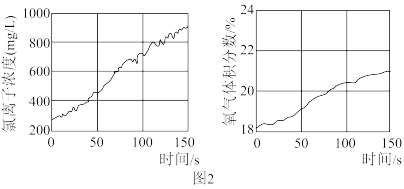
①解释图2两图中曲线变化的原因_________ (用化学方程式表示)。
②上述整个实验过程中,溶液 的变化情况是
的变化情况是_________ 。
(4)向含有酚酞的 溶液中滴加氯水,当氯水滴到一定量时,溶液红色会褪去。
溶液中滴加氯水,当氯水滴到一定量时,溶液红色会褪去。
①产生上述现象的原因可能有两种:一种是氯水中的酸与氢氧化钠发生中和反应,另一种是_________ 。
②设计实验验证溶液红色褪去的原因_________ 。(写出实验操作、现象及结论)。
(5)亚氯酸钠( )是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
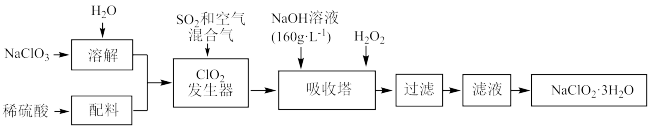
已知:a. 的溶解度随温度升高而增大,适当条件下可结晶析出
的溶解度随温度升高而增大,适当条件下可结晶析出 ;
;
b.纯 易分解爆炸,一般用稀有气体或空气稀释到10%以下较安全。
易分解爆炸,一般用稀有气体或空气稀释到10%以下较安全。
① 发生器中发生反应的离子方程式为
发生器中发生反应的离子方程式为_________ ,在发生器中鼓入空气的作用可能是_________ (填字母,下同)。
A.将 氧化成
氧化成 ,增强酸性
,增强酸性
B.稀释 以防止爆炸
以防止爆炸
C.将 氧化成
氧化成
②吸收塔中为防止 被还原成
被还原成 ,所用还原剂的还原性应适中。除
,所用还原剂的还原性应适中。除 外还可以选择的还原剂是
外还可以选择的还原剂是_________ 。
A. B.
B. C.
C. D.
D.
(1)舍勒发现氯气的方法是实验室制取氯气(如图1)的主要方法之一。

①装置A中发生反应的化学方程式为
②装置B中饱和食盐水的作用是
(2)泰纳将氯气通入石灰水,并进一步改进,制得了我们现在常用的漂白粉。漂白粉溶于水后,会与空气中的
 反应产生具有漂白、杀菌作用的
反应产生具有漂白、杀菌作用的(3)贝托莱发现氯气能溶于水。同学们利用数字化实验探究氯水失效的原因,进行实验:用强光照射盛有新制氯水的密闭广口瓶,并用传感器测定广口瓶中氯离子浓度和广口瓶中氧气的体积分数,得到如图2曲线。

①解释图2两图中曲线变化的原因
②上述整个实验过程中,溶液
 的变化情况是
的变化情况是(4)向含有酚酞的
 溶液中滴加氯水,当氯水滴到一定量时,溶液红色会褪去。
溶液中滴加氯水,当氯水滴到一定量时,溶液红色会褪去。①产生上述现象的原因可能有两种:一种是氯水中的酸与氢氧化钠发生中和反应,另一种是
②设计实验验证溶液红色褪去的原因
(5)亚氯酸钠(
 )是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图: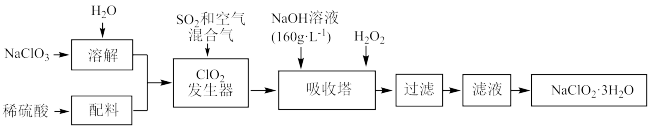
已知:a.
 的溶解度随温度升高而增大,适当条件下可结晶析出
的溶解度随温度升高而增大,适当条件下可结晶析出 ;
;b.纯
 易分解爆炸,一般用稀有气体或空气稀释到10%以下较安全。
易分解爆炸,一般用稀有气体或空气稀释到10%以下较安全。①
 发生器中发生反应的离子方程式为
发生器中发生反应的离子方程式为A.将
 氧化成
氧化成 ,增强酸性
,增强酸性B.稀释
 以防止爆炸
以防止爆炸C.将
 氧化成
氧化成
②吸收塔中为防止
 被还原成
被还原成 ,所用还原剂的还原性应适中。除
,所用还原剂的还原性应适中。除 外还可以选择的还原剂是
外还可以选择的还原剂是A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(I)实验室可由软锰矿(主要成分为MnO2)制备KMnO4,方法如下:软锰矿和过量的固体KOH和KClO3在高温下反应,生成锰酸钾(K2MnO4)和KCl;用水溶解,滤去残渣,滤液酸化后,K2MnO4转变为MnO2和KMnO4;滤去MnO2沉淀,浓缩溶液,结晶得到深紫色的针状KMnO4。试回答:
(1)软锰矿制备K2MnO4的化学方程式是____________________________ 。
(2)K2MnO4制备KMnO4的离子方程式是__________________________________ 。
(3)KMnO4能与热的稀硫酸酸化的Na2C2O4反应,生成Mn2+和CO2,该反应的化学方程式是________________________________________________ 。
(II)检验Na2SO3样品部分被氧化的实验操作及现象_____________________ 。
(III)在强碱溶液中NaClO与Fe(OH)3反应生成Na2FeO4:_______________________ 。
(1)软锰矿制备K2MnO4的化学方程式是
(2)K2MnO4制备KMnO4的离子方程式是
(3)KMnO4能与热的稀硫酸酸化的Na2C2O4反应,生成Mn2+和CO2,该反应的化学方程式是
(II)检验Na2SO3样品部分被氧化的实验操作及现象
(III)在强碱溶液中NaClO与Fe(OH)3反应生成Na2FeO4:
您最近一年使用:0次



