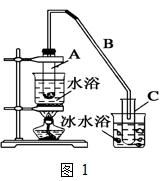
某化学小组采用类似制乙酸乙酯的装置(如图1),以环己醇制备环己烯(二者均易挥发)。
已知: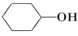
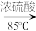
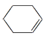 +H2O
+H2O
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①导管B除了导气外还具有的作用是______ 。
②试管C置于冰水浴中的目的是______ 。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_____ 层(填“上”或“下”),分液后用______ (填入编号)洗涤。
a.KMnO4溶液 b.稀硫酸 c.Na2CO3溶液
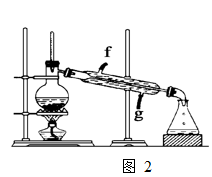
②再将环己烯按如图2装置蒸馏,蒸馏时要加入生石灰。
③收集产品时,控制的温度应在_____ 左右,实验制得的环己烯精品质量低于理论产量,可能的原因是_____ 。
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)检测
以下区分环己烯精品和粗品的方法,合理的是______ 。
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点

已知:

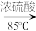
 +H2O
+H2O| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①导管B除了导气外还具有的作用是
②试管C置于冰水浴中的目的是
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在
a.KMnO4溶液 b.稀硫酸 c.Na2CO3溶液
②再将环己烯按如图2装置蒸馏,蒸馏时要加入生石灰。

③收集产品时,控制的温度应在
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)检测
以下区分环己烯精品和粗品的方法,合理的是
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
更新时间:2022/12/20 16:37:30
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】用如图所示的实验装置制备少量乙酸乙酯。请回答问题,将所选方法的数字代号填在括号中:
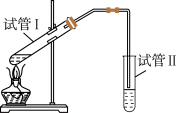
(1)试管Ⅰ中盛有由2mL浓硫酸、3mL乙醇、2mL冰醋酸组成的反应混合液,其中浓硫酸的作用是________ 。
①催化剂和吸水剂,②脱水剂
(2)试管Ⅱ中的导管口为什么要在液面之上?________ 。
①防止倒吸,②有利于气体导出
(3)试管Ⅱ中的Na2CO3溶液的主要作用是(不定项)________ 。
①降低乙酸乙酯在溶液中的溶解度;
②除去挥发出的乙酸;
③溶解挥发出的乙醇。

(1)试管Ⅰ中盛有由2mL浓硫酸、3mL乙醇、2mL冰醋酸组成的反应混合液,其中浓硫酸的作用是
①催化剂和吸水剂,②脱水剂
(2)试管Ⅱ中的导管口为什么要在液面之上?
①防止倒吸,②有利于气体导出
(3)试管Ⅱ中的Na2CO3溶液的主要作用是(不定项)
①降低乙酸乙酯在溶液中的溶解度;
②除去挥发出的乙酸;
③溶解挥发出的乙醇。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】实验室制乙酸乙酯的主要装置如图所示,主要步骤①在a试管中按2:3:2的体积比配制浓硫酸、乙醇、乙酸的混合物;②按图示连接装置,使产生的蒸气经导管通到b试管所盛的饱和碳酸钠溶液(加入几滴酚酞试液)中;③小火加热a试管中的混合液;④等b试管中收集到约2mL产物时停止加热。撤下b试管并用力振荡,然后静置,待其中液体分层;⑤分离出乙酸乙酯。
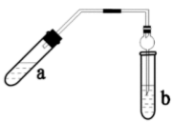
请回答下列问题:
(1)若实验中用含 的乙醇与乙酸作用,该反应的化学方程式是
的乙醇与乙酸作用,该反应的化学方程式是_______ 。
(2)装置中使用球形干燥管除起到冷凝作用外,另一重要作用是_______ ,步骤④中可观察到b试管中有细小的气泡冒出,写出该反应的离子方程式_______ 。
(3)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用如图所示装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管b再测有机层的厚度,实验记录如表:实验
①实验D的目的是与实验C相对照,证明 对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是
对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是_______ mL和_______  。
。
②分析实验_______ (填实验编号)的数据,可以推测出浓 的吸水性提高了乙酸乙酯的产率。浓硫酸的吸水性能够提高乙酸乙酯产率的原因是
的吸水性提高了乙酸乙酯的产率。浓硫酸的吸水性能够提高乙酸乙酯产率的原因是_______ 。

请回答下列问题:
(1)若实验中用含
 的乙醇与乙酸作用,该反应的化学方程式是
的乙醇与乙酸作用,该反应的化学方程式是(2)装置中使用球形干燥管除起到冷凝作用外,另一重要作用是
(3)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用如图所示装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管b再测有机层的厚度,实验记录如表:实验
| 实验编号 | 试管a中试剂 | 试管b试剂 | 测得有机层的厚度/cm |
| A | 3mL乙醇、2mL乙酸、1mL 18 浓硫酸 浓硫酸 | 饱和 溶液 溶液 | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 | |
| C | 3mL乙醇、2mL乙酸、6mL 3  | 1.2 | |
| D | 3mL乙醇、2mL乙酸、盐酸 | 1.2 |
 对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是
对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是 。
。②分析实验
 的吸水性提高了乙酸乙酯的产率。浓硫酸的吸水性能够提高乙酸乙酯产率的原因是
的吸水性提高了乙酸乙酯的产率。浓硫酸的吸水性能够提高乙酸乙酯产率的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】乙酸乙酯是一种重要的有机化工原料和工业溶剂,具有低毒性,有甜味,浓度较高时有刺激性气味,易挥发,属于一级易燃品,应储存于低温通风处,远离火种火源。实验室一般通过乙酸和乙醇的酯化反应来制取,实验装置如图所示(夹持装置已省略),主要步骤如下:
①在甲试管中加入 浓硫酸、
浓硫酸、 乙酸和
乙酸和 乙醇,再加入几片碎瓷片。
乙醇,再加入几片碎瓷片。
②按图连接好装置(装置的气密性良好),小火均匀地加热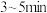 。
。
③待乙试管收集到一定量产物后停止加热,撤出乙试管并用力振荡,然后静置待分层。
④分离出乙酸乙酯层,洗涤、干燥,得乙酸乙酯产品。

(1)写出上述实验中生成乙酸乙酯反应的化学方程式:____ 。乙试管中长玻璃导管的作用是____ 。
(2)步骤②中需要用小火均匀加热,其主要原因是____ 。
(3)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上述实验装置进行下列3组实验。实验开始时先用酒精灯微热甲试管中的试剂 ,再加热使之微微沸腾
,再加热使之微微沸腾 。实验结束后,充分振荡乙试管并测其有机层的厚度,实验数据记录如下:
。实验结束后,充分振荡乙试管并测其有机层的厚度,实验数据记录如下:
①实验C中a=_____ 。
②分析实验____ (填字母)的数据,可以推测出浓 的吸水性提高了乙酸乙酯的产率。
的吸水性提高了乙酸乙酯的产率。
③已知;乙酸的密度为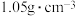 ,乙醇的密度为
,乙醇的密度为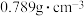 ,实验
,实验 收集到的乙酸乙酯的质量为
收集到的乙酸乙酯的质量为 。则该反应中产品的产率为
。则该反应中产品的产率为_____ (产率 )
)
①在甲试管中加入
 浓硫酸、
浓硫酸、 乙酸和
乙酸和 乙醇,再加入几片碎瓷片。
乙醇,再加入几片碎瓷片。②按图连接好装置(装置的气密性良好),小火均匀地加热
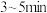 。
。③待乙试管收集到一定量产物后停止加热,撤出乙试管并用力振荡,然后静置待分层。
④分离出乙酸乙酯层,洗涤、干燥,得乙酸乙酯产品。

(1)写出上述实验中生成乙酸乙酯反应的化学方程式:
(2)步骤②中需要用小火均匀加热,其主要原因是
(3)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上述实验装置进行下列3组实验。实验开始时先用酒精灯微热甲试管中的试剂
 ,再加热使之微微沸腾
,再加热使之微微沸腾 。实验结束后,充分振荡乙试管并测其有机层的厚度,实验数据记录如下:
。实验结束后,充分振荡乙试管并测其有机层的厚度,实验数据记录如下:| 实验组号 | 甲试管中试剂 | 乙试管中试剂 | 有机层的厚度/ |
| A |  乙醇、 乙醇、 乙酸、 乙酸、 浓硫酸 浓硫酸 | 饱和 溶液 溶液 | 3.0 |
| B |  乙醇、 乙醇、 乙酸、 乙酸、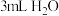 | 0.1 | |
| C |  乙醇、 乙醇、 乙酸、 乙酸、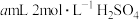 溶液 溶液 | 0.6 |
②分析实验
 的吸水性提高了乙酸乙酯的产率。
的吸水性提高了乙酸乙酯的产率。③已知;乙酸的密度为
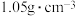 ,乙醇的密度为
,乙醇的密度为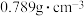 ,实验
,实验 收集到的乙酸乙酯的质量为
收集到的乙酸乙酯的质量为 。则该反应中产品的产率为
。则该反应中产品的产率为 )
)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】乙酰水杨酸(阿司匹林)是目前常用药物之一。实验室通过水杨酸进行乙酰化制备阿司匹林的一种方法如下:
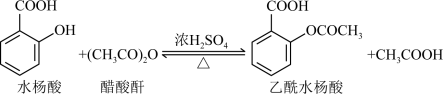
实验过程:在100mL锥形瓶中加入水杨酸6.9g及醋酸酐10mL,充分摇动使固体完全溶解。
缓慢滴加0.5mL浓硫酸后加热,维持瓶内温度在70℃左右,充分反应。稍冷后进行如下操作。
①在不断搅拌下将反应后的混合物倒入100mL冷水中,析出固体,过滤。
②所得结晶粗品加入50mL饱和碳酸氢钠溶液,溶解、过滤。
③滤液用浓盐酸酸化后冷却、过滤得固体。
④固体经纯化得白色的乙酰水杨酸晶体2.7g。
回答下列问题:
(1)该合成反应中应采用________(填字母)加热。
(2)下列玻璃仪器中,①中需使用的有________ (填字母),不需使用的有________________ (填名称)
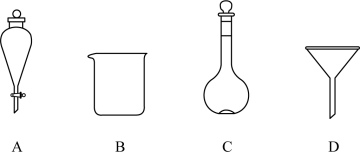
(3)①中需使用冷水目的是充分析出乙酰水杨酸固体,推测原因:_________________ 。
(4)③中加入浓盐酸的目的:________________________ 。
(5)④采用的纯化方法为________________ 。
(6)本实验的产率是________ %。

水杨酸 | 醋酸酐 | 乙酰水杨酸 | |
熔点/℃ | 157~159 | -72~-74 | 135~138 |
相对密度/( | 1.44 | 1.10 | 1.35 |
相对分子质量 | 138 | 102 | 180 |
缓慢滴加0.5mL浓硫酸后加热,维持瓶内温度在70℃左右,充分反应。稍冷后进行如下操作。
①在不断搅拌下将反应后的混合物倒入100mL冷水中,析出固体,过滤。
②所得结晶粗品加入50mL饱和碳酸氢钠溶液,溶解、过滤。
③滤液用浓盐酸酸化后冷却、过滤得固体。
④固体经纯化得白色的乙酰水杨酸晶体2.7g。
回答下列问题:
(1)该合成反应中应采用________(填字母)加热。
| A.热水浴 | B.酒精灯 | C.煤气灯 | D.电炉 |

(3)①中需使用冷水目的是充分析出乙酰水杨酸固体,推测原因:
(4)③中加入浓盐酸的目的:
(5)④采用的纯化方法为
(6)本实验的产率是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】草酸及其化合物在工业中有重要作用,例如:草酸可用于除铁锈,反应的离子方程式为: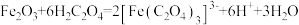 ;草酸铁铵[(NH4)3Fe(C2O4)3]是一种常用的金属着色剂。
;草酸铁铵[(NH4)3Fe(C2O4)3]是一种常用的金属着色剂。
(1)草酸(H2C2O4)是一种弱酸,不稳定,受热或遇浓硫酸会发生分解。在浓硫酸催化作用下,用硝酸氧化葡萄糖可制取草酸,实验装置如图所示
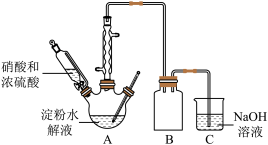
①装置B的作用是___________ 。
②葡萄糖溶液可由反应 得到。该实验中证明淀粉已经完全水解的实验操作及现象是
得到。该实验中证明淀粉已经完全水解的实验操作及现象是___________________ 。
③55℃~60℃时,装置A中生成H2C2O4,同时生成NO。要将16.2g淀粉完全水解后的淀粉水解液完全转化为草酸,理论上消耗2mol•L-1HNO3溶液的体积为___________ mL。
④该实验中催化剂浓硫酸用量过多,会导致草酸产率减少,原因是_____________________ 。
(2)制得的草酸铁铵晶体中往往会混有少量草酸,为测定(NH4)3Fe(C2O4)3.3H2O(M=428g/mol)的含量,进行下列实验:称取样品9.46g,加稀硫酸溶解后,配成100mL溶液。取20.00mL配制的溶液,用浓度为0.2000mol/L的KMnO4溶液滴定至终点时消耗KMnO4溶液28.00mL。已知: (未配平)。通过计算,确定样品中(NH4)3Fe(C2O4)3.3H2O的质量分数
(未配平)。通过计算,确定样品中(NH4)3Fe(C2O4)3.3H2O的质量分数___________ (写出计算过程)。
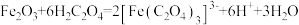 ;草酸铁铵[(NH4)3Fe(C2O4)3]是一种常用的金属着色剂。
;草酸铁铵[(NH4)3Fe(C2O4)3]是一种常用的金属着色剂。(1)草酸(H2C2O4)是一种弱酸,不稳定,受热或遇浓硫酸会发生分解。在浓硫酸催化作用下,用硝酸氧化葡萄糖可制取草酸,实验装置如图所示

①装置B的作用是
②葡萄糖溶液可由反应
 得到。该实验中证明淀粉已经完全水解的实验操作及现象是
得到。该实验中证明淀粉已经完全水解的实验操作及现象是③55℃~60℃时,装置A中生成H2C2O4,同时生成NO。要将16.2g淀粉完全水解后的淀粉水解液完全转化为草酸,理论上消耗2mol•L-1HNO3溶液的体积为
④该实验中催化剂浓硫酸用量过多,会导致草酸产率减少,原因是
(2)制得的草酸铁铵晶体中往往会混有少量草酸,为测定(NH4)3Fe(C2O4)3.3H2O(M=428g/mol)的含量,进行下列实验:称取样品9.46g,加稀硫酸溶解后,配成100mL溶液。取20.00mL配制的溶液,用浓度为0.2000mol/L的KMnO4溶液滴定至终点时消耗KMnO4溶液28.00mL。已知:
 (未配平)。通过计算,确定样品中(NH4)3Fe(C2O4)3.3H2O的质量分数
(未配平)。通过计算,确定样品中(NH4)3Fe(C2O4)3.3H2O的质量分数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
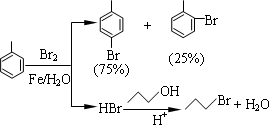
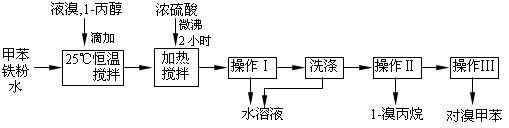
【推荐3】对溴甲苯是合成农药溴螨酯的重要原料。工业用液溴、甲苯与1-丙醇共热合成对溴甲苯和1-溴丙烷,其原子利用率很高。实验室模拟的合成流程和相关数据如下:已知:甲苯与溴在有水存在时能反应。
(1)液溴的颜色是_________ ,实验室存放液溴时应密闭保存,同时需要在试剂瓶中加________ ,以减少挥发。
(2)25℃恒温搅拌至溴的颜色完全褪去时完成甲苯的溴代反应。搅拌的目的是__________ 。加入水的作用是:易于控制温度;____________________ 。
(3)加热搅拌操作中加入浓硫酸,搅拌,完成1-丙醇的取代反应,加入浓硫酸的作用是_________ ,加热微沸2小时的目的是_______________ 。
(4)操作Ⅰ的名称是___________ ,洗涤操作应在_________ (填写仪器名称)中进行。
(5)经以上分离操作后,粗对溴甲苯中还含有的最主要杂质为________ (填写名称),使用操作Ⅱ分离出1-溴丙烷的原理是______________________________________ 。
(6)分离出的水溶液中含HBr、H2SO4和Fe3+离子,将水溶液稀释定容至1000mL,取20.00mL,加入几滴甲基橙作指示剂,用一定浓度的NaOH溶液滴定,测定出HBr的物质的量明显低于理论值,原因是_____________________ ;有同学认为无需加入指示剂,也能完成滴定,提出这一观点的理由是_______________________________ 。
| 物质 | 甲苯 | 1-丙醇 | 1-溴丙烷 |
| 沸点℃ | 110.8 | 97.2 | 71 |
| 物质 | 对溴甲苯 | 邻溴甲苯 | |
| 沸点℃ | 184.3 | 181.7 | |


(1)液溴的颜色是
(2)25℃恒温搅拌至溴的颜色完全褪去时完成甲苯的溴代反应。搅拌的目的是
(3)加热搅拌操作中加入浓硫酸,搅拌,完成1-丙醇的取代反应,加入浓硫酸的作用是
(4)操作Ⅰ的名称是
(5)经以上分离操作后,粗对溴甲苯中还含有的最主要杂质为
(6)分离出的水溶液中含HBr、H2SO4和Fe3+离子,将水溶液稀释定容至1000mL,取20.00mL,加入几滴甲基橙作指示剂,用一定浓度的NaOH溶液滴定,测定出HBr的物质的量明显低于理论值,原因是
您最近一年使用:0次

 )
)

