某实验小组用0.50 NaOH溶液和0.50
NaOH溶液和0.50 硫酸溶液进行中和热的测定。
硫酸溶液进行中和热的测定。
(一)配制0.50 NaOH溶液。
NaOH溶液。
(1)若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体_______ g。
(2)从下图中选择称量NaOH固体所需要的仪器_______ (填字母)。
(二)测定稀硫酸和稀氢氧化钠反应的中和热的实验装置如图所示。
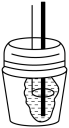
(3)写出该反应的热化学方程式(中和热 ):
):_______ 。
(4)取50mLNaOH溶液和30mL硫酸溶液进行实验,实验数据如下表。
①请填写表中的空白:
②近似认为0.50 NaOH溶液和0.50
NaOH溶液和0.50 硫酸溶液的密度都是1
硫酸溶液的密度都是1 ,中和后生成溶液的比热容
,中和后生成溶液的比热容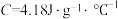 。则测得中和热
。则测得中和热 =
=_______  (取小数点后一位)。
(取小数点后一位)。
③上述实验数值结果与57.3 有偏差,产生偏差的原因可能是
有偏差,产生偏差的原因可能是_______ (填字母)。
A.实验装置保温、隔热效果差
B.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
C.用温度计测定NaOH溶液起始温度后直接测定 溶液的温度
溶液的温度
 NaOH溶液和0.50
NaOH溶液和0.50 硫酸溶液进行中和热的测定。
硫酸溶液进行中和热的测定。(一)配制0.50
 NaOH溶液。
NaOH溶液。(1)若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体
(2)从下图中选择称量NaOH固体所需要的仪器
| 序号 | a | b | c | d | e | f |
| 仪器 | 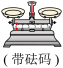 |  |  |  |  |  |
(二)测定稀硫酸和稀氢氧化钠反应的中和热的实验装置如图所示。

(3)写出该反应的热化学方程式(中和热
 ):
):(4)取50mLNaOH溶液和30mL硫酸溶液进行实验,实验数据如下表。
①请填写表中的空白:
| 实验次数 | 起始温度 /℃ /℃ | 终止温度 /℃ /℃ | 温度差平均值 (  - - )/℃ )/℃ | ||
 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
 NaOH溶液和0.50
NaOH溶液和0.50 硫酸溶液的密度都是1
硫酸溶液的密度都是1 ,中和后生成溶液的比热容
,中和后生成溶液的比热容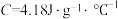 。则测得中和热
。则测得中和热 =
= (取小数点后一位)。
(取小数点后一位)。③上述实验数值结果与57.3
 有偏差,产生偏差的原因可能是
有偏差,产生偏差的原因可能是A.实验装置保温、隔热效果差
B.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
C.用温度计测定NaOH溶液起始温度后直接测定
 溶液的温度
溶液的温度
22-23高二上·河南鹤壁·期末 查看更多[3]
更新时间:2022/12/31 09:29:47
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】中和热的测定是高中化学中重要的定量实验。取50mL、0.55mol/L的NaOH溶液与50mL、0.25mol/L的H2SO4溶液置于如图所示的装置中进行中和热的测定实验,回答下列问题:
(1)从如图所示实验装置看,其中尚缺少的一种玻璃用品是_____________ ,除此之外,装置的一个明显错误是___________________________________________________ 。
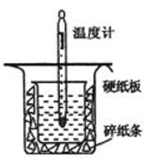
(2)NaOH溶液稍过量的原因是_______________________________________________ 。
(3)若改用60mL、0.25mol/L的H2SO4溶液和50mL、0.55mol/L的NaOH溶液进行反应,与上述实验相比,所放出的热量_____________ (填“相等”或“不相等”),若实验操作均正确,则所求中和热_______________ (填“相等”或“不相等”)。
(4)倒入NaOH溶液的正确操作是__________
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次性迅速倒入
(5)实验数据如下表:
①近似认为0.55mol/L NaOH溶液和0.25mol/L H2SO4溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g∙℃),则中和热△H=__________ (取小数点后一位)。
②上述实验的结果与57.3kJ/mol有偏差,产生偏差的原因可能是____________ 。
A.实验装置保温、隔热效果差
B.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
C.做实验的当天室温较高
D.量取H2SO4时仰视读数
(1)从如图所示实验装置看,其中尚缺少的一种玻璃用品是

(2)NaOH溶液稍过量的原因是
(3)若改用60mL、0.25mol/L的H2SO4溶液和50mL、0.55mol/L的NaOH溶液进行反应,与上述实验相比,所放出的热量
(4)倒入NaOH溶液的正确操作是
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次性迅速倒入
(5)实验数据如下表:
| 温度 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
②上述实验的结果与57.3kJ/mol有偏差,产生偏差的原因可能是
A.实验装置保温、隔热效果差
B.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
C.做实验的当天室温较高
D.量取H2SO4时仰视读数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】中和热的测定实验中取0.5 mol/L的NaOH溶液50 mL与0.25 mol/L的硫酸50 mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:
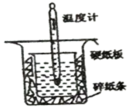
(1)从上图实验装置看,其中尚缺少的一种玻璃用品是___ ,除此之外装置中的一个明显错误是___ 。
(2)若改用60 mL 0.25mol/LH2SO4和50 mL 0.55mol/LNaOH溶液进行反应与上述实验相比,所放出的热量_____ ( 填“相等”或“不相等”)。
(3)近似认为0.55 mol/L NaOH溶液和0.25 mol/L硫酸溶液的密度都是l g/cm3,中和后生成溶液的比热c=4.18 J(g·℃),通过以上数据计算中和热△H=____ (结果保留小数点后一位)。
(4)上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)______ 。
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把 NaOH溶液倒入盛有硫酸的小烧杯中

(1)从上图实验装置看,其中尚缺少的一种玻璃用品是
(2)若改用60 mL 0.25mol/LH2SO4和50 mL 0.55mol/LNaOH溶液进行反应与上述实验相比,所放出的热量
温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | ||
H2SO4 | NaOH | 平均值 | ||
1 | 26.2 | 26.0 | 26.1 | 29.5 |
2 | 27.0 | 27.4 | 27.2 | 32.3 |
3 | 25.9 | 25.9 | 25.9 | 29.2 |
4 | 26.4 | 26.2 | 26.3 | 29.8 |
(4)上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把 NaOH溶液倒入盛有硫酸的小烧杯中
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
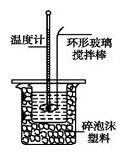
(1)在操作正确的前提下,提高中和热测定准确性的关键是_________
(2)做1次完整的中和热测定实验,温度计需使用________ 次,某同学为了省去清洗温度计的麻烦,建议实验时使用两支温度计分别测量酸和碱的温度,你是否同意该同学的观点,为什么?__________ ,_____________________________
(3)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量__________ (填“相等、不相等”),所求中和热__________ (填“相等、不相等”),简述理由 ___________ 。

(1)在操作正确的前提下,提高中和热测定准确性的关键是
(2)做1次完整的中和热测定实验,温度计需使用
(3)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室利用下图装置进行中和热的测定,请回答下列问题:
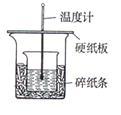
(1)在操作正确的前提下,提高中和热测定准确性的关键是________
(2)做1次完整的中和热测定实验,温度计需使用_____________ 次,某同学为了省去清洗温度计的麻烦,建议实验时使用两支温度计分别测量酸和碱的温度,你是否同意该同学的观点,为什么?____________________________ 。

(1)在操作正确的前提下,提高中和热测定准确性的关键是
(2)做1次完整的中和热测定实验,温度计需使用
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.LiH可作飞船的燃料,已知下列反应:
①2Li(s)+H2(g)═2LiH(s)△H=﹣182kJ•mol﹣1;
②2H2(g)+O2(g)═2H2O(1)△H═﹣572kJ•mol﹣1;
③4Li(s)+O2(g)═2Li2O(s)△H═﹣1196kJ•mol﹣1。
(1)写出LiH在O2中燃烧的热化学方程式__________________ 。
Ⅱ.中和热是指酸跟碱发生中和反应生成1mol H2O所放出的热量.某学生想通过测定反应过程中所放出的热量来计算中和热.他将50mL 0.5mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题:
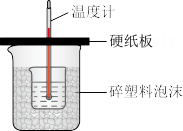
(2)从实验装置上看,图中尚缺少的一种玻璃用品是_____ ,烧杯间填满碎塑料泡沫的作用是_____ 。
(3)大烧杯上如不盖硬纸板,则求得的中和热数值_____ (填“偏大”、“偏小’、“无影响”)。
(4)实验中改用60mL 0.50mol/L的盐酸跟50mL 0.55mol/L的NaOH溶液进行反应,与上述实验相比,所求中和热的数值会_____ (填“相等”或“不相等”),理由是_____ 。
(5)设50mL 0.5mol/L的盐酸与50mL 0.55mol/L的NaOH溶液反应的反应热为△H1,25mL 0.5mol/L的浓硫酸与50mL 0.55mol/L的NaOH溶液反应的反应热为△H2,50mL 0.5mol/L的醋酸与50mL 0.55mol/L的NaOH溶液反应的反应热为△H3,则△H1、△H2、△H3的关系是____ (用“>”“<”或“=”连接)。
①2Li(s)+H2(g)═2LiH(s)△H=﹣182kJ•mol﹣1;
②2H2(g)+O2(g)═2H2O(1)△H═﹣572kJ•mol﹣1;
③4Li(s)+O2(g)═2Li2O(s)△H═﹣1196kJ•mol﹣1。
(1)写出LiH在O2中燃烧的热化学方程式
Ⅱ.中和热是指酸跟碱发生中和反应生成1mol H2O所放出的热量.某学生想通过测定反应过程中所放出的热量来计算中和热.他将50mL 0.5mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题:

(2)从实验装置上看,图中尚缺少的一种玻璃用品是
(3)大烧杯上如不盖硬纸板,则求得的中和热数值
(4)实验中改用60mL 0.50mol/L的盐酸跟50mL 0.55mol/L的NaOH溶液进行反应,与上述实验相比,所求中和热的数值会
(5)设50mL 0.5mol/L的盐酸与50mL 0.55mol/L的NaOH溶液反应的反应热为△H1,25mL 0.5mol/L的浓硫酸与50mL 0.55mol/L的NaOH溶液反应的反应热为△H2,50mL 0.5mol/L的醋酸与50mL 0.55mol/L的NaOH溶液反应的反应热为△H3,则△H1、△H2、△H3的关系是
您最近一年使用:0次
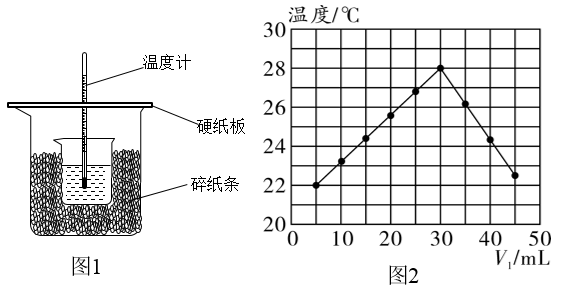
【推荐3】某实验小组设计用 50mL 0.50mol·L-1盐酸和50mL 0.55mol·L-1氢氧化钠溶液在如图1装置中进行中和反应,通过测定反应过程中所放出的热量计算中和热。
(1)在大小烧杯之间填充碎泡沫塑料的主要作用是___________ 。
(2)从实验装置上看,图1中尚缺少的一种玻璃用品是:___________ 。
(3)若改用 60mL 0.50mol·L-1盐酸和 50mL 0.55mol·L-1氢氧化钠溶液进行反应,则与上述实验相比,所放热量___________ (填“增加”、“减少”或“不变”,下同),所求中和热数值___________ 。
(4)假设盐酸和氢氧化钠溶液的密度都是1g·cm-3,又知中和反应后生成溶液的比热容c=4.18J·g-1·℃-1,为了计算中和热,某学生实验数据记录如表:
平均温度差是___________ ℃,该实验测得的中和热ΔH=___________ kJ·mol-1(结果精确到0.1)。
(5)在中和热测定实验中,若用温度计测定NaOH溶液起始温度后直接测定盐酸的温度,则测得的中和热数值___________ (填“偏大”“偏小”或“不变”)。
(6)实验小组另取V1mL0.50mol·L-1HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图2所示(实验中始终保持V1+V2=50mL)。则实验小组做该实验时的环境温度___________ (填“高于”“低于”或“等于”)22℃,NaOH溶液的浓度为___________ mol·L-1。

(1)在大小烧杯之间填充碎泡沫塑料的主要作用是
(2)从实验装置上看,图1中尚缺少的一种玻璃用品是:
(3)若改用 60mL 0.50mol·L-1盐酸和 50mL 0.55mol·L-1氢氧化钠溶液进行反应,则与上述实验相比,所放热量
(4)假设盐酸和氢氧化钠溶液的密度都是1g·cm-3,又知中和反应后生成溶液的比热容c=4.18J·g-1·℃-1,为了计算中和热,某学生实验数据记录如表:
| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | 氢氧化钠溶液 | 混合溶液 | |
1 | 20 | 20.1 | 23 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
(5)在中和热测定实验中,若用温度计测定NaOH溶液起始温度后直接测定盐酸的温度,则测得的中和热数值
(6)实验小组另取V1mL0.50mol·L-1HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图2所示(实验中始终保持V1+V2=50mL)。则实验小组做该实验时的环境温度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】一种生活中常用的纯碱溶液浓度为 0.5 mol/L,某同学欲用纯碱粉末配制该溶液 480 mL 备用。请回答下列相关问题:
(1)除烧杯、玻璃棒外,一定还需要用到的玻璃仪器有____________
(2)计算:需要称取纯碱固体的质量为__________ g
(3)配制时,正确的操作顺序是(每个序号只用一次)_______________
A.用少量水洗涤烧杯 2 次~3 次,洗涤液均注入容量瓶,振荡
B.在盛有纯碱固体的烧杯中加入适量水溶解
C.将恢复到室温的溶液沿玻璃棒注入容量瓶中
D.将容量瓶塞紧,上下颠倒摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度线相平
F.继续往容量瓶内小心加水,直到液面接近刻度 1 cm~2 cm 处
(4)下列会导致所配溶液实际浓度偏高的是____________
a.在 C 步骤中未恢复到室温即注入容量瓶
b.在 D 步骤完成后发现液面低于刻度线
c.在 E 步骤中俯视凹液面
(5)若欲用上述溶液另外配制 100 mL 0.2 mol/L 的纯碱溶液,则需取用上述溶液的体积为_________ mL
(1)除烧杯、玻璃棒外,一定还需要用到的玻璃仪器有
(2)计算:需要称取纯碱固体的质量为
(3)配制时,正确的操作顺序是(每个序号只用一次)
A.用少量水洗涤烧杯 2 次~3 次,洗涤液均注入容量瓶,振荡
B.在盛有纯碱固体的烧杯中加入适量水溶解
C.将恢复到室温的溶液沿玻璃棒注入容量瓶中
D.将容量瓶塞紧,上下颠倒摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度线相平
F.继续往容量瓶内小心加水,直到液面接近刻度 1 cm~2 cm 处
(4)下列会导致所配溶液实际浓度偏高的是
a.在 C 步骤中未恢复到室温即注入容量瓶
b.在 D 步骤完成后发现液面低于刻度线
c.在 E 步骤中俯视凹液面
(5)若欲用上述溶液另外配制 100 mL 0.2 mol/L 的纯碱溶液,则需取用上述溶液的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为_______ mol·L-1
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_______(填字母)。
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol·L-1的稀盐酸。
①该学生需要量取_______ mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在横线填表示“偏大”、“偏小”或“无影响”)。
a.用量筒量取浓盐酸时俯视观察凹液面_______
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水_______
(4)①假设该同学成功配制了0.400mol·L-1的盐酸,他又用该盐酸中和1L0.0100mol·L-1的NaOH溶液,则该同学需取_______ mL盐酸。如果他要配制500ml0.100mol·L-1NaOH溶液,他要用托盘天平称量_______ gNaOH固体。
②假设该同学用新配制的盐酸中和含0.4gNaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是_______ 。(填字母)
A.浓盐酸挥发,浓度不足
B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线
D.加水时超过刻度线,用胶头滴管吸出
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:1.19 g·cm-3 HCl的质量分数:36.5%) |
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_______(填字母)。
| A.溶液中HCl的物质的量 | B.溶液的浓度 |
| C.溶液中Cl-的数目 | D.溶液的密度 |
①该学生需要量取
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在横线填表示“偏大”、“偏小”或“无影响”)。
a.用量筒量取浓盐酸时俯视观察凹液面
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
(4)①假设该同学成功配制了0.400mol·L-1的盐酸,他又用该盐酸中和1L0.0100mol·L-1的NaOH溶液,则该同学需取
②假设该同学用新配制的盐酸中和含0.4gNaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是
A.浓盐酸挥发,浓度不足
B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线
D.加水时超过刻度线,用胶头滴管吸出
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】阅读下列科普短文并填空:
海洋约占地球表面积的 ,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如
,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和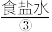 用以生产
用以生产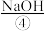 、
、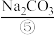 、
、 、
、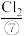 、
、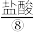 等,苦卤经过氯气氧化,热空气吹出、
等,苦卤经过氯气氧化,热空气吹出、 吸收等一系列操作可获得
吸收等一系列操作可获得 。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
(1)实验室可用_______ 、_______ (填化学式)溶液检验①中的阴离子。
(2)实验室可用MnO2与⑧的浓溶液在加热条件下制取⑦,请写出其离子方程式_______ ,100mL 12 mol·L-1的盐酸溶液与足量的MnO2反应实际生成的气体体积(标准状况下)_______ 6.72L(填“>”、“<”或“=”)。
(3)实验室需要220 mL 0.1 mol·L-1 ⑤的溶液,应该用托盘天平称取Na2CO3·10H2O晶体质量为_______ g;配制溶液所需仪器除烧杯、量筒、玻璃棒、胶头滴管外,还必须用到的一种玻璃仪器为_______ 。
(4)下列操作使配制的溶液物质的量浓度的偏低的是_______。
(5)海水提溴的过程中涉及的反应有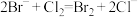 ,
, ,根据上述反应可判断
,根据上述反应可判断 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为_______ 。潮湿的Cl2和SO2都具有漂白性,将其混合后其漂白性_______ (填“增强”、“减弱”或“无影响”)
海洋约占地球表面积的
 ,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如
,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和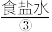 用以生产
用以生产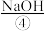 、
、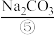 、
、 、
、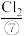 、
、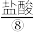 等,苦卤经过氯气氧化,热空气吹出、
等,苦卤经过氯气氧化,热空气吹出、 吸收等一系列操作可获得
吸收等一系列操作可获得 。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。(1)实验室可用
(2)实验室可用MnO2与⑧的浓溶液在加热条件下制取⑦,请写出其离子方程式
(3)实验室需要220 mL 0.1 mol·L-1 ⑤的溶液,应该用托盘天平称取Na2CO3·10H2O晶体质量为
(4)下列操作使配制的溶液物质的量浓度的偏低的是_______。
| A.定容时俯视刻度线 |
| B.转移前,容量瓶内有蒸馏水 |
| C.定容时水加多了用胶头滴管吸出 |
| D.称量是将砝码放在托盘天平的左盘(托盘天平1g以下用游码) |
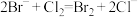 ,
, ,根据上述反应可判断
,根据上述反应可判断 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为
您最近一年使用:0次

 0
0

